Carbazool: eigenschappen, productie en toepassingen

Carbazool is een heterocyclische aromatische koolwaterstof met de chemische formule C12H9N. Het werd voor het eerst geïsoleerd uit steenkoolteer in 1872 door Graebe en Glaser. De structuur ervan bevat een dibenzopyrrool bestaande uit een vijfringige stikstofbevattende ring gefuseerd aan twee benzeenringen.
Inhoudsopgave
1. Fysieke eigenschappen van carbazool
Carbazool is een witte tot lichtgele kristallijne vaste stof met een duidelijke geur. De belangrijkste fysieke eigenschappen zijn:
- Molaire massa: 167,21 g/mol
- Smeltpunt: 246 °C
- Kookpunt: 354,8 °C bij 101,3 kPa
- Dichtheid: 1,1035 g/cm³ bij 18 °C
- Kristalmorfologie: platen of tafels; sublimeerbaar
- Oplosbaarheid:
- Zeer oplosbaar: aceton, pyridine
- Matig oplosbaar: di-ethylether, ethanol
- Licht oplosbaar: chloroform, azijnzuur, koolstoftetrachloride en koolstofdisulfide
- Zeer oplosbaar: geconcentreerd zwavelzuur
- Praktisch onoplosbaar: water (≈ 1 mg/L bij 25 °C)
- Thermodynamische eigenschappen:
- Smeltwarmte: 176,3 kJ/kg
- Verbrandingswarmte: 3,719 × 104 kJ/kg bij 25 °C
2. Chemische reactiviteit van carbazool
Carbazool vertoont diverse reactiviteit vanwege zijn aromatische aard en het vrije elektronenpaar op zijn stikstofatoom. Hier is een overzicht van zijn belangrijkste chemische reacties:
1. N-substitutie en alkylering
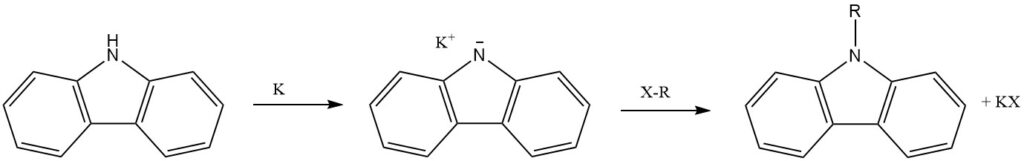
De N-waterstof van carbazole, die als secundair amine fungeert, ondergaat gemakkelijk substitutie met alkalimetalen (Li, Na en K). Dit leidt tot de introductie van andere functionele groepen via verdere reacties.
Het N-atoom van carbazole kan worden gealkyleerd, waarbij N-alkylsubstituenten met verschillende eigenschappen worden geïntroduceerd.
2. Halogenering, nitrering en sulfonering

Elektrofiele substitutiereacties zoals halogenering, nitrering en sulfonering richten zich bij voorkeur op de 3- en 6-posities op de carbazolring vanwege hun hogere elektronendichtheid. Er zijn zware omstandigheden nodig voor verdere substitutie op de 1-, 8- en andere posities, wat leidt tot 1,3,6- en 1,3,6,8-derivaten.
Het kan ook alkylerings– en acyleringsreacties ondergaan op de aromatische ring.
3. Hydrogenering
Carbazool ondergaat gemakkelijk hydrogenering, wat gedeeltelijk of volledig verzadigde derivaten oplevert. Afhankelijk van de reactieomstandigheden kan 1,2,3,4-tetrahydro-, hexahydro- of zelfs dodecahydrocarbazool worden gevormd.
4. Oxidatie
Oxidatie met sterke oxidatiemiddelen zoals chromaten of permanganaten splitst de aromatische ring, waarbij verschillende dicarbazylproducten worden gevormd, afhankelijk van de splitsingsplaats. 3,3′-dicarbazyl wordt gevormd door chromaatoxidatie, terwijl 9,9′-dicarbazyl wordt verkregen door oxidatie met permanganaat.
5. Carboxylering

Behandeling met alkalimetaalcarbonaten en koolstofdioxide kan carbonzuurgroepen op de carbazolring introduceren. De positie van de carboxylgroep (3- of 1-) is afhankelijk van de reactietemperatuur.
3. Productie van carbazool
Belangrijkste punten:
- Carbazool is gemakkelijk verkrijgbaar in steenkoolteer en kan worden gescheiden van antraceen met behulp van verschillende methoden.
- Er bestaan synthetische routes, maar deze zijn momenteel minder concurrerend dan de winning van steenkoolteer.
- Moderne hogetemperatuursmeltkristallisatie biedt een veelbelovende aanpak voor duurzame carbazoolproductie
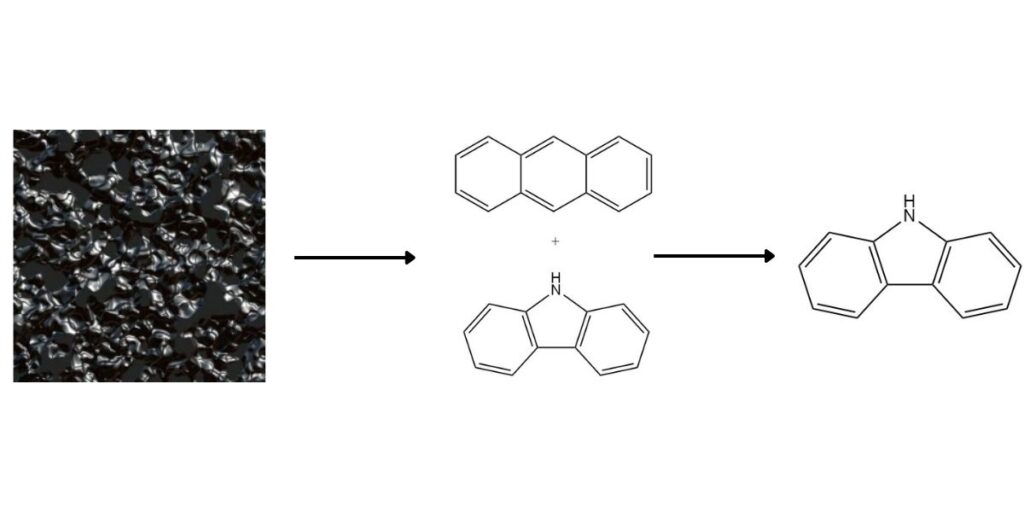
Carbazool is als waardevolle heterocyclische aromatische verbinding aanwezig in hogetemperatuurkoolteer in een gemiddelde concentratie van 0,9%. Hoewel het traditioneel wordt verkregen als een co-product tijdens de productie van antraceen, bieden verschillende methoden een specifieke carbazool-terugwinning.
1. Scheiding van antraceen:
Het hogere kookpunt en de differentiële oplosbaarheid van carbazool vergemakkelijken de scheiding van antraceen. Veelvoorkomende methoden zijn:
- Extractie of complexvorming: Gebruikmaken van oplosmiddelen zoals pyridine, ketonen, benzeen/methanol-mengsels, of specifieke middelen zoals N-methylpyrrolidon, dimethylacetamide, dialkylsulfoxiden of dialkylformamiden.
- Azeotropische destillatie: Gebruikmaken van ethyleenglycol om de vorming van een azeotroop met carbazool te benutten, waardoor scheiding door fractionele destillatie mogelijk wordt.
- Selectieve hydrogenering: Anthraceen omzetten in gehydrogeneerde derivaten terwijl carbazool onaangetast blijft.
2. Chemische scheiding:
Historisch gezien werden methoden zoals kaliumhydroxide of geconcentreerde zwavelzuurfusie gebruikt voor carbazool-scheiding. Hun economische levensvatbaarheid is echter afgenomen.
3. Zuivering uit pyridinemoederlogen:
Pyridinemoederlogen die ontstaan tijdens de zuivering van antraceen kunnen worden geconcentreerd en geherkristalliseerd uit chloorbenzeen om zuiver carbazool te verkrijgen.
4. Synthetische routes voor carbazol
Er bestaan verschillende synthetische methoden voor de productie van carbazool, maar hun industriële betekenis is beperkt vergeleken met de winning van steenkoolteer:
- Conversie van cyclohexanonazine naar octahydrocarbazool gevolgd door dehydrogenering.
- Reductieve cyclisatie van 2-nitrobifenyl.
- Dehydrogenering en cyclisatie van verschillende precursors zoals difenylamine, o-aminobifenyl of N-cyclohexylideenaniline.
Een moderne en efficiënte methode voor het terugwinnen van carbazoolen uit steenkoolteer is oplosmiddelvrije, hoge-temperatuur smeltkristallisatie. Dit proces biedt voordelen in termen van milieu-impact en kosteneffectiviteit.
4. Toepassingen van carbazool
Hoewel carbazool voornamelijk wordt gewonnen uit steenkoolteer (jaarlijks meer dan 3.500 ton), wordt het gebruikt in verschillende industrieën, waaronder: kleurstoffen en pigmenten, pesticiden en polymeren, optische materialen en lichtgevende diodes en in de bouw en lijmen.
Kleurstoffen en pigmenten:
- Hydronblauw: de condensatie van carbazool met p-nitrosofenol en daaropvolgende sulfurisatie levert deze commercieel belangrijke blauwe zwavelkleurstof op.
- Naftol AS en antrachinon Kleurstoffen: Carbazool dient als een voorloper voor verschillende azo- en antrachinonkleurstoffen die worden gebruikt in textiel- en industriële toepassingen.
- Styrylkleurstoffen: N-ethylcarbazool maakt de synthese mogelijk van levendige styrylkleurstoffen die worden gebruikt in verschillende materialen en producten.
- Dioxazinekleurstoffen en pigmenten: N-ethyl-3-aminocarbazool speelt een sleutelrol bij het creëren van deze waardevolle kleurstoffen voor organische pigmenten en azinekleurstoffen.
- Carbazool draagt bij aan de productie van de reactieve kleurstoffen, bekend om hun sterke binding aan synthetische vezels.
Pesticiden en polymeren:
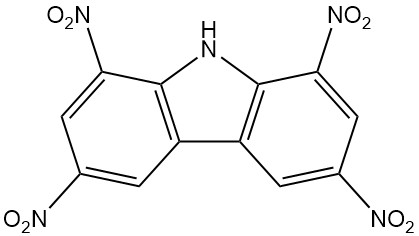
- Nirosan: 1,3,6,8-tetranitrocarbazool, een effectief insecticide, is sinds 1939 commercieel verkrijgbaar.
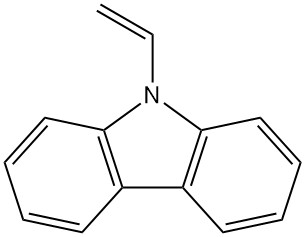
- Poly(vinylcarbazool): N-vinylcarbazoolpolymerisatie levert dit thermisch en chemisch stabiele polymeer (Luvican, Polectron) op dat wordt gebruikt voor elektrische toepassingen vanwege het lage diëlektrische verlies en de fotogeleiding.
Optische materialen en lichtgevende diodes:
- Fotorefractieve materialen: Methacrylaatcarbazoolpolymeren combineren fotogeleiding en elektro-optische eigenschappen, waardoor ze ideaal zijn voor gegevensopslag met hoge dichtheid, beeldverwerking en computing.
- Triplet-emitters: Carbazoolverbindingen worden gebruikt als hostmaterialen voor triplet-emitters in organische lichtgevende diodes (OLED’s), waardoor hun efficiëntie en helderheid worden verbeterd.
Constructie en kleefstoffen:
- Novolakharsen: Carbazool reageert met fenolen en formaldehyde om deze hittebestendige polymeren te vormen, waardevol voor lijmen en coatings.
- Betonweekmakers: Cocondensatie van carbazool met fenolen en formaldehyde, gevolgd door sulfonering, levert effectieve weekmakers voor beton op.
Hoge-prestatiepolymeren:
Thermische condensatie van 3,6-diaminocarbazool met dicarbonzuren produceert elastische en thermisch stabiele polyamiden met diverse toepassingen.
5. Carbazoolderivaten

| Derivaat | CAS-nummer | Formule | Molaire massa (g/mol) | Smeltpunt (°C) | Synthese |
|---|---|---|---|---|---|
| N-ethylcarbazool | 86-28-2 | C14H13N | 195,27 | 68 | Ethylering van carbazol met di-ethylsulfaat |
| 1,3,6,8-tetranitrocarbazool | 4543-33-3 | C12H5O8N5 | 347,20 | 312 | Nitratie van carbazol met salpeterzuur en zwavelzuur |
| N-vinylcarbazool | 1484-13-5 | C14H11N | 193,25 | 65 | Uit carbazol-kalium met ethyleenoxide of vinylchloride, of uit carbazol en acetyleen |
6. Toxicologie van carbazool
Carbazool vertoont een lage acute orale toxiciteit, met LD50-waarden van meer dan 5000 mg/kg bij ratten. Intraperitoneale toediening bij muizen laat echter een significant lagere LD50 van 200 mg/kg zien, wat wijst op routeafhankelijke toxiciteit.
Beroepsmatige blootstelling aan carbazool is in verband gebracht met folliculitis en comedo’s, hoewel dierstudies een minimaal potentieel voor huid- en oogirritatie aantonen, zelfs onder fotoactivatie.
Carbazol ondergaat glucuronidatie en daaropvolgende uitscheiding via de urine bij ratten en konijnen.
Hoge dosering carbazool (270-1050 mg/kg lg/dag) gedurende 96 weken induceerde lever- en voormaagcarcinomen bij B6C3F1-muizen, maar er werd geen tumorigene activiteit waargenomen bij pasgeboren muizen na intraperitoneale injecties.
Op basis van beperkt bewijs wordt carbazool door het International Agency for Research on Cancer (IARC) geclassificeerd als Groep 3 (niet classificeerbaar wat betreft carcinogeniciteit voor mensen). Het had geen mutagene activiteit in verschillende bacteriële testen.
9-Ethylcarbazool, een derivaat, vertoonde een zwak mutageen effect in één bacteriestam, maar was inactief in een andere, wat duidt op een beperkt mutageen potentieel.
Dermale toediening van carbazool tot 250 mg/kg lichaamsgewicht/dag tijdens de zwangerschap veroorzaakte geen afwijkingen in de ontwikkeling van de rattenfoetus.
Referenties
- Carbazole; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a05_059.pub2
- Carbazole; – https://www.sigmaaldrich.com/US/en/product/sigma/c5132
- https://en.wikipedia.org/wiki/Carbazole
