o-Cresolo: proprietà, reazioni, produzione e usi
Cos’è l’o-cresolo?
L’o-cresolo, noto anche come 2-metilfenolo, è un composto organico con formula chimica C7H8O. È un solido cristallino incolore a temperatura ambiente con odore fenolico ed è altamente solubile nella maggior parte dei solventi organici.
Sommario
1. Proprietà fisiche dell’o-cresolo
L’o-cresolo puro è un solido cristallino incolore a temperatura ambiente; tuttavia, assume una colorazione che va dal giallo al marrone dopo un periodo di conservazione prolungato. L’o-cresolo ha un odore fenolico e assorbe l’umidità dall’aria.
L’o-cresolo è altamente solubile in fenolo e in molti solventi organici come alcoli alifatici, eteri, cloroformio e glicerolo, ed è meno solubile in acqua rispetto al fenolo.
L’o-cresolo può essere distillato con vapore e forma azeotropi con diversi composti, ad esempio decano, 1-decene, 1-undecene, dodecano, 1,2,4,5-tetrametilbenzene, divinilbenzene, glicole etilenico, dietilenglicole metilico ed etere etilico.
Le principali proprietà fisiche dell’o-cresolo sono riassunte nella seguente tabella:
| Proprietà | Valore |
|---|---|
| Numero CAS | [95-48-7] |
| Formula chimica | C7H8O |
| Peso molecolare | 108,14 g/mol |
| Punto di fusione a 101,3 kPa | 30,99 °C |
| Punto di ebollizione a 101,3 kPa | 191,00 °C |
| Densità a 25 °C | 1,135 g/cm3 |
| Densità a 50 °C | 1,0222 g/cm3 |
| Viscosità a 50 °C | 3,06 mPa·s |
| Indice di rifrazione a 50 °C | 1,5310 |
| Costante dielettrica a 50 °C | 6,00 |
| Conduttanza specifica a 50 °C | 0,43×10-10 S/cm |
| Tensione superficiale a 50 °C | 34,4×10-6 N/m |
| Costante di dissociazione a 25 °C | 4,8×10-11 |
| Temperatura critica | 424,4 °C |
| Pressione critica | 5,01 MPa |
| Densità critica | 384 kg/m3 |
| Capacità termica cp a 25 °C (gas) | 127,3 J mol-1 K-1 |
| Capacità termica cp a 25 °C (solido) | 154,7 J mol-1 K-1 |
| Capacità termica cp a 50 °C (liquido) | 237,9 J mol-1 K-1 |
| Entalpia di fusione ΔHm al punto di fusione, 101,3 kPa | 15,830 kJ/mol |
| Entalpia di sublimazione ΔHsub a 25 °C, 101,3 kPa | 76,07 kJ/mol |
| Entalpia di vaporizzazione ΔHv al punto di ebollizione, 101,3 kPa | 45,222 kJ/mol |
| Entalpia di combustione ΔH°c a 25 °C, 101,3 kPa | - 3696 kJ/mol |
| Entalpia di formazione ΔH°f a 25 °C, 101,3 kPa | -204,8 kJ/mol |
| ΔH°f a 25 °C (gas), 101,3 kPa | - 128,7 kJ/mol |
| Energia libera di formazione ΔG°f a 25 °C, 101,3 kPa | - 55,7 kJ/mol |
| ΔG°f a 25 °C (gas) e 101,3 kPa | - 33,0 kJ/mol |
| Entropia S a 25 °C e 101,3 kPa | 165,5 J mol-1 K-1 |
| Entropia S° a 25 °C (gas) e 101,3 kPa | 352,8 J mol-1 K-1 |
| Solubilità in acqua a 25 °C | 2,6% in peso |
| Solubilità in acqua a 100 °C | 4,8% in peso |
| Coefficiente di distribuzione log P ottanolo/acqua a 25 °C | 1,95 |
| Densità di vapore (aria = 1) | 3,72 |
| Punto di infiammabilità (vaso chiuso) | 81 °C |
| Temperatura di accensione | 555 °C |
| Limite di infiammabilità, inferiore, in aria a 20 °C, 101,3 kPa | 1,3 vol% |
2. Reazioni chimiche dell’o-cresolo
L’o-cresolo è chimicamente simile al fenolo. È un acido debole e si dissolve in soluzioni alcaline acquose per formare sali stabili in acqua noti come o-cresolati. Pertanto, possono essere estratti in una soluzione di idrossido di sodio da solventi non miscibili con acqua.
Il gruppo ossidrilico dell’o-cresolo può essere eterificato con alogenuri alchilici, dialchilsolfati, dialchilcarbonati ed esteri dell’acido toluensolfonico e reagire con anidridi aciliche o cloruri acilici per formare i corrispondenti esteri tolilici, che sono normalmente chiamati esteri “o-cresilici”.
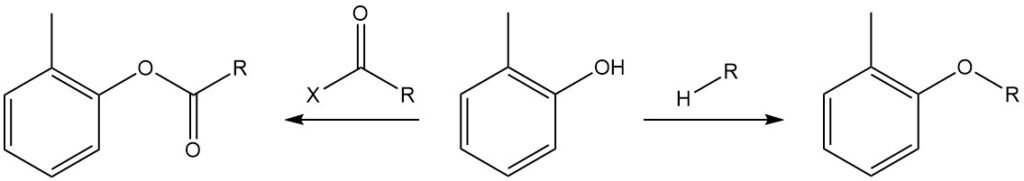
Il gruppo OH dell’o-cresolo reagisce con gli isocianati per formare uretani.
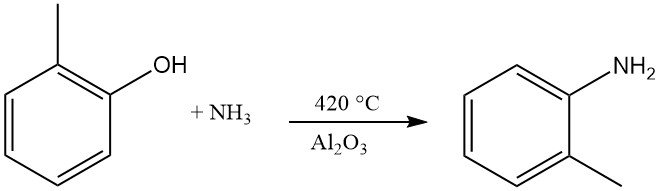
L’o-toluidina si forma per reazione dell’o-cresolo con ammoniaca a una temperatura di 420 °C e in presenza di Al2O3.
Diversi 2-alogenotolueni possono essere ottenuti sostituendo il gruppo ossidrilico dell’o-cresolo. Esempi includono la reazione con ossitetrafluoruro di zolfo a 150 °C, con tricloruro di difenilfosfina a 220 °C o con tribromuro di fosforo a 280 °C per produrre rispettivamente il corrispondente 2-fluoro-, 2-cloro- o 2-bromotoluene.
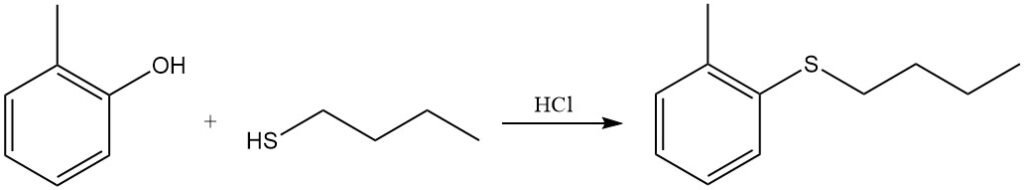
Il gruppo OH fenolico dell’o-cresolo può essere sostituito da un gruppo tiobutile per reazione con butantiolo in acido cloridrico.
Il toluene si ottiene per distillazione del cresolo con polvere di zinco e può anche essere formato per idrogenazione in fase vapore a 300-400 °C sotto pressione (fino a 8 MPa) in presenza di catalizzatori (metalli di transizione e ossido di alluminio).
L’idrodealchilazione dell’o-cresolo a fenolo può essere ottenuta utilizzando catalizzatori a 400-500 °C o per via puramente termica a 500-700 °C.
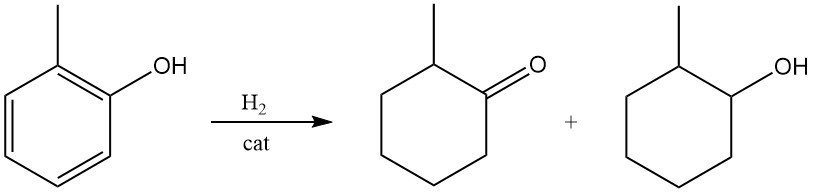
Il 2-metilcicloesanone o il 2-metilcicloesanolo possono essere formati in condizioni blande mediante idrogenazione dell’o-cresolo su catalizzatori a base di nichel Raney o metalli nobili.
L’o-cresolo è sensibile all’ossidazione e, a seconda dell’agente ossidante e delle condizioni di reazione, produce un gran numero di composti come idrochinoni, chinoli, chinoni, chetoni ciclici, furani, cresoli dimerici e trimerici ed eteri tolilici.
Se il gruppo ossidrilico dell’o-cresolo è protetto mediante esterificazione o eterificazione, il gruppo metilico può essere selettivamente mono-, di- o triclorurato, oppure ossidato selettivamente a un gruppo formilico (ad esempio, con biossido di manganese o ossigeno) o a un gruppo carbossilico (acido salicilico) con una soluzione di permanganato acido.
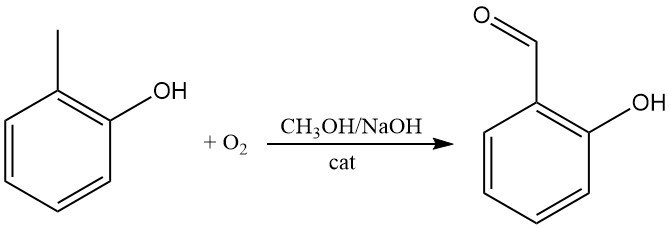
L’o-cresolo può essere ossidato direttamente con ossigeno per dare 2-idrossibenzaldeide, ad esempio, in idrossido di sodio metanolico in presenza di quantità catalitiche di tetraarilporfine di ferro.
La fusione alcalina dell’o-cresolo in presenza di ossido di piombo o biossido di manganese produce direttamente acido 2-idrossibenzoico.
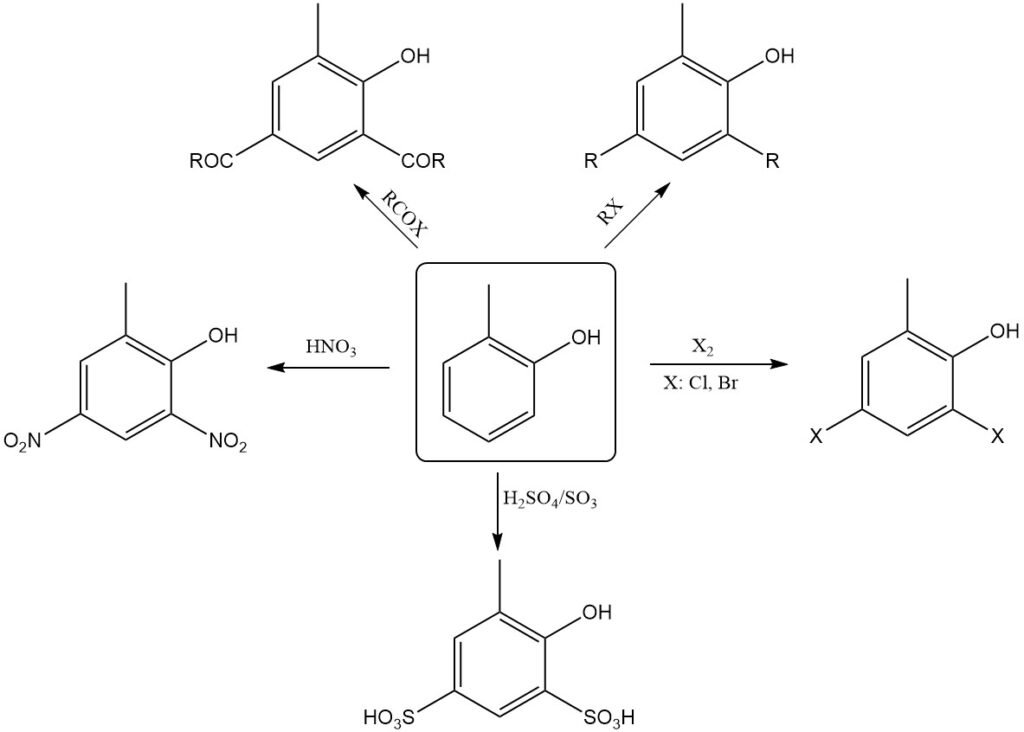
Similmente al fenolo, l’o-cresolo subisce facilmente sostituzione elettrofila principalmente nelle posizioni o e p rispetto al gruppo ossidrilico. Pertanto, può essere nitrato anche con acido nitrico diluito.
Nitrosazione, alogenazione, solfonazione, alchilazione e acilazione avvengono facilmente. Quando l’o-cresolo viene riscaldato con catalizzatori di Friedel-Crafts, come AlCl3, isomerizza a m-cresolo, l’isomero più stabile dal punto di vista termodinamico.
Il riscaldamento di o-cresolati secchi di metalli alcalini con CO2 sotto pressione produce acidi idrossi(metil)benzoici (reazione di Kolbe-Schmitt).
La reazione della formaldeide con o-cresolo in presenza di alcali a temperatura ambiente produce alcoli idrossi(metil)benzilici, che in condizioni acide o a temperature elevate condensano formando resine ad alto peso molecolare.
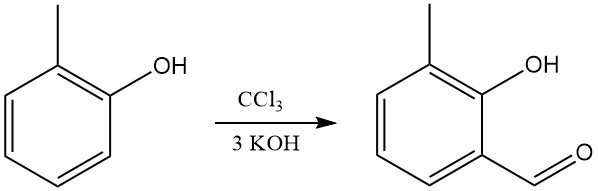
L’o-cresolo reagisce con cloroformio e alcali per formare principalmente o-idrossi(metil)benzaldeidi (sintesi di Reimer-Tiemann).
L’o-cresolo mostra proprietà corrosive aggressive nei confronti di diversi metalli, in particolare a temperature elevate. L’entità della corrosione è influenzata dalla presenza di acqua nella soluzione di cresolo.
Gli acciai inossidabili al cromo-nichel e gli acciai al cromo offrono una resistenza limitata alla corrosione da o-cresolo. Il nichel mostra una resistenza alla corrosione superiore, mentre il tantalio è considerato completamente resistente.
L’alluminio e le sue leghe sono soggetti a grave corrosione, soprattutto a basso contenuto d’acqua, e le leghe di rame e ottone dovrebbero essere evitate a causa della loro suscettibilità alla corrosione.
3. Formazione e isolamento del cresolo
I cresoli (una miscela di isomeri orto, meta e para) venivano storicamente ottenuti esclusivamente dal catrame di carbone. Dopo la Seconda Guerra Mondiale, le sostanze caustiche esaurite delle raffinerie sono emerse come ulteriore fonte. Dalla metà degli anni ’60, la produzione sintetica di cresoli è cresciuta significativamente.
Attualmente, il “cresolo sintetico” rappresenta circa il 60% della domanda negli Stati Uniti, in Europa e in Giappone, mentre il “cresolo naturale”, derivato dal catrame di carbone e dalle sostanze caustiche esaurite delle raffinerie, rappresenta solo il 40% circa.
Una miscela di cresoli, xilenoli e una varietà di altri composti fenolici si trova nelle acque reflue generate dai processi di cracking, nei catrami e nei prodotti simili al catrame derivati dal cracking termico, dal cracking termico ossidativo e dal cracking termico idrogenante di materiali naturali come carbone bituminoso, lignite, scisto bituminoso, torba, legno, lignina e altri biomateriali.
Le rese e le quantità relative di cresoli, xilenoli e altri fenoli prodotti dipendono non solo dal materiale di partenza, ma anche dalle condizioni di processo, tra cui temperatura, tempo di residenza, tipo di reattore e modalità operativa.
Per il carbone bituminoso, l’idrogenazione produce le quantità più elevate, seguita dalla carbonizzazione a bassa temperatura, mentre la coking ad alta temperatura produce le rese più basse. La gassificazione della lignite produce significativamente più fenoli, cresoli e xilenoli rispetto al carbone bituminoso.
Piccole quantità di cresoli, xilenoli e altri derivati fenolici si formano anche durante il cracking catalitico e termico delle frazioni petrolifere, in particolare il cracking termico con coking.
Attualmente, cresoli e xilenoli vengono isolati principalmente dai catrami di carbone ottenuti tramite coking ad alta temperatura, carbonizzazione a bassa temperatura, gassificazione a pressione di Lurgi del carbone e caustici esauriti di raffineria.
3.1. Isolamento del cresolo dai catrami di carbone

Storicamente, il catrame di carbone è stato una fonte significativa di cresoli e xilenoli. Tuttavia, la sua produzione è in costante calo negli ultimi quattro decenni, con una produzione annua stimata tra le 30.000 e le 40.000 tonnellate.
Il catrame di cokeria ad alta temperatura, un sottoprodotto della produzione di coke metallurgico, contiene circa lo 0,4-0,6% di fenolo, lo 0,8-1% di cresoli e lo 0,2-0,5% di xilenoli.
Nel Regno Unito, i cresoli venivano prodotti anche da catrami di carbone a bassa temperatura ottenuti nella produzione di combustibili senza fumo. Tuttavia, la disponibilità di questi catrami è diminuita significativamente negli anni ’90.
Attualmente, la principale fonte di cresoli “naturali” sono i sottoprodotti liquidi ottenuti dalla gassificazione del carbone bituminoso mediante il processo Lurgi. Questo processo è utilizzato principalmente in Sudafrica per la produzione di gas di sintesi per gli impianti Fischer-Tropsch.
I sottoprodotti liquidi di questo processo, la cui composizione è simile a quella dei catrami a bassa temperatura, producono annualmente circa 35.000-55.000 tonnellate di cresoli e xilenoli.
Negli Stati Uniti, i sottoprodotti liquidi dei gassificatori Lurgi della Dakota Gasification Company, che gasifica la lignite per produrre gas naturale sintetico, rappresentano una fonte significativa di cresoli “naturali”. La produzione annua stimata da questa fonte è di circa 5.000 tonnellate di o-cresolo e 11.000 tonnellate di m/p-cresolo.
Per isolare cresoli e xilenoli dal catrame di carbone, si utilizza comunemente l’estrazione con una soluzione di idrossido di sodio. Nel processo Lurgi di fenoraffinazione, l’olio fenolico, che bolle a 180-210 °C, e il filtrato di olio naftalico vengono estratti per ottenere i fenoli.
Gli idrocarburi e le basi piridiniche presenti nella soluzione caustica fenolica grezza vengono rimossi mediante distillazione a vapore, seguita dalla liberazione del fenolo grezzo con anidride carbonica.
Le soluzioni caustiche fenoliche provenienti dagli effluenti delle cokerie, che contengono principalmente fenolo e cresolo con quantità minime di xilenoli, vengono spesso incorporate nel processo di estrazione. Ciò può comportare un’ampia variazione nella composizione del fenolo grezzo risultante.
Ad esempio, il fenolo grezzo ottenuto dal catrame di carbone tedesco da cokeria ad alta temperatura può contenere il 15% di acqua, il 30% di fenolo, il 12% di o-cresolo, il 18% di m-cresolo, il 12% di p-cresolo, l’8% di xilenoli e il 5% di trimetilfenoli, oltre a fenoli altobollenti.
Per purificare ulteriormente le frazioni di acido cresilico da oli neutri, basi di catrame, composti solforati e sostanze fenoliche indesiderate, la Dakota Gasification Co. ha sviluppato una distillazione estrattiva con dietilenglicole.
Aziende come Sasol Phenolics, Merichem Co., Coalite Chemicals, Rütgers-VfT AG, DEZA Corporation e diverse aziende giapponesi utilizzano questo processo per isolare cresoli e xilenoli dal catrame di carbone.
3.2. Recupero del cresolo dai caustici esausti di raffineria
Negli Stati Uniti, cresoli e xilenoli si ottengono dalle frazioni di nafta prodotte durante il cracking catalitico e termico nell’industria petrolifera. Queste frazioni contengono circa lo 0,1% di fenoli C6-C8. Durante il processo di lavaggio per rimuovere i composti solforati da queste frazioni, cresoli e xilenoli vengono estratti anche utilizzando soluzioni alcaline concentrate.
Le caustiche cresilate esauste ottenute da questo processo variano notevolmente in composizione, contenendo tipicamente il 20-25% di fenoli C6-C8 e il 10-15% di composti solforati.
Fino all’inizio degli anni ’90, queste caustiche venivano raccolte e riprocessate da aziende specializzate. Tuttavia, a causa della crescente concorrenza dei produttori di o-cresoli sintetici, delle normative ambientali più severe e della carenza di materie prime, molte di queste aziende hanno chiuso i battenti.
Merichem è attualmente l’unico grande trasformatore di caustiche esauste di raffineria negli Stati Uniti.
Presso Northwest Petrochemical, un ex impianto di trasformazione, i tioli nella soluzione alcalina venivano ossidati con aria per produrre disolfuri, che venivano poi decantati. I fenoli rimanenti venivano precipitati con anidride carbonica e decantati. I fenoli rimanenti venivano estratti con un solvente organico e quindi riestratti con una fase acquosa alcalina.
Questo processo ha prodotto una miscela fenolica contenente circa il 20% di fenolo, il 18% di o-cresolo, il 22% di m-cresolo, il 9% di p-cresolo, il 28% di xilenolo e il 3% di fenoli superiori. Questa miscela è stata poi separata per distillazione.
The Merichem Company utilizza l’acido solfidrico, un prodotto di scarto delle raffinerie, per precipitare i fenoli al posto dell’anidride carbonica. La soluzione di solfuro ottenuta viene concentrata per produrre solfuro di sodio, utilizzato nell’industria cartaria e nella lavorazione dei minerali.
Il condensato di vapore acqueo formatosi durante questo processo viene separato con gas naturale per rimuovere i composti odorigeni e quindi fatto passare attraverso una torre di raffreddamento. Il gas naturale viene utilizzato come combustibile nell’inceneritore dell’aria del processo finale.
L’acqua dell’impianto viene riciclata in un sistema integrato, e la maggior parte dell’acqua viene rilasciata nell’ambiente sotto forma di vapore acqueo dalle torri di raffreddamento.
La Pittsburgh Consolidated Chemical Company utilizzava in precedenza un processo che prevedeva il trattamento diretto delle caustiche esaurite di raffineria con gas di combustione contenenti anidride carbonica. Il fenolo grezzo precipitato veniva quindi distillato ed estratto con una soluzione acquosa di metanolo-nafta leggera.
Dopo aver rimosso i residui tiolici e basici con una resina a scambio ionico, gli acidi cresilici venivano recuperati tramite distillazione frazionata.
La capacità di produzione di cresilici di Merichem era di circa 55.000 tonnellate all’anno nel 1996. Tuttavia, questa cifra include fenolo, xilenoli e altri alchilfenoli. Merichem ha ampliato le sue attività per includere la lavorazione di cresilici da varie fonti, inclusi gli impianti di gassificazione del carbone.
Il recupero di cresoli e xilenoli da caustiche esaurite di raffineria è stato principalmente limitato agli Stati Uniti. In Germania, diverse tecniche di raffinazione e la produzione di caustiche esaurite contenenti cresolo potrebbero non essere adatte a un riprocessamento economico. Inoltre, il passaggio all’idrotrattamento e al processo Merox nelle raffinerie ha ridotto la produzione di caustiche esaurite e il recupero di cresoli.
4. Produzione industriale di o-cresolo
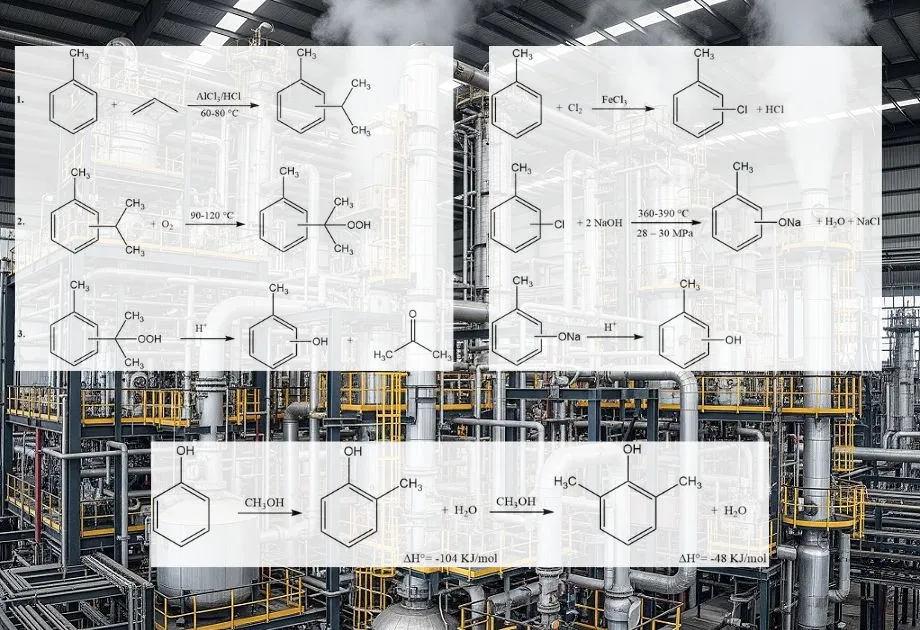
L’orto-cresolo (o-cresolo) viene prodotto principalmente attraverso metodi di sintesi, poiché il recupero tradizionale dal catrame di carbone e dalle sostanze caustiche di raffineria non è sufficiente a soddisfare la domanda globale. Questi processi producono una miscela di isomeri del cresolo. Da queste miscele, solo l’o-cresolo può essere separato come prodotto puro per distillazione.
Vengono impiegati diversi processi industriali, spesso a partire da toluene o fenolo:
- Metilazione del fenolo in fase vapore: Questo è un metodo industriale ampiamente diffuso. Il fenolo reagisce con il metanolo in fase gassosa su un catalizzatore acido solido, come allumina, ossido di magnesio o ossido di gallio. La reazione avviene tipicamente a temperature elevate (ad esempio, 200-400 °C). Questo processo produce selettivamente o-cresolo e 2,6-xilenolo.
- Idrolisi alcalina del clorotoluene: Questo metodo prevede l’idrolisi del 2-clorotoluene in un mezzo alcalino. L’atomo di cloro viene sostituito da un gruppo ossidrilico, portando alla formazione di o-cresolo. Questo processo può produrre una miscela di isomeri del cresolo, con rapporti variabili a seconda delle condizioni specifiche e dei catalizzatori utilizzati.
- Fusione alcalina di toluensolfonati: Questo processo utilizza il toluene come materia prima, che viene prima solfonato per formare acido toluensolfonico. Il sale sodico dell’acido toluensolfonico subisce quindi una fusione alcalina (reazione con idrossido di sodio fuso) per produrre cresossido di sodio, che viene successivamente acidificato per produrre cresolo.
- Scissione del cimene idroperossido: Questo processo, sempre a partire dal toluene, prevede la formazione di cimene (isopropiltoluene), che viene poi ossidato a cimene idroperossido. La successiva decomposizione acido-catalizzata (scissione) del cimene idroperossido produce cresolo e acetone.
Per un articolo completo e dettagliato sulla produzione di cresolo, consultare l’articolo seguente.
5. Usi dell’o-cresolo
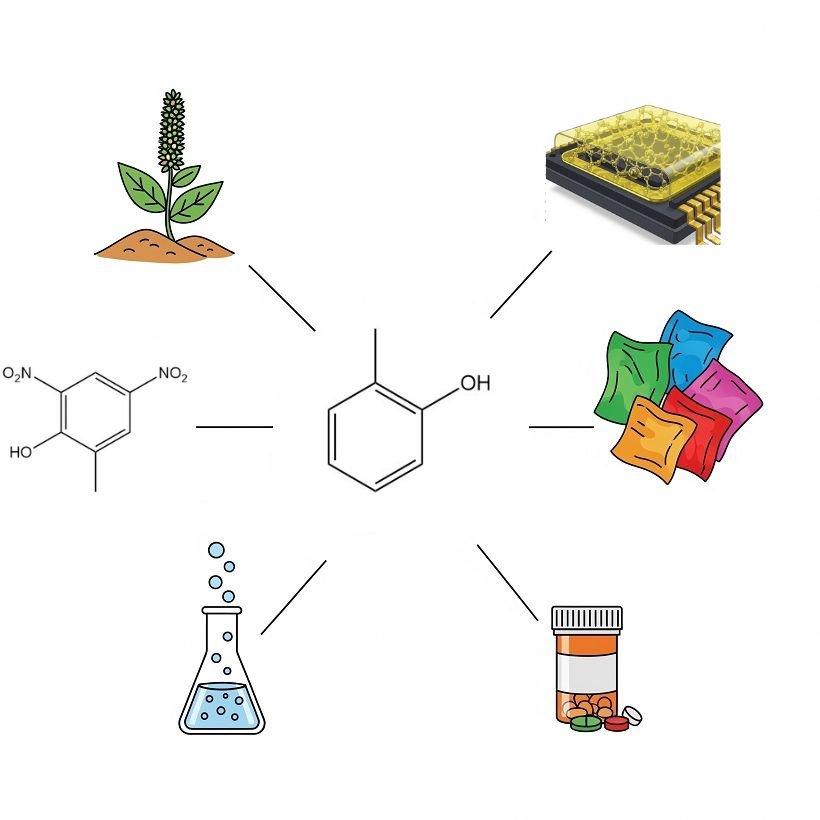
L’o-cresolo funge da intermedio chimico versatile e solvente in diversi settori industriali.
Una delle principali applicazioni in Europa riguarda la sua clorurazione a 4-cloro-o-cresolo, utilizzato come precursore per gli acidi clorofenossialcanoici, tra cui l’acido 4-cloro-2-metilfenossiacetico, l’acido 2-(4-cloro-2-metilfenossi)-propionico e l’acido γ-(4-cloro-2-metilfenossi)butirrico, tutti noti come erbicidi selettivi.
Una quantità minore di o-cresolo viene sottoposta a nitrazione per produrre 4,6-dinitro-o-cresolo. Questo derivato presenta proprietà sia erbicide che insetticide. Viene anche utilizzato come inibitore di polimerizzazione durante la produzione e la distillazione dello stirene.
L’o-cresolo ad elevata purezza è sempre più utilizzato, soprattutto in Giappone, nella produzione di resine novolacche epossidiche-o-cresoliche (resine ECN). Queste resine vengono impiegate come materiali di tenuta per circuiti integrati. L’o-cresolo di qualità standard viene utilizzato nella modifica delle resine fenolo-formaldeide convenzionali.
L’o-cresolo è anche un importante precursore per vari intermedi coloranti. Quantitativamente, l’acido o-cresotinico (acido o-idrossimetilbenzoico), sintetizzato tramite la reazione di Kolbe, è il più significativo. Questo acido viene successivamente utilizzato nella produzione farmaceutica, mentre i suoi esteri metilici vengono utilizzati come ausiliari di tintura.
Una quantità considerevole di o-cresolo viene utilizzata come solvente, direttamente o previa idrogenazione a 2-metilcicloesanolo o 2-metilcicloesanone. La sua forma di estere carbonato funge da materiale di partenza nella sintesi della cumarina.
L’alchilazione dell’o-cresolo con propene produce carvacrolo (3-isopropil-6-metilfenolo), impiegato come antisettico e nelle fragranze.
Quantità minori di o-cresolo vengono alchilate con isobutene, fungendo da materiale di partenza per diversi antiossidanti, componenti per materiali di registrazione termica e prodotti farmaceutici, come il miorilassante Mephenesin.
Riferimenti
- Cresols and Xylenols; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/abs/10.1002/14356007.a08_025
- Cresols; Encyclopedia of Toxicology, Volume 1. – https://www.sciencedirect.com/science/article/abs/pii/B9780123864543002967
