Alcol allilico: proprietà, produzione, reazione e usi
Cos’è l’alcol allilico?
L’alcol allilico è un composto organico con formula chimica C3H6O. È un liquido limpido e incolore con un odore pungente, simile all’aglio, ed è classificato sia come alcol primario che come alcol insaturo a causa della presenza di un doppio legame nella sua struttura molecolare.
Il doppio legame si trova tra il secondo e il terzo atomo di carbonio nella molecola e il gruppo idrossile (-OH) è attaccato al primo atomo di carbonio.
Sommario
1. Proprietà fisiche dell’alcol allilico
L’alcol allilico (nome IUPAC: prop-2-en-1-olo) è un liquido incolore e mobile dall’odore irritante. Ha una formula molecolare di C3H6O e una massa molare di 58,08 g/mol. Il punto di fusione è -129 °C e il punto di ebollizione è 96,9 °C (101,3 kPa). L’alcol allilico è miscibile con acqua e solventi organici.
| Proprietà | Valore |
|---|---|
| Densità relativa |
|
| Indice di rifrazione |
|
| Temperatura critica | Tcrit = 271,9 °C |
| Calore di vaporizzazione a 101,3 kPa | 39,98 kJ/mol |
| Calore specifico del vapore | Cp (g), (20 °C e 101,3 kPa) = 2,428 kJ/kg.K |
| Calore specifico del liquido | Cp (l), (20,5 – 95,5 °C) = 2,784 kJ/kg.K |
| Calore di combustione a p costante | 1853,8 kJ/mol |
| Viscosità |
|
| Tensione superficiale |
|
| Momento di dipolo | 1,63 D |
| Costante dielettrica | a 16,2 °C, λ = 60 cm : 20,3 |
| Limiti di accensione nell'aria | a 100 °C, 101,3 kPa = 2,5 – 18,0 vol % |
| Punto di infiammabilità (vaso chiuso) | 22,2 °C |
L’alcol allilico è miscibile con acqua e solventi organici in tutte le proporzioni a 20 °C. Forma azeotropi binari con acqua, benzene, etere diallilico, cloruro di allile, tricloroetilene e azeotropi ternari con (acqua, benzene) e (acqua, etere diallilico).
2. Reazioni chimiche dell’alcol allilico
L’alcol allilico è un composto versatile che può subire una varietà di reazioni, tra cui reazioni di ossidazione, riduzione, idrogenazione, condensazione e addizione.
A temperatura ambiente, l’alcol allilico è stabile sotto forma di sostanza liquida. Tuttavia, riscaldando l’alcol allilico a temperature superiori a 100 °C si ottiene la creazione di polimeri solubili in acqua (alcoli poliallilici), che reagiscono con acidi alchenoici per produrre oli essiccanti.
Può anche essere innestato su poliimmidi o copolimerizzato con stirene in presenza di ossigeno.
Le schiume poliuretaniche ignifughe sono prodotte tramite reazione di condensazione tra alcol allilico e polieteri metilglucoside, seguita da bromurazione e successiva aggiunta di isocianati.
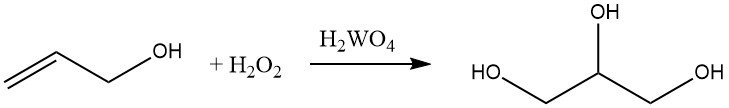
L’alcol allilico può essere idrossilato con perossido di idrogeno in presenza di acido di tungsteno per formare glicerolo. Questa reazione è commercialmente importante per la produzione di glicerolo.
L’idrossilazione mediante idroperossidi organici con un catalizzatore al vanadio produce glicidolo (ossiranilmetanolo), che può essere ottenuto anche tramite la reazione dell’alcol allilico con peracidi.
La deidrogenazione in fase gassosa con aria in presenza di catalizzatori quali palladio, argento o rame porta alla formazione di acroleina.
L’ossidazione in fase liquida dell’alcol allilico mediante un catalizzatore al palladio produce acido acrilico e acroleina con una selettività dell’83%.
L’idrogenazione catalitica dell’alcol allilico produce 1-propanolo.
La clorurazione dell’alcol allilico in una soluzione acquosa produce mono- e dicloridrine di glicerolo che possono essere ulteriormente idrolizzate per produrre glicerolo.
La bromurazione in una soluzione acquosa tamponata da cloruro di calcio determina la formazione di 2,3-dibromo-1-propanolo, un composto utilizzato nei materiali ignifughi.
La reazione dell’alcol allilico con cloruro di allile produce etere diallile (punto di ebollizione: 94 °C), mentre con il cloruro di metallile produce etere di allile metallile.
L’alcol allilico può aggiungersi al tetracloruro di carbonio mediante inizio radicalico per formare 2,4,4,4-tetracloro-1-butanolo (intermedio utilizzato nei ritardanti di fiamma).
Può essere idroformilato in presenza di cobalto carbonile per formare 4-idrossibutirraldeide. Con catalizzatori al complesso di rodio, la resa di 4-idrossibutirraldeide viene migliorata all’80%. L’aldeide può quindi essere idrogenata a 1,4-butandiolo che è un monomero prezioso per la sintesi di poliuretani.
Se l’idroformilazione dell’alcol allilico avviene nella fase vapore utilizzando complessi di trifenilfosfina di rodio supportati su supporti porosi, si ottiene un’elevata resa di tetraidro-2-furanolo (94%).
L’alcol allilico può essere carbonilato in una soluzione di acido acetico con un catalizzatore di cloruro di palladio per formare acido 3-butenoico.
3. Produzione di alcol allilico
L’alcol allilico è in genere prodotto dal propene, che è un idrocarburo gassoso. Esistono diversi modi per produrre alcol allilico dal propene, ma i due metodi più comuni sono: il processo del cloruro di allile e il processo dell’ossido di propilene.
3.1. Produzione di alcol allilico mediante idrolisi del cloruro di allile
L’idrolisi del cloruro di allile è un processo commerciale per la produzione di alcol allilico. Il cloruro di allile viene fatto reagire con una soluzione diluita di idrossido di sodio a 150 °C e 1,3 – 1,4 MPa, producendo alcol allilico all’85 – 95%.
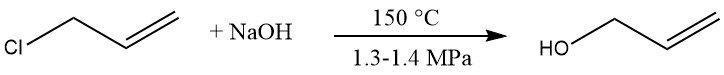
I sottoprodotti sono diallil etere (5-10%), cloropropeni, propionaldeide e materiale altobollente.
Il cloruro di allile e la soluzione acquosa alcalina devono essere miscelati accuratamente per mantenere un valore di pH costante. Il cloruro di allile deve essere convertito quasi quantitativamente perché è corrosivo e non può essere recuperato economicamente. La reazione viene quindi eseguita in un reattore di riciclo, con il nichel come materiale più adatto per il reattore.
Un impianto commerciale per la produzione di alcol allilico mediante idrolisi continua del cloruro di allile è mostrato nella Figura 1. L’acqua viene rimossa dall’alcol allilico grezzo mediante distillazione azeotropica con diallil etere come trascinatore. L’azeotropo alcol allilico grezzo – acqua (alcol allilico al 72%) può essere utilizzato senza ulteriore purificazione per alcune reazioni.
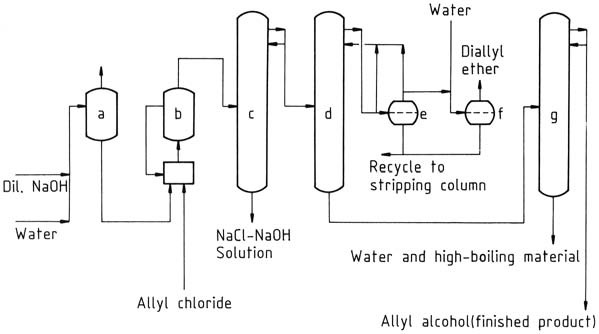
a) Preriscaldatore; b) Reattore di idrolisi con sistema di riciclo; c) Colonna di strippaggio; d) Colonna di disidratazione; e) Separatore; f) Vasca di lavaggio dell'etere diallilico; g) Colonna di purificazione dell'alcol allilico
Ecco alcuni dettagli aggiuntivi sull’idrolisi del cloruro di allile:
- La reazione è esotermica, quindi è importante controllare la temperatura per evitare la formazione di sottoprodotti.
- La reazione è anche corrosiva, quindi è importante utilizzare materiali resistenti alla corrosione per il reattore e le tubazioni.
- I sottoprodotti della reazione possono essere riciclati o venduti come sottoprodotti.
- La fase di distillazione azeotropica viene utilizzata per rimuovere l’acqua dall’alcol allilico grezzo. Questa fase è necessaria per ottenere un prodotto di alcol allilico ad alta purezza.
3.2. Produzione di alcol allilico mediante isomerizzazione dell’ossido di propene
La riorganizzazione catalitica dell’ossido di propene è ora più ampiamente utilizzata nella produzione commerciale rispetto all’idrolisi del cloruro di allile. Il catalizzatore preferito per questa reazione è il fosfato di litio.
Nel processo in fase vapore, il vapore di ossido di propene viene diretto su un catalizzatore al fosfato di litio, con temperature che vanno da 250 a 350 °C. Questo catalizzatore è composto fino al 30% di materiale inerte in una struttura a letto fisso. Le conversioni sono di circa il 70-75%, accompagnate da una selettività allilica del 97%.
Le rese spazio-temporali risultanti sono di 0,5 kg di alcol allilico per litro di catalizzatore all’ora. Olin Mathieson impiega un catalizzatore al fosfato di litio che incorpora l’1% di idrossido alcalino; tuttavia, questo catalizzatore deve essere rigenerato dopo 40 ore mediante lavaggio con acetone.
Un catalizzatore distinto, formulato da Chemische Werke Hüls, contiene il 73,6% di fosfato di litio e il 17,5% di silice, e non richiede alcuna rigenerazione. Sorprendentemente, anche dopo 1200 ore, mantiene una selettività dell’alcol allilico del 97,3%.
Sebbene l’arseniato di litio sia stato suggerito come catalizzatore di isomerizzazione, non offre alcun vantaggio sostanziale rispetto al fosfato di litio. Un metodo precedente, catalizzato dall’ossido di cromo e sviluppato da Wyandotte Chemical Corp., dimostra conversioni e selettività significativamente inferiori.
Nel processo in fase liquida, il processo Progil utilizza un catalizzatore di fosfato di litio finemente macinato sospeso in solventi ad alto punto di ebollizione come il terfenile o l’alchilbenzene. L’ossido di propene viene introdotto nella sospensione a 280 °C.
Questa variante raggiunge un tasso di conversione del 60%, una selettività dell’alcol allilico del 92% e una resa spazio-temporale di 1 kg di alcol allilico per litro all’ora. La durata del catalizzatore varia da 500 a 1000 ore.
Una tecnica comparabile, brevettata da Jefferson Chemical Co., utilizza una miscela di solventi di bifenile e difeniletere.
3.3. Produzione di alcol allilico mediante idrolisi dell’acetato di allile
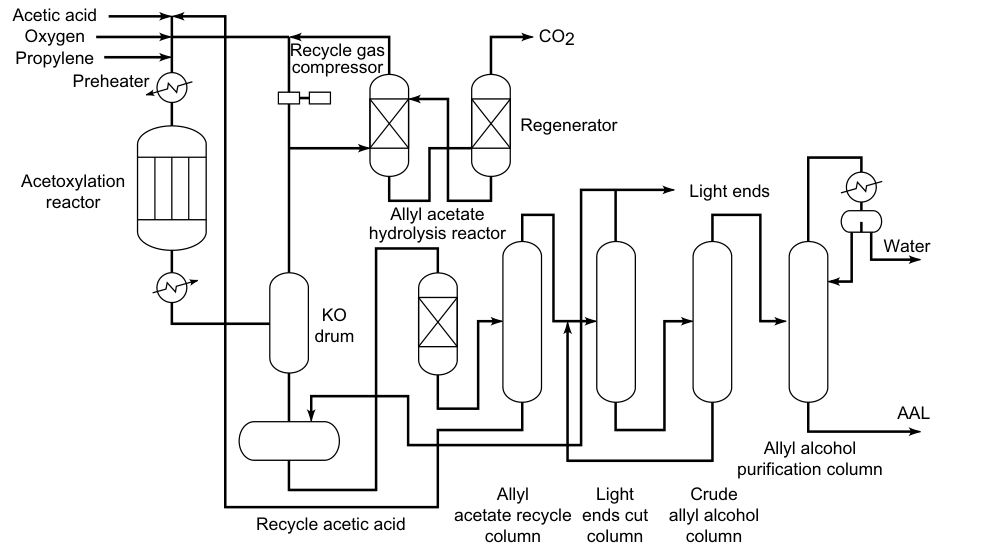
Propene, acido acetico e ossigeno reagiscono in fase gassosa su catalizzatori al palladio per formare acetato di allile:
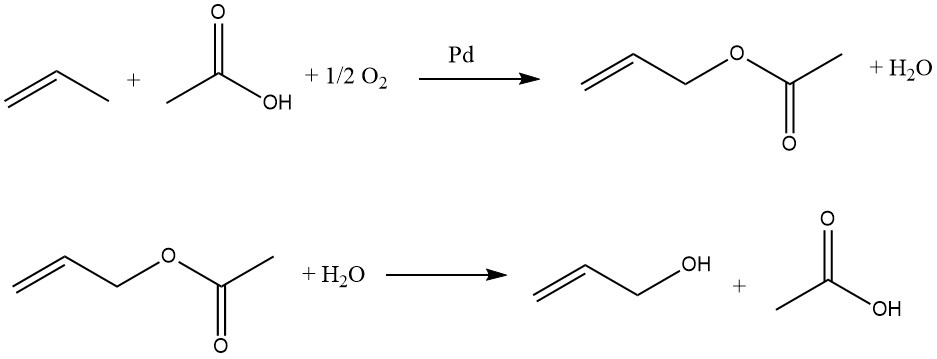
Questa reazione è esotermica, quindi la temperatura del reattore deve essere controllata. L’acetato di allile viene quindi idrolizzato in alcol allilico in un reattore separato. L’acido acetico viene recuperato e riutilizzato nell’ossidazione del propene. Pertanto, solo propene e ossigeno sono necessari come materie prime per la preparazione dell’alcol allilico.
Questo processo non richiede cloro, il che lo rende più ecologico rispetto ad altri metodi di produzione di alcol allilico. L’acetato di allile può essere idrolizzato riscaldandolo a circa 230 °C e 3 MPa.
Nel processo Bayer, l’idrolisi viene eseguita cataliticamente su uno scambiatore cationico acido (polistirene solfonato) a 100 °C. La resa complessiva dell’alcol allilico è del 90%.
3.4. Produzione di alcol allilico mediante idrogenazione dell’acroleina
L’alcol allilico viene sintetizzato mediante idrogenazione catalitica dell’acroleina in fase di vapore. Utilizzando catalizzatori cadmio-zinco è possibile raggiungere una resa fino al 70% e risultati simili possono essere ottenuti utilizzando leghe argento-cadmio supportate su supporti inerti come allumina o silice.
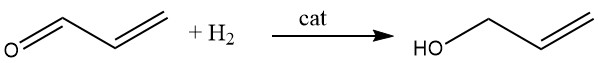
In alternativa, l’acroleina può essere ridotta con etanolo o alcol isopropilico in presenza di una miscela di ossido di magnesio e ossido di zinco. Questa reazione avviene in fase di vapore a 400 °C, con conseguenti rese di alcol allilico fino all’80%.
4. Utilizzi dell’alcol allilico
Gli utilizzi dell’alcol allilico sono i seguenti:
- Produzione di glicerolo: l’alcol allilico è stato inizialmente impiegato come materia prima nella produzione di glicerolo da aziende come Daicel Chemical Company.
- Monomero per Dietilenglicole bis(allilcarbonato): prima del 1985, l’alcol allilico è stato utilizzato come monomero nella produzione di dietilenglicole bis(allilcarbonato), che viene utilizzato nella creazione di lenti ottiche in plastica.
- Produzione di epicloridrina: Showa Denko K.K. ha iniziato a utilizzare l’alcol allilico come precursore nella produzione di epicloridrina, un composto utilizzato in varie applicazioni. Anche altri produttori di epicloridrina hanno preso in considerazione la transizione al processo con alcol allilico.
- Produzione di 1,4-butandiolo: ARCO Chemical Company ha creato un importante impianto di produzione di alcol allilico e ha utilizzato l’alcol allilico come materia prima nella produzione di 1,4-butandiolo. Questa è un’applicazione degna di nota, che segna il primo caso di produzione industriale di 1,4-butandiolo utilizzando alcol allilico.
- Produzione di esteri allilici: l’alcol allilico funge da materia prima primaria per la produzione di esteri allilici, in particolare di diallil ftalati e metacrilato di allile.
- Produzione di etere allilico: l’alcol allilico è utilizzato anche nella produzione di etere allilico, in particolare di etere glicidilico di allile.
- Copolimero di stirene-alcol allilico: un copolimero di stirene-alcol allilico è prodotto da Monsanto Chemical Company. Questo copolimero trova applicazioni in vernici idrosolubili, resine alchidiche e uretani come polioli.
- L’alcol allilico subisce reazioni di copolimerizzazione con altri monomeri per produrre intermedi utilizzati nella fabbricazione di materiali ignifughi o come nematocida, fungicida o conservante.
5. Tossicologia e salute sul lavoro
L’alcol allilico è stato ampiamente studiato per i suoi effetti irritanti e tossici. Il suo odore può essere percepito a circa 0,8 ppm.
Concentrazioni tra 6 e 12 ppm causano irritazione nasale, mentre 25 ppm inducono grave irritazione oculare con sintomi come lacrimazione, sensibilità alla luce, visione offuscata e dolore agli occhi.
Concentrazioni più elevate possono portare a necrosi corneale e cecità temporanea. Gli individui sensibili possono manifestare irritazione oculare a concentrazioni basse come 2-5 ppm.
Negli studi sugli animali, l’inalazione giornaliera di vapori di alcol allilico a concentrazioni da 2 a 7 ppm per 7 ore al giorno per 6 mesi è stata tollerata da cani, conigli, porcellini d’India e ratti.
Il valore limite di soglia (TLV) e la concentrazione massima ammissibile (MAK) per l’alcol allilico sono entrambi fissati a 2 ppm. Il limite di esposizione a breve termine è più alto, a 4 ppm.
L’alcol allilico ha mostrato effetti epatotossici, con necrosi delle cellule epatiche osservata nei ratti dopo somministrazione orale e intraperitoneale. Singole applicazioni orali hanno causato necrosi epatica nei ratti, con conseguenti decessi. La LD50 per i conigli è compresa tra 50 e 80 mg/kg e per i ratti è di 64 mg/kg.
Il contatto cutaneo con l’alcol allilico comporta un rischio di intossicazione sistemica a causa del suo elevato tasso di assorbimento. Anche piccole quantità, come una singola goccia (circa 50 mg), possono causare effetti sistemici insieme a irritazione locale.
I ratti esposti a 50 ppm di alcol allilico nell’acqua potabile per 15 settimane hanno mostrato tolleranza senza effetti avversi evidenti.
Questi risultati evidenziano la natura tossica e irritante dell’alcol allilico, con varie soglie di concentrazione e potenziali effetti su diverse vie di esposizione. Le linee guida sulla sicurezza sul lavoro e i potenziali rischi associati all’esposizione cutanea sono considerazioni importanti quando si maneggia questo composto.
Riferimenti
- Allyl Compounds; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_425
- Allyl Alcohol and Monoallyl Derivatives; Kirk-Othmer Encyclopedia of Chemical Technology. – https://onlinelibrary.wiley.com/doi/10.1002/0471238961.0112122514010701.a01.pub2
