Acido nitrobenzoico: proprietà, reazioni e produzione
Gli acidi nitrobenzoici sono derivati dell’acido benzoico con la formula generale C7H5NO4. Due isomeri (meta e para) sono commercialmente importanti. Gli acidi nitrobenzoici sono circa dieci volte più acidi dell’acido benzoico a causa della presenza del gruppo nitro.
Sommario
Acido 2-nitrobenzoico o acido o-nitrobenzoico

L’acido 2-nitrobenzoico è un acido mononitrobenzoico in cui il gruppo nitro è in posizione orto rispetto al gruppo carbossilico. È un solido insolubile in acqua e solubile in alcol come il metanolo.
Proprietà fisiche dell’acido 2-nitrobenzoico
Le proprietà fisiche dell’acido 2-nitrobenzoico sono elencate di seguito:
- Massa molare = 167,12 g/mol
- Punto di fusione = 148 °C
- Densità = 1,575
- Solubilità in acqua = 0,75 g/100 ml (a 25 °C)
- Solubilità in metanolo = 42,72 g/100 ml (a 10 °C)
- Solubilità in benzene = 0,294 g/100 ml (a 10 °C)
- Costante di dissociazione, Ka (a 18 °C) = 6,1 × 10-3
- Temperatura di decarbossilazione = 180 °C
Reazioni chimiche dell’acido 2-nitrobenzoico
L’acido 2-nitrobenzoico subisce la tipica reazione degli acidi carbossilici aromatici e dei composti nitroaromatici:
L’acido antranilico può essere prodotto dalla riduzione del gruppo nitro in un’ammina.
Il gruppo carbossilico forma esteri con alcoli e cloruro di 2-nitrobenzoile con agenti cloruranti.
A temperature superiori a 180 °C, l’acido 2-nitrobenzoico forma nitrobenze per decarbossilazione.
L’anello aromatico può subire reazioni di sostituzione, ma è difficile a causa della presenza di gruppi disattivanti.
Produzione di acido 2-nitrobenzoico
L’acido 2-nitrobenzoico viene preparato mediante l’ossidazione del 2-nitrotoluene con acido nitrico.

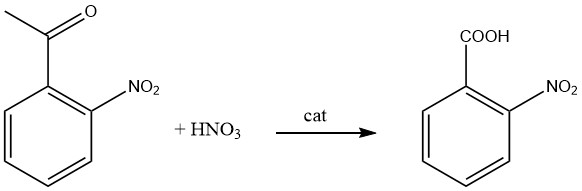
Monsanto Chemicals Ltd. ha sviluppato un metodo di produzione per l’acido 2-nitrobenzoico mediante ossidazione del 2-nitroacetofenone con acido nitrico acquoso in presenza di metavanadato di ammonio come catalizzatore sotto riflusso.
Sono necessarie otto moli di acido nitrico per convertire una mole di 2-nitroacetofenone a una temperatura di 60 °C alla temperatura di riflusso della miscela.
Raffreddando la miscela di reazione, si formano i cristalli grezzi di acido 2-nitrobenzoico che vengono recuperati da essa mediante filtrazione, quindi purificati mediante ricristallizzazione da solventi quali benzene, etanolo, miscele benzene-etanolo, esano, ecc.
Acido 3-nitrobenzoico o acido m-nitrobenzoico

L’acido 3-nitrobenzoico è un solido bianco. I sostituenti carbossilico e nitro sono in posizione meta l’uno rispetto all’altro, motivo per cui è anche chiamato acido m-nitrobenzoico. È un importante precursore nella produzione di coloranti.
Proprietà fisiche dell’acido 3-nitrobenzoico
Le proprietà fisiche dell’acido 3-nitrobenzoico sono elencate di seguito:
- Massa molare = 167,12 g/mol
- Punto di fusione = 142 °C
- Densità = 1,494
- Solubilità in acqua = 0,24 g/100 ml (a 15 °C)
- Solubilità in metanolo = 47,34 g/100 ml (a 10 °C)
- Solubilità in benzene = 0,795 g/100 ml (a 10 °C)
- Costante di dissociazione, Ka (a 25 °C) = 3,48 × 10-4
- Temperatura di decarbossilazione = 238 °C
Reazioni chimiche dell’acido 3-nitrobenzoico
L’acido 3-nitrobenzoico subisce la tipica reazione degli acidi carbossilici aromatici e dei composti nitroaromatici:
L’acido 3-amminobenzoico può essere prodotto dalla riduzione del gruppo nitro in un’ammina.
Il gruppo carbossilico forma esteri con alcoli e cloruro di 3-nitrobenzoile con agenti cloruranti.
A temperature superiori a 238 °C, l’acido 3-nitrobenzoico forma nitrobenze per decarbossilazione.
L’anello aromatico può subire reazioni di sostituzione, ma è difficile a causa della presenza di gruppi disattivanti.
Produzione di acido 3-nitrobenzoico
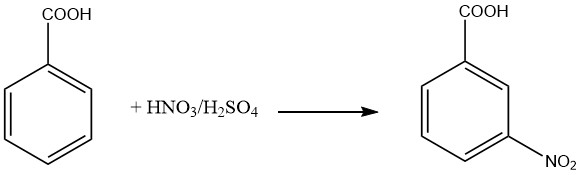
L’acido 3-nitrobenzoico viene preparato mediante la nitrazione dell’acido benzoico in condizioni di bassa temperatura. Durante questo processo, circa il 20% dell’isomero 2-nitro e l’1,5% dell’isomero 4-nitro vengono prodotti insieme all’acido 3-nitrobenzoico desiderato. Per ottenere l’acido 3-nitrobenzoico purificato, può essere impiegata la ricristallizzazione del sale di sodio.
Una resa maggiore di 3-nitrobenzaldeide, un precursore dell’acido 3-nitrobenzoico, può essere ottenuta mediante l’ossidazione controllata della benzaldeide. L’acido 3-nitrobenzoico funge da intermedio nella sintesi dell’acido 3-amminobenzoico e dei coloranti azoici. Il suo derivato, l’acido 4-cloro-3-nitrobenzoico, agisce come intermedio nella produzione di coloranti.
Acido 4-nitrobenzoico o acido p-nitrobenzoico
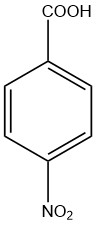
L’acido 4-nitrobenzoico è un acido mononitrobenzoico con i due gruppi in posizione para tra loro. È anche chiamato acido para-nitrobenzoico. È un solido giallo pallido insolubile in acqua e leggermente solubile in metanolo.
Proprietà fisiche dell’acido 4-nitrobenzoico
Le proprietà fisiche dell’acido 4-nitrobenzoico sono le seguenti:
- Massa molare = 167,12 g/mol
- Punto di fusione = 240 °C
- Densità = 1,61
- Solubilità in acqua = 0,02 g/100 ml (a 15 °C)
- Solubilità in metanolo = 9,6 g/100 ml (a 10 °C)
- Solubilità in benzene = 0,017 g/100 ml (a 12,5 °C)
- Costante di dissociazione, Ka (a 25 °C) = 3,93 × 10-4
- Temperatura di decarbossilazione > 240 °C
Reazioni chimiche dell’acido 4-nitrobenzoico
L’acido 4-nitrobenzoico subisce la tipica reazione degli acidi carbossilici aromatici e dei composti nitroaromatici:
L’acido 4-amminobenzoico può essere prodotto dalla riduzione del gruppo nitro in un’ammina.
Il gruppo carbossilico forma esteri con alcoli e cloruro di 4-nitrobenzoile con agenti cloruranti che è un materiale di partenza per il cloridrato di procaina e l’acido folico.
A temperature superiori a 240 °C, l’acido 4-nitrobenzoico forma nitrobenze per decarbossilazione.
L’anello aromatico può subire reazioni di sostituzione, ma è difficile a causa della presenza di gruppi disattivanti.
Produzione di acido 4-nitrobenzoico
L’acido 4-nitrobenzoico è prodotto commercialmente dall’ossidazione del 4-nitrotoluene con ossigeno molecolare. L’ossidazione con acido nitrico al 15% a 175 °C produce l’acido con una resa dell’88,5%.

Monsanto Chemicals Ltd. ha sviluppato un metodo di produzione per l’acido 4-nitrobenzoico mediante ossidazione del 4-nitroacetofenone con acido nitrico acquoso in presenza di metavanadato di ammonio come catalizzatore sotto riflusso.
Sono necessarie otto moli di acido nitrico per convertire una mole di 4-nitroacetofenone a una temperatura di 60 °C alla temperatura di riflusso della miscela.
Raffreddando la miscela di reazione, si formano i cristalli grezzi di acido 4-nitrobenzoico che vengono recuperati da essa mediante filtrazione, quindi purificati mediante ricristallizzazione da solventi quali benzene, etanolo, miscele benzene-etanolo, esano, ecc.

Un metodo interessante prevede la nitrazione e la successiva ossidazione del polistirene. Questo metodo sfrutta l’impedimento sterico della catena polimerica per migliorare il rapporto para/orto del prodotto.
Riferimenti
- Benzoic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a03_555
- Preparation of 2-and 4-nitrobenzoic acid. – https://patents.google.com/patent/US2695311A/en
