Acide thioglycolique : propriétés, réactions, production et utilisations
Qu’est-ce que l’acide thioglycolique ?
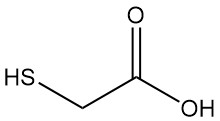
L’acide thioglycolique, également connu sous le nom d’acide mercaptoacétique, est l’acide mercaptocarboxylique le plus simple et le plus important sur le plan industriel, dont la formule est HSCH2COOH. Il s’agit d’un liquide incolore à l’odeur forte et désagréable.
L’acide mercaptoacétique a été synthétisé pour la première fois en 1862 par Carius en faisant réagir l’acide chloroacétique avec du sulfure d’hydrogène de potassium.
Table des matières
1. Propriétés physiques de l’acide thioglycolique
L’acide thioglycolique est un liquide clair et incolore à l’odeur caractéristique. Il est miscible avec l’eau, les mono- et polyalcools, les éthers, les cétones, les esters, les hydrocarbures chlorés et les hydrocarbures aromatiques, mais insoluble dans les hydrocarbures aliphatiques.
Les esters de l’acide thioglycolique sont pour la plupart des liquides incolores aux odeurs caractéristiques. Les esters cétyliques et stéaryliques sont des cires jaune pâle.
Certaines propriétés physiques de l’acide mercaptoacétique sont résumées dans le tableau suivant.
| Propriété | Valeur |
|---|---|
| Numéro CAS | [68-11-1] |
| Formule | HSCH2COOH |
| Masse moléculaire | 92,11 g/mol |
| Point de fusion | -16,5 °C |
| Point d'ébullition à 2,3 kPa | 110–112 °C |
| Point d'ébullition à 0,1 kPa | 79 – 80 °C |
| Indice de réfraction | 1,5027 |
| Densité | 1,325 g/cm3 |
| pKa1 | 3,82 |
| pKa2 | 9,30 |
| Chaleur de combustion | 1450 kJ/mol |
| Pression de vapeur (30 °C) | 0,02 kPa |
| Densité de vapeur | 3,18 |
| Point d'éclair | 126 °C |
2. Réactions de l’acide mercaptoacétique
L’acide mercaptoacétique (acide thioglycolique) possède deux groupes fonctionnels réactifs : un groupe thiol (mercapto) et un groupe acide carboxylique. Cette bifonctionnalité lui permet de participer à diverses réactions, formant divers produits.
L’acide thioglycolique forme facilement des sels avec ses groupes carboxylate et thiol. Il s’agit notamment de sels métalliques, d’esters, d’amides, d’anilides et de thioéthers.
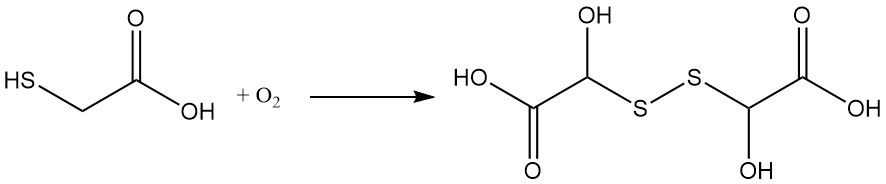
L’acide mercaptoacétique subit une oxydation, même lorsqu’il est exposé à l’air. Cette réaction conduit à la formation d’acide dithiodiglycolique. Des traces de métaux comme le cuivre, le fer et le manganèse peuvent catalyser cette oxydation.
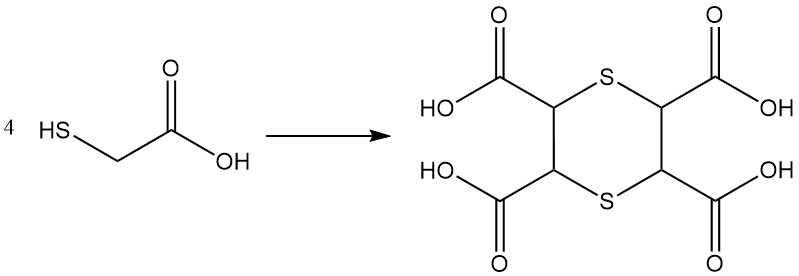
Les solutions concentrées (80 %) d’acide thioglycolique subissent des réactions de condensation pour produire des produits de polycondensation linéaires et cycliques ; les exemples incluent la formation d’un acide tétracarboxylique avec une structure cyclique 1,4-dithiane.
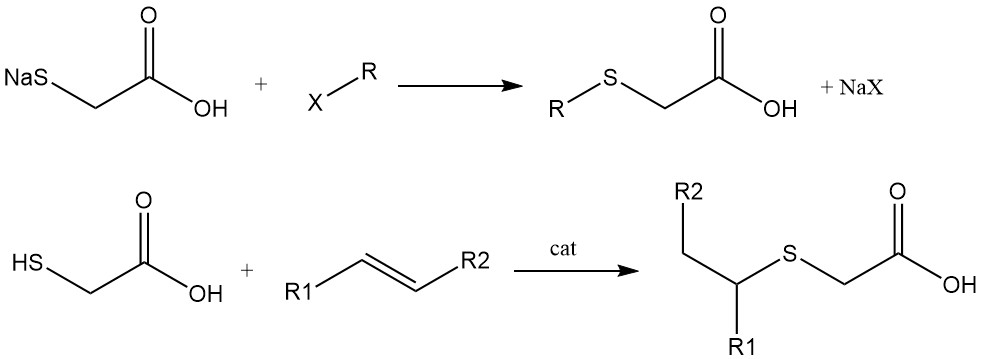
Les thioéthers sont préparés par des réactions entre les sels de sodium ou de potassium du groupe mercapto et des halogénures d’alkyle, ou par l’addition d’acide mercaptoacétique ou de ses dérivés aux doubles ou triples liaisons. La régiosélectivité de ces réactions (Markovnikov vs. anti-Markovnikov) dépend du catalyseur choisi.
L’acide thioglycolique et ses dérivés réagissent avec les aldéhydes et les cétones pour former divers produits, notamment des mercaptals, des mercaptols ou des thioéthers α,β-insaturés. Ces réactions sont catalysées par des acides, tels que les acides minéraux ou les acides toluènesulfoniques.
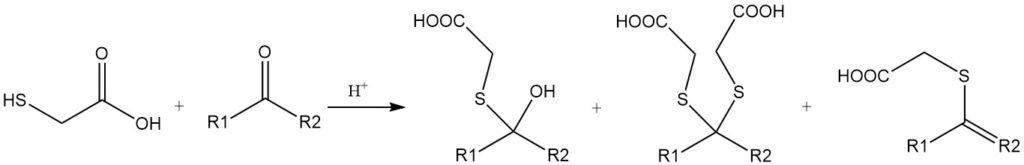
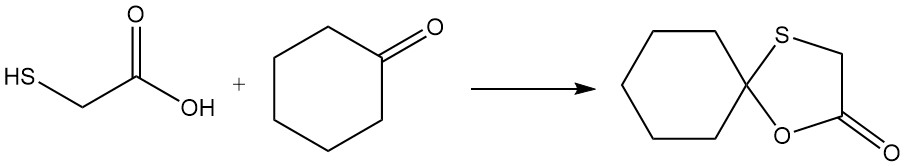
L’acide mercaptoacétique peut participer à une réaction unique dans laquelle les groupes mercapto et carboxyle réagissent simultanément avec un groupe carbonyle. Un exemple est la réaction avec la cyclohexanone, qui donne la 2,2-pentaméthylène-1,3-oxathiolane-5-one.
La forte nature réductrice de l’acide thioglycolique est utilisée pour étudier les systèmes redox biochimiques et l’activité enzymatique. De plus, ses propriétés réductrices sont utilisées dans divers procédés industriels comme les préparations capillaires à froid et la modification de la laine.
L’utilisation de l’acide mercaptoacétique dans l’ondulation permanente des cheveux repose sur sa capacité à réduire et à cliver les ponts disulfures dans la kératine des cheveux.
3. Production d’acide thioglycolique
L’acide thioglycolique (acide mercaptoacétique) est produit commercialement par la réaction de l’acide chloroacétique ou de ses sels avec des sulfures d’hydrogène de métaux alcalins (NaHS ou KHS). Cette réaction produit des sous-produits indésirables tels que l’acide thiodiglycolique, l’acide dithiodiglycolique et l’acide glycolique.
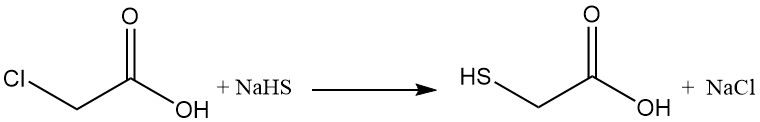
L’isolement du produit souhaité est obtenu par acidification du mélange réactionnel, suivie d’une extraction avec des solvants organiques tels que des éthers, des alcools ou des hydrocarbures chlorés, puis le produit brut est purifié par distillation.
Les méthodes de production utilisent des procédés par lots et en continu, avec certaines variantes utilisant une pression partielle de sulfure d’hydrogène ou de dioxyde de carbone.
Les procédés alternatifs utilisent les flux résiduaires de la réduction des composés nitrés aromatiques comme source de soufre au lieu des sulfures d’hydrogène de métaux alcalins. De plus, un procédé spécifique est basé sur le clivage de l’acide imidazolyl mercaptoacétique avec du sulfure de sodium.
Il existe plusieurs autres voies de synthèse de l’acide mercaptoacétique :
- Clivage du sel de Bunte (NaO3SSCH2COOH) dérivé de l’acide chloroacétique et du thiosulfate de sodium à l’aide d’acide sulfurique dilué.
- Réduction de l’acide dithioglycolique préparé à partir d’acide chloroacétique et de polysulfures de métaux alcalins.
- Décomposition de l’ester xanthate formé à partir de l’acide chloroacétique et de l’éthylxanthate de potassium.
L’acide mercaptoacétique anhydre est produit par distillation du produit de qualité technique avec du toluène. Le contact avec des catalyseurs métalliques pendant la production doit être minimisé pour éviter la dimérisation de l’acide thioglycolique anhydre.
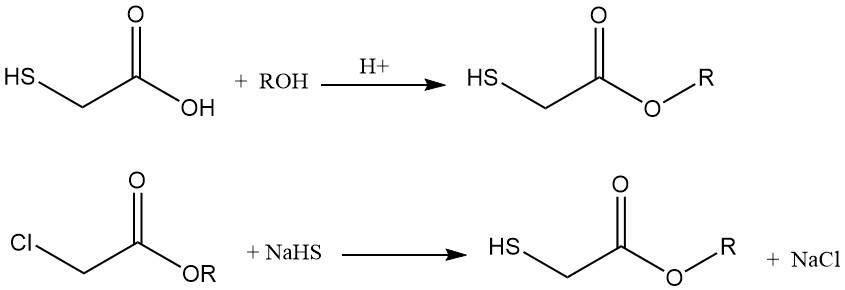
Les esters de l’acide thioglycolique peuvent être synthétisés par deux méthodes principales :
- L’estérification avec des alcools, où l’alcool peut être utilisé comme solvant d’extraction après la synthèse acide.
- La réaction du chloroacétate d’alkyle correspondant avec le thiosulfate de sodium.
4. Utilisations de l’acide thioglycolique
L’acide mercaptoacétique (acide thioglycolique) et ses dérivés ont trouvé diverses applications dans diverses industries depuis 1950 environ.
L’ammonium, les sels d’éthanolammonium et, de plus en plus, le monothioglycolate de glycérol sont utilisés pour formuler des solutions de permanentes pour la coiffure. Le sel de calcium de l’acide thioglycolique est utilisé dans les crèmes dépilatoires pour l’épilation.
Les dérivés de l’acide mercaptoacétique sont utilisés dans les procédés de permanentes de la laine, en particulier dans la fabrication de chapeaux.
Les composés organostanniques dérivés de l’acide thioglycolique, comme le dialkylétain bis (thioglycolate d’isooctyle) et l’alkylétain tris (thioglycolate d’isooctyle), sont des stabilisateurs thermiques très efficaces pour le polychlorure de vinyle (PVC). Leur faible toxicité et leur migration minimale les rendent adaptés aux matériaux d’emballage de qualité alimentaire et aux conduites d’eau potable.
Les esters, en particulier ceux dérivés d’alcools supérieurs comme l’isooctanol et le décanol et les amides de l’acide mercaptoacétique, sont utilisés comme catalyseurs et antioxydants lors de la production de divers plastiques et caoutchoucs.
Le sel de sodium de l’acide thioglycolique est un composant du milieu nutritif de Brewer utilisé pour cultiver des bactéries anaérobies.
L’acide mercaptoacétique est utilisé en chimie analytique pour séparer le fer et l’aluminium et comme réactif pour détecter divers métaux, notamment le fer, le nitrite, l’uranium, le vanadium, le chrome, le cuivre, le molybdène et le palladium.
Il est également utilisé comme composé matriciel dans la spectrométrie de masse à bombardement atomique rapide, une technique d’analyse des biomolécules, et dans le processus d’isolement doux de la lignine en combinaison avec le trifluorure de bore.
Dans l’industrie pharmaceutique, les dérivés de l’acide thioglycolique sont utilisés comme matières premières pour la synthèse du thiophène et du dihydrothiophène. Les acides S-aryl mercaptoacétiques sont des intermédiaires utilisés dans la production de colorants.
La production mondiale d’acide thioglycolique est estimée entre 15 000 et 20 000 tonnes par an.
5. Toxicologie de l’acide thioglycolique
Le contact direct avec l’acide thioglycolique peut irriter la peau et les yeux. L’inhalation de vapeurs d’acide mercaptoacétique peut irriter les muqueuses, provoquant toux et essoufflement, retard de cicatrisation des plaies et cloques.
En raison de ces risques potentiels pour la santé, il est essentiel de porter des gants et des lunettes de protection lors de la manipulation de l’acide thioglycolique.
La valeur limite d’exposition (TLV) établie pour l’acide mercaptoacétique est de 1 ppm (5 mg/m³), ce qui correspond à la concentration maximale dans l’air pour une journée de travail de 8 heures et une semaine de travail de 40 heures à laquelle la plupart des travailleurs peuvent être exposés de manière répétée sans effets néfastes sur la santé.
Des études indiquent que la DL50 orale (dose létale pour 50 % de la population testée) chez le rat pour l’acide thioglycolique est de 261 mg/kg.
En général, les dérivés de l’acide mercaptoacétique et les produits disponibles dans le commerce qui en contiennent sont nettement moins toxiques que l’acide pur. De plus, les réglementations légales imposent souvent des concentrations maximales sûres pour ces produits, minimisant ainsi les risques pour la santé lors de leur utilisation prévue.
Référence
- Mercaptoacetic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_265
