Bencidina: Producción, Reacciones y Usos
La bencidina es una base de difenilo que se utiliza ampliamente como intermediario en la fabricación de colorantes y pigmentos azoicos. También se utiliza como agente reticulante en plásticos de poliuretano y como reactivo analítico y de diagnóstico.
La bencidina puede reaccionar con una variedad de sustancias, incluidos cationes, aniones, compuestos orgánicos y agentes oxidantes. Esta versatilidad los convierte en herramientas valiosas para una amplia gama de aplicaciones.
Tabla de contenido
1. Propiedades físicas de la bencidina
La bencidina, un compuesto diaácido con fórmula química C12H12N2 y masa molar 184,24 g/mol, presenta las siguientes propiedades físicas:
| Propiedad | Valor |
|---|---|
| Apariencia | Polvo blanco |
| Punto de fusión | 128 °C (barras gruesas), 122-125 °C (modificación metaestable) |
| Punto de ebullición | 400-401 °C |
| Densidad | 1,25 g/cm³ |
| Solubilidad en agua | 1 parte en peso en 2447 partes de agua a 12 °C, 106,5 partes de agua a 100 °C |
| Solubilidad en disolventes orgánicos | Escasamente soluble en éter (45 partes) y etanol absoluto (13 partes) a 20 °C |
| Acidez | Diácido (puede donar dos protones en solución) |
| Constantes de disociación (a 30 °C) | K1 = 9,3 x 10⁻¹⁰, K2 = 5,6 x 10⁻¹¹ |
| Calor de neutralización | 106,5 kJ/mol |
| Presión de vapor | < 0,1 mmHg a 25 °C |
| Índice de refracción | 1,652 a 25 °C |
| Punto de inflamación | 205 °C |
| Temperatura de autoignición | 300°C |
2. Reacciones químicas de la bencidina
La bencidina exhibe las siguientes reacciones químicas:
- Exposición al aire: La bencidina se decolora cuando se expone al aire.
- Resistencia al agua: La bencidina es resistente al agua.
- Reacciones de color: La bencidina forma coloraciones azules, verdes o rojas y precipita con agentes oxidantes. Estas reacciones son valiosas para detectar agentes oxidantes.
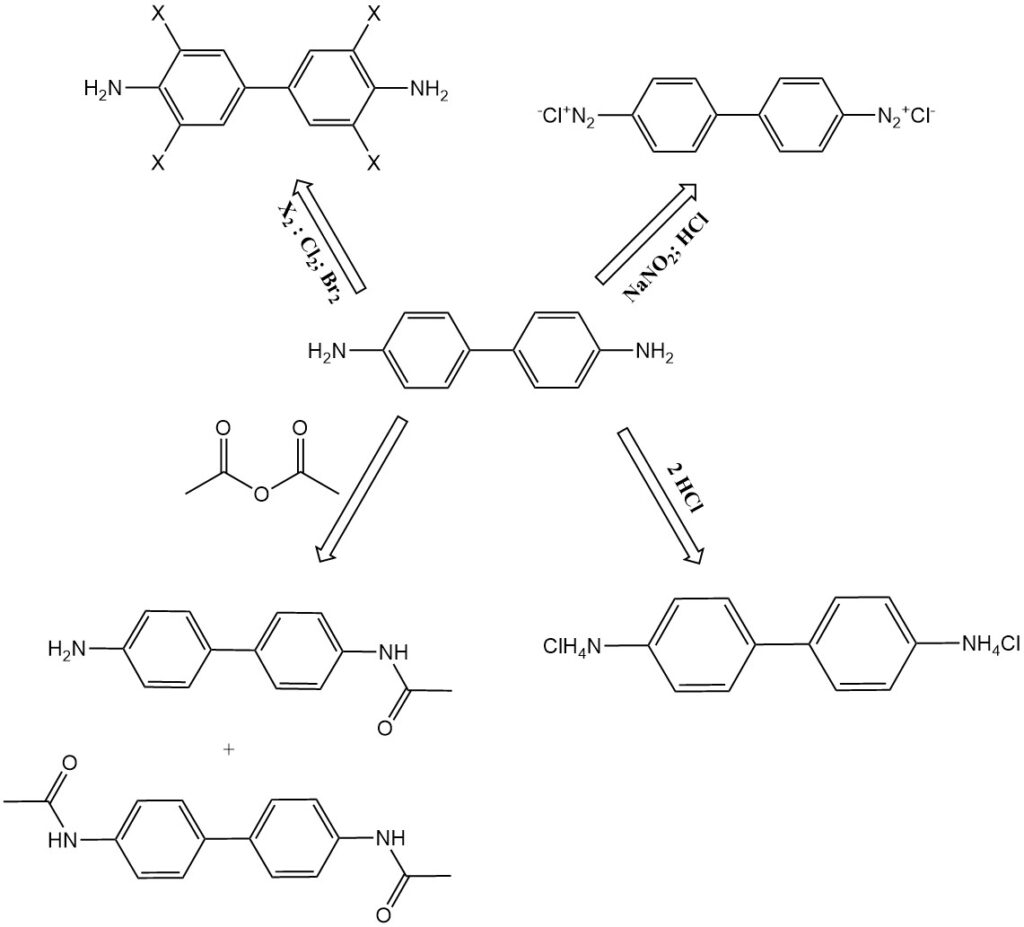
- Cloración y bromación: la bencidina se transforma en 3,3′,5,5′-tetraclorobencidina y tetrabromobencidina, respectivamente.
- Nitración y sulfonación: El sulfato de bencidina produce 2-nitrobencidina, 2,2′-dinitrobenceno y 2,3′-dinitrobenceno mediante reacciones de nitración. En condiciones de sulfonación se pueden formar ácidos sulfónicos y sulfonas de bencidina.
- N-acetilación: la bencidina reacciona con anhídrido acético para formar productos de N-acetilación, como N-acetil-bencidina y N,N’-diacetil-bencidina. Estos compuestos también se encuentran como metabolitos en la digestión animal.
- Diazotización: La bencidina se puede diazotar para formar compuestos de tetrazonio. El primer grupo de diazonio se acopla vigorosamente, mientras que el segundo reacciona más lentamente. Esto permite la producción de colorantes diazo asimétricos.
- Formación de sales: La bencidina forma sales con ácidos, como el monoclorhidrato de bencidina, el diclorhidrato de bencidina y el sulfato de bencidina.
3. Producción de bencidina
La bencidina se produce en tres etapas:
- Reducción del grupo nitro para formar compuestos hidrazo.
- Reordenamiento de bencidina
- Aislamiento básico
La bencidina se fabrica industrialmente a partir de nitrobenceno desde finales del siglo XIX. Los métodos de producción comunes incluyen la reducción de hierro alcalino, la reducción de amalgama y la reducción electroquímica.
El hidrazobenceno resultante se reordena con ácido clorhídrico o ácido sulfúrico durante el enfriamiento y el producto se aísla como clorhidrato de bencidina o sulfato de bencidina. Para minimizar el riesgo de toxicidad crónica, siempre que sea posible se evita la conversión de estas sales a la base libre.
3.1. Reducción de nitrobenceno
La reducción de nitrobenceno a hidrazobenceno se puede representar mediante la siguiente ecuación:
2 C6H5NO2 + 10 H → C6H5NH-NHC6H5 + 4 H2O
Este proceso de reducción se conoce como proceso de Haber y avanza a través de varias etapas, que implican la condensación intermedia de un compuesto nitroso con un compuesto de hidroxilamina para formar el compuesto azoxi.
Este método da como resultado la formación de compuestos hidrazo simétricos. El subproducto primario generado es la amina primaria monocíclica, como la anilina, correspondiente al compuesto nitro original. Este subproducto se forma tanto a partir de la reducción adicional de la fenilhidroxiamina como de la desproporción del compuesto hidrazo inestable.
Se emplean varias técnicas de reducción en aplicaciones industriales, que incluyen:
1. Reducción con polvo de zinc: este método implica la reducción de compuestos nitro aromáticos con polvo de zinc en un ambiente alcalino. La reacción viene dada por:
2 C6H5NO2 + 5 Zn + 10 NaOH → C6H5NH-NHC6H5 + 5 Na2ZnO2 + 4 H2O
Industrialmente, el nitrobenceno se disuelve en un disolvente de alto punto de ebullición y en la solución se suspende polvo de zinc. Se emulsiona una solución de hidróxido de sodio y se produce la reducción. Es necesario un control cuidadoso de la temperatura de la reacción y el proceso se completa cuando el color rojo de la etapa azo desaparece.
2. Reducción con hierro: la reducción con hierro y una solución de hidróxido de sodio es menos común en la química preparativa, pero se ha explorado para la producción comercial. La ecuación de reducción es:
2 C6H5NO2 + 4 Fe + 6 H2O → C6H5NH-NHC6H5 + 2 Fe(OH)2 + 2 Fe(OH)3
En este método se utilizan diversas formas de hierro, como virutas de hierro fundido o polvo de hierro. La reducción se realiza en una relación molar de 1:2:4 para nitrobenceno, hierro e hidróxido de sodio, respectivamente.
3. Reducción con amalgama de sodio: la amalgama de sodio se emplea para la reducción de nitrobenceno a temperaturas elevadas. La reducción se produce en una mezcla emulsionada de nitrobenceno en agua o hidróxido de sodio y se forma el producto azobenceno. Sin embargo, durante este proceso puede producirse cierta reducción excesiva a aminas monocíclicas.
4. Reducción electrolítica: la reducción electroquímica a escala comercial es otro método utilizado para la reducción de compuestos nitro a hidrazo. Implica el uso de celdas electrolíticas con cátodos, diafragmas y ánodos, y la reacción se puede representar como:
2 C6H5NO2 + 10 H+ + 10 e- → C6H5NH-NHC6H5 + 4 H2O
La reducción se lleva a cabo a temperaturas elevadas y densidades de corriente específicas, y el proceso se regula controlando la adición de reactivos.
5. Reducción catalítica: el nitrobenceno se puede reducir a hidrazobenceno mediante hidrogenación catalítica en presencia de un catalizador de paladio-carbono. Este método puede incluir alcohol diluido, una base y condiciones de temperatura y presión elevadas.
Existen otros agentes reductores utilizados en la química preparativa, como diversos metales, amalgamas y agentes reductores orgánicos como metanol, formaldehído y glucosa, que se emplean en función de requisitos de reacción específicos.
3.2. Reordenamiento de bencidina
La transposición de bencidina es un paso clave en la producción de compuestos de diaminodifenilo. Estos compuestos se forman reorganizando compuestos hidrazo aromáticos, que inicialmente se derivan de la reducción de compuestos nitro aromáticos con una solución alcalina.
El proceso de reordenamiento, típicamente catalizado por ácidos minerales, conduce a la formación de compuestos de diaminodifenilo (1), (2) y (3) y compuestos de aminodifenilamina (4) y (5).

- Los reordenamientos orto producen pequeñas cantidades de o-bencidina (2,2′-diaminodifenilo) (2) y difenilina (2,4′-diaminodifenilo) (3).
- Los reordenamientos parciales producen o-semidina (2-aminodifenilamina) (4) y p-semidina (4-aminodifenilamina) (5).

El tipo y la cantidad de productos de reordenamiento están influenciados por la estructura química del material de partida, pero sólo pueden ajustarse mínimamente variando las condiciones de reacción. Algunos subproductos, como la difenilina (3), se producen en cantidades de hasta el 15% pero no tienen valor comercial.
La transposición de bencidina es una verdadera reacción intramolecular, lo que significa que no produce bencidinas mixtas a partir de mezclas de diferentes compuestos hidrazo. En cambio, produce exclusivamente la correspondiente bencidina asimétrica a partir de hidrazobencenos asimétricamente sustituidos.
En el proceso industrial, la transposición de bencidina comienza con la solución caliente obtenida al reducir el nitrobenceno al hidrazobenceno. Si bien no siempre es necesario un aislamiento intermedio del hidrazobenceno, sí es aconsejable en casos específicos, como en las reducciones de amalgama.
Para reducir el contenido azo del hidrazobenceno, se pueden agregar algunos agentes reductores como hidrosulfito de sodio (ditionito de sodio) o polvo de zinc antes de la reordenación.
La reacción ocurre cuando la solución de hidrazobenceno se mezcla con un ácido mineral adecuado, generalmente entre un 10 y un 30 % de ácido clorhídrico, entre un 20 y un 80 % de ácido sulfúrico o una mezcla de ambos.
La temperatura óptima para la transposición es de 100 °C para las bases de difenilo. Es fundamental mantener las temperaturas dentro del rango adecuado, ya que el calor excesivo puede reducir el rendimiento, que normalmente se sitúa entre el 70 y el 95%.
3.3. Aislamiento de producto puro
La etapa más importante de la transposición de bencidina es la formación de la sal de bencidina del ácido clorhídrico o sulfúrico. Esta sal se puede aislar directamente, por ejemplo mediante sal con cloruro de sodio o sulfato de sodio, o convertirse primero en la base libre usando un álcali diluido, como una solución de hidróxido de sodio o una solución de amoníaco.
Los productos secundarios, especialmente la anilina y la difenilina, se pueden separar gracias a su mayor solubilidad. El azobenceno es el único compuesto que queda en el disolvente inerte después de la extracción con ácido y puede devolverse al proceso de reducción.
4. Usos de la bencidina
La bencidina tiene varias aplicaciones, entre ellas:
- Producción de tintes: la bencidina se utiliza para producir tintes azoicos para lana, algodón y cuero. Sin embargo, su uso en esta capacidad ha disminuido debido a su carcinogenicidad.
- Determinación cuantitativa de ácido sulfúrico: la bencidina se puede utilizar para determinar la concentración de ácido sulfúrico.
- Detección y determinación de aniones e iones metálicos: la bencidina se puede utilizar para detectar y cuantificar diversos aniones e iones metálicos.
- Detección de cloro libre o piridina: La bencidina se puede utilizar para detectar trazas de cloro libre o piridina en el agua potable.
- Detección de sangre: la bencidina se puede utilizar para detectar sangre en función de su cambio de color de verde a azul en presencia de peróxido de hidrógeno y peroxidasas.
- Producción de caucho: la bencidina se utiliza como agente reticulante en la producción de productos de caucho, como neumáticos y mangueras.
- Producción de plástico: La bencidina se utiliza como estabilizador en la producción de algunos plásticos.
- Producción farmacéutica: la bencidina se utiliza como intermediario en la producción de algunos productos farmacéuticos, como antihistamínicos y antiespasmódicos.
La bencidina es un compuesto altamente tóxico, pero se sigue utilizando en diversas síntesis y aplicaciones químicas.
5. Toxicología de la bencidina
Toxicidad oral aguda: DL50 en ratas = 1,57 g/kg
Exposición dietética subaguda: los efectos adversos en ratones incluyen hinchazón turbia del hígado, degeneración vacuolar de los túbulos renales, hiperplasia de elementos mieloides en la médula ósea y cambios de células linfoides en el timo y el bazo.
Absorción dérmica y pulmonar: Hay información limitada disponible, pero las manifestaciones sistémicas de toxicidad sugieren que puede ocurrir una absorción significativa.
Inyección intravenosa y metabolismo: la bencidina se convierte en N-acetilbencidina y N,N’-diacetilbencidina, que luego se transforman en N-hidroxi-N,N’-diacetilbencidina y 3-hidroxi-N,N’-diacetilbencidina. Este último compuesto se une a los ácidos nucleicos.
Resultados de la prueba de Ames: la bencidina da positivo en la prueba de Ames y también se ha demostrado que sus metabolitos inducen mutaciones.
Efectos del ADN: la bencidina provoca roturas de cadenas de ADN y transformación celular. Induce la síntesis de ADN no programada en células HeLa y hepatocitos de rata.
Propiedades cancerígenas: se ha demostrado que el clorhidrato de bencidina induce carcinoma hepatocelular en ratones y otros cánceres en ratas, hámsteres y humanos.
La bencidina es un potente carcinógeno en animales y humanos. Está clasificado como Grupo A1 por la comisión MAK y Grupo A1b por la ACGIH.
Referencia
- Benzidine and Benzidine Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a03_539
