Thioglykolsäure: Eigenschaften, Reaktionen, Herstellung und Verwendung
Was ist Thioglykolsäure?
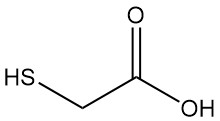
Thioglykolsäure, auch Mercaptoessigsäure genannt, ist die einfachste und industriell bedeutendste Mercaptocarbonsäure mit der Formel HSCH2COOH. Sie ist eine farblose Flüssigkeit mit einem starken, unangenehmen Geruch.
Mercaptoessigsäure wurde erstmals 1862 von Carius synthetisiert, indem er Chloressigsäure mit Kaliumhydrogensulfid reagierte.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Thioglykolsäure
Thioglykolsäure ist eine klare, farblose Flüssigkeit mit einem charakteristischen Geruch. Sie ist mischbar mit Wasser, Mono- und Polyalkoholen, Ethern, Ketonen, Estern, chlorierten Kohlenwasserstoffen und aromatischen Kohlenwasserstoffen, aber unlöslich in aliphatischen Kohlenwasserstoffen.
Die Ester der Thioglykolsäure sind meist farblose Flüssigkeiten mit charakteristischen Gerüchen. Die Cetyl- und Stearylester sind blassgelbe Wachse.
Einige physikalische Eigenschaften der Mercaptoessigsäure sind in der folgenden Tabelle zusammengefasst.
| Eigenschaft | Wert |
|---|---|
| CAS-Nummer | [68-11-1] |
| Formel | HSCH2COOH |
| Molekularmasse | 92,11 g/mol |
| Schmelzpunkt | -16,5 °C |
| Siedepunkt bei 2,3 kPa | 110–112 °C |
| Siedepunkt bei 0,1 kPa | 79 – 80 °C |
| Brechungsindex | 1,5027 |
| Dichte | 1,325 g/cm3 |
| pKa1 | 3,82 |
| pKa2 | 9,30 |
| Verbrennungswärme | 1450 kJ/mol |
| Dampfdruck (30 °C) | 0,02 kPa |
| Dampfdichte | 3,18 |
| Flammpunkt | 126 °C |
2. Reaktionen der Mercaptoessigsäure
Mercaptoessigsäure (Thioglykolsäure) besitzt zwei reaktive funktionelle Gruppen: eine Thiolgruppe (Mercapto) und eine Carbonsäuregruppe. Diese Bifunktionalität ermöglicht es ihr, an verschiedenen Reaktionen teilzunehmen und unterschiedliche Produkte zu bilden.
Thioglykolsäure bildet leicht Salze mit ihren Carboxylat- und Thiolgruppen. Dazu gehören Metallsalze, Ester, Amide, Anilide und Thioether.
Mercaptoessigsäure oxidiert, sogar bei Kontakt mit Luft. Diese Reaktion führt zur Bildung von Dithiodiglykolsäure. Spurenmetalle wie Kupfer, Eisen und Mangan können diese Oxidation katalysieren.
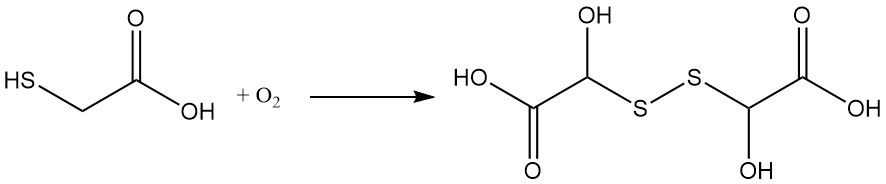
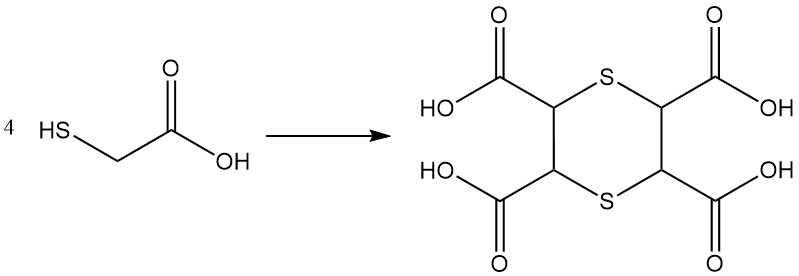
Konzentrierte Lösungen (80 %) von Thioglykolsäure unterliegen Kondensationsreaktionen zu linearen und zyklischen Polykondensationsprodukten; Beispiele hierfür sind die Bildung einer Tetracarbonsäure mit einer 1,4-Dithian-Ringstruktur.
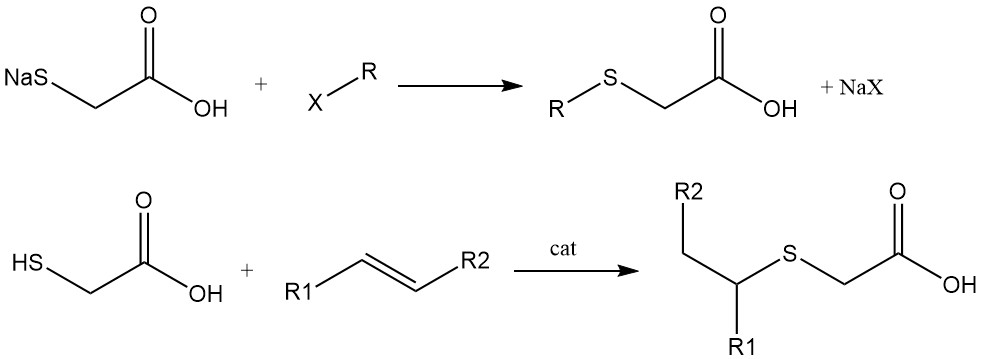
Thioether werden durch Reaktionen zwischen den Natrium- oder Kaliumsalzen der Mercaptogruppe und Alkylhalogeniden oder durch Addition von Mercaptoessigsäure oder ihren Derivaten an Doppel- oder Dreifachbindungen hergestellt. Die Regioselektivität dieser Reaktionen (Markownikow- oder Anti-Markownikow-Reaktion) hängt vom gewählten Katalysator ab.
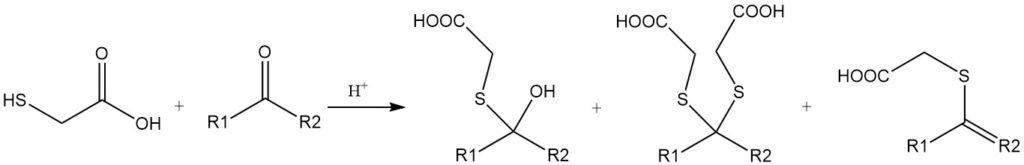
Thioglykolsäure und ihre Derivate reagieren mit Aldehyden und Ketonen zu verschiedenen Produkten, darunter Mercaptale, Mercaptole oder α,β-ungesättigte Thioether. Diese Reaktionen werden durch Säuren wie Mineralsäuren oder Toluolsulfonsäuren katalysiert.
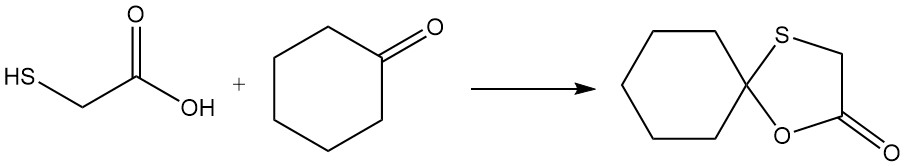
Mercaptoessigsäure kann an einer einzigartigen Reaktion teilnehmen, bei der sowohl die Mercapto- als auch die Carboxylgruppe gleichzeitig mit einer Carbonylgruppe reagieren. Ein Beispiel ist die Reaktion mit Cyclohexanon, die 2,2-Pentamethylen-1,3-oxathiolan-5-on ergibt.
Die stark reduzierende Wirkung der Thioglykolsäure wird zur Untersuchung biochemischer Redoxsysteme und Enzymaktivität genutzt. Darüber hinaus werden ihre reduzierenden Eigenschaften in verschiedenen industriellen Prozessen wie Haarpräparaten zum Kaltwellen und zur Wollmodifizierung eingesetzt.
Die Verwendung von Mercaptoessigsäure bei Dauerwellen basiert auf ihrer Fähigkeit, die Disulfidbrücken im Haarkeratin zu reduzieren und zu spalten.
3. Herstellung von Thioglykolsäure
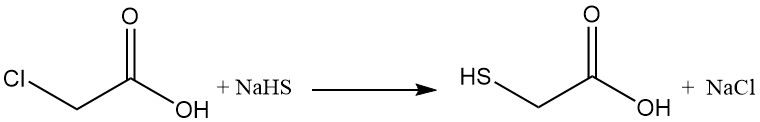
Thioglykolsäure (Mercaptoessigsäure) wird kommerziell durch die Reaktion von Chloressigsäure oder ihren Salzen mit Alkalimetallhydrogensulfiden (NaHS oder KHS) hergestellt. Diese Reaktion erzeugt unerwünschte Nebenprodukte wie Thiodiglykolsäure, Dithiodiglykolsäure und Glykolsäure.
Die Isolierung des gewünschten Produkts erfolgt durch Ansäuern des Reaktionsgemischs, gefolgt von Extraktion mit organischen Lösungsmitteln wie Ethern, Alkoholen oder chlorierten Kohlenwasserstoffen. Anschließend wird das Rohprodukt durch Destillation gereinigt.
Bei den Herstellungsverfahren kommen sowohl Batch- als auch kontinuierliche Prozesse zum Einsatz, wobei bei einigen Varianten ein Partialdruck von Schwefelwasserstoff oder Kohlendioxid verwendet wird.
Bei alternativen Verfahren werden Abfallströme aus der Reduktion aromatischer Nitroverbindungen anstelle von Alkalimetallwasserstoffsulfiden als Schwefelquelle verwendet. Außerdem basiert ein spezielles Verfahren auf der Spaltung von Imidazolylmercaptoessigsäure mit Natriumsulfid.
Es gibt mehrere andere Wege zur Synthese von Mercaptoessigsäure:
- Spaltung des aus Chloressigsäure und Natriumthiosulfat gewonnenen Buntesalzes (NaO3SSCH2COOH) mit verdünnter Schwefelsäure.
- Reduktion von aus Chloressigsäure und Alkalimetallpolysulfiden hergestellter Dithioglykolsäure.
- Zersetzung des aus Chloressigsäure und Kaliumethylxanthat gebildeten Xanthatesters.
Wasserfreie Mercaptoessigsäure wird durch Destillation des technischen Produkts mit Toluol hergestellt. Der Kontakt mit Metallkatalysatoren während der Produktion muss minimiert werden, um eine Dimerisierung der wasserfreien Thioglykolsäure zu verhindern.
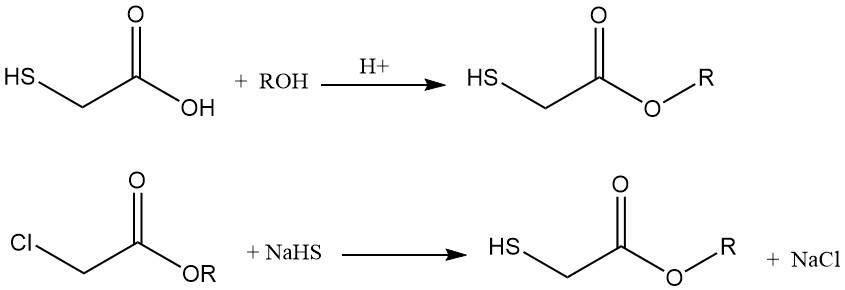
Ester der Thioglykolsäure können auf zwei Arten synthetisiert werden:
- Veresterung mit Alkoholen, wobei der Alkohol nach der Säuresynthese als Extraktionslösungsmittel verwendet werden kann.
- Reaktion des entsprechenden Alkylchloracetats mit Natriumthiosulfat.
4. Verwendung von Thioglykolsäure
Mercaptoessigsäure (Thioglykolsäure) und ihre Derivate finden seit etwa 1950 in verschiedenen Branchen Anwendung.
Ammonium, Ethanolammoniumsalze und zunehmend auch Glycerinmonothioglykolat werden zur Formulierung von Kaltwelllösungen für Haarstyling verwendet. Das Calciumsalz der Thioglykolsäure wird in Enthaarungscremes zur Haarentfernung verwendet.
Derivate der Mercaptoessigsäure werden in Dauerwellverfahren für Wolle eingesetzt, insbesondere bei der Hutherstellung.
Organozinnverbindungen, die von Thioglykolsäure abgeleitet sind, wie Dialkylzinnbis(isooctylthioglykolat) und Alkylzinntris(isooctylthioglykolat), sind hochwirksame Wärmestabilisatoren für Polyvinylchlorid (PVC). Aufgrund ihrer geringen Toxizität und minimalen Migration eignen sie sich für Verpackungsmaterialien in Lebensmittelqualität und Trinkwasserleitungen.
Ester, insbesondere solche aus höheren Alkoholen wie Isooctanol und Decanol sowie Amide der Mercaptoessigsäure, werden als Katalysatoren und Antioxidantien bei der Herstellung verschiedener Kunststoffe und Gummis verwendet.
Das Natriumsalz der Thioglykolsäure ist ein Bestandteil des Nährmediums nach Brewer, das zur Kultivierung anaerober Bakterien verwendet wird.
Mercaptoessigsäure wird in der analytischen Chemie zur Trennung von Eisen und Aluminium und als Reagenz zur Erkennung verschiedener Metalle wie Eisen, Nitrit, Uran, Vanadium, Chrom, Kupfer, Molybdän und Palladium verwendet.
Sie wird auch als Matrixverbindung in der Massenspektrometrie mit schnellem Atombeschuss, einer Technik zur Analyse von Biomolekülen, und im schonenden Isolierungsprozess von Lignin in Kombination mit Bortrifluorid verwendet.
In der pharmazeutischen Industrie werden Thioglykolsäurederivate als Ausgangsstoffe für die Synthese von Thiophen und Dihydrothiophen verwendet. S-Arylmercaptoessigsäuren sind Zwischenprodukte bei der Herstellung von Farbstoffen.
Die weltweite Produktion von Thioglykolsäure wird auf 15.000 bis 20.000 Tonnen pro Jahr geschätzt.
5. Toxikologie von Thioglykolsäure
Direkter Kontakt mit Thioglykolsäure kann Haut und Augen reizen. Das Einatmen von Mercaptoessigsäuredämpfen kann die Schleimhäute reizen, was zu Husten und Kurzatmigkeit, verzögerter Wundheilung und Blasenbildung führen kann.
Aufgrund dieser potenziellen Gesundheitsrisiken ist es wichtig, beim Umgang mit Thioglykolsäure Schutzhandschuhe und eine Schutzbrille zu tragen.
Der für Mercaptoessigsäure festgelegte Grenzwert (TLV) beträgt 1 ppm (5 mg/m³), was die maximale Konzentration in der Luft für einen 8-Stunden-Arbeitstag und eine 40-Stunden-Arbeitswoche darstellt, der die meisten Arbeitnehmer wiederholt ohne gesundheitsschädliche Auswirkungen ausgesetzt werden können.
Studien zeigen, dass die orale LD50 (tödliche Dosis für 50 % der Testpopulation) bei Ratten für Thioglykolsäure 261 mg/kg beträgt.
Im Allgemeinen sind Derivate der Mercaptoessigsäure und handelsübliche Produkte, die diese enthalten, deutlich weniger toxisch als reine Säure. Darüber hinaus schreiben gesetzliche Bestimmungen häufig sichere Höchstkonzentrationen für diese Produkte vor, um die Gesundheitsrisiken bei der bestimmungsgemäßen Verwendung zu minimieren.
Referenz
- Mercaptoacetic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_265
