Herstellung und Verwendung von Natriumglutamat
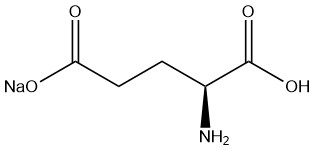
Mononatriumglutamat (MSG) ist ein Natriumsalz der L-Glutaminsäure, das in der Lebensmittelindustrie häufig als Geschmacksverstärker eingesetzt wird. Laut Nikkan Keizai Tsushinsha Co., Ltd. erreichte die MSG-Produktion im März 2013 3 Millionen Tonnen.
L-Glutaminsäure ist eine der am häufigsten vorkommenden Aminosäuren, die natürlicherweise in Proteinen oder als freie Aminosäure in Lösung vorkommen. Es wird häufig in kommerziellen Lebensmitteln wie verpackten und zubereiteten Lebensmitteln, Fertigsuppen und als Tischgewürz verwendet.
1866 isolierte RITTHAUSEN L-Glutaminsäure aus dem sauren Hydrolysat von Weizengluten. Später im Jahr 1890 identifizierte WOLFF die chemische Struktur von L-Glutaminsäure auf synthetischem Wege.
KIKUNAE IKEDA entdeckte 1908 die geschmacksverstärkenden Eigenschaften des Mononatriumsalzes der Glutaminsäure.
Inhaltsverzeichnis
1. Produktion von Natriumglutamat
1.1. Klassische Prozesse
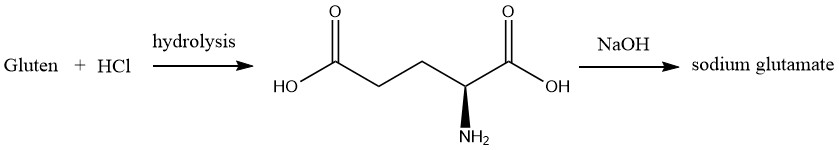
Die industrielle Produktion von Mononatriumglutamat (MSG) begann 1909 und dauerte bis 1965. Während dieser Zeit wurde als Hauptrohstoff Weizengluten verwendet, das aufgrund seines hohen Gehalts an L-Glutaminsäure (ca. 25 Gew.-%) vom Weizenmehl abgetrennt wurde. .
Nach 1934 wurden auch entfettete Sojabohnenflocken als Rohstoff verwendet, da dabei keine Stärke als Nebenprodukt anfiel.
Die Hydrolyse von Rohstoffen erfolgte durch Erhitzen mit Salzsäure. Nach dem Konzentrieren unter vermindertem Druck und der Zugabe von konzentrierter Salzsäure wurden durch Abkühlen des Hydrolysats L-Glutaminsäure-Hydrochlorid-Kristalle gebildet.
Aufgrund seiner geringen Löslichkeit in konzentrierter Salzsäure lässt sich L-Glutaminsäure in Form seines Hydrochlorids leicht von anderen Aminosäuren trennen.
Die L-Glutaminsäure-Hydrochlorid-Kristalle wurden durch Filtration gesammelt, in warmem Wasser gelöst und die Lösung filtriert, um alle unlöslichen Huminstoffe zu entfernen, die durch die Reaktion von Aminosäuren mit Kohlenhydraten entstanden.
Der pH-Wert des Filtrats wurde mit Natriumhydroxid oder Ammoniak auf 3,2, den isoelektrischen Punkt von L-Glutaminsäure, eingestellt, um L-Glutaminsäurekristalle auszufällen.
Die Ausbeute an L-Glutaminsäure war aufgrund ihrer geringen Wasserlöslichkeit hoch (0,864 g pro 100 ml bei 25 °C). Die rohen L-Glutaminsäurekristalle wurden in Wasser suspendiert und mit Natriumhydroxid neutralisiert.
Die Lösung wurde dann mit Aktivkohle entfärbt, was zu einer klaren Lösung führte, die konzentriert wurde, um MSG-Kristalle zu kristallisieren. Die MSG-Kristalle wurden durch Zentrifugieren von der Mutterlauge getrennt und zur Verpackung getrocknet.
1.2.Produktion von Natriumglutamat durch Fermentation

In den frühen 1950er Jahren berichteten DAGLEY und Kollegen über das Vorhandensein geringer Mengen an Aminosäuren im Kulturmedium von Escherichia coli. Sie beobachteten, dass die Zugabe von überschüssigen Ammoniumsalzen zu einer Steigerung der Aminosäureproduktion führte.
Im Jahr 1957 stellten KINOSHITA et al. entdeckte Bakterien, die erhebliche Mengen an L-Glutaminsäure ansammeln. Die KINOSHITA et al. Die Methode mit Micrococcus glutamicus (später umbenannt in Corynebacterium glutamicum) ergab Ausbeuten an L-Glutaminsäure von etwa 30 %, die sofort in der industriellen Produktion eingesetzt wurden.
Bakterien, die L-Glutaminsäure produzieren, sind in der Natur weit verbreitet, und die meisten dieser Bakterien sind grampositiv, nicht sporenbildend, nicht beweglich und benötigen Biotin für ihr Wachstum. Für die industrielle Produktion von Mononatriumglutamat (MSG) werden üblicherweise Melasse und Stärkehydrolysat als Rohstoffe verwendet. Die Anreicherung von L-Glutaminsäure wird nicht durch ihre Biosynthese in den Bakterienzellen, sondern durch ihre Sekretion gesteuert.
Biotin ist eines der essentiellen Vitamine für das Zellwachstum, doch eine für das Zellwachstum ausreichende Biotinkonzentration im Kulturmedium macht die Zellmembranen für L-Glutamat undurchlässig, was zu einer schlechten Anreicherung führt.
Der kritische Biotingehalt der Zellen für die L-Glutaminsäureproduktion liegt bei 0,5 mg/g Trockenzellen. Somit ist die Anreicherung von L-Glutaminsäure dann am höchsten, wenn die Biotinkonzentration für ein maximales Wachstum nicht optimal ist.
Daher konnten biotinreiche Rohstoffe wie Rübenmelasse und Zuckerrohrmelasse erst verwendet werden, als die biotinhemmenden Wirkungen von C16–C18-gesättigten Polyoxyethylenfettsäureestern entdeckt wurden.
Es wird angenommen, dass die Begrenzung der Biotinmenge zu einer unvollständigen Biosynthese von Ölsäure führt, was zu einer Verringerung der Phospholipide in der Zellmembran führt und die Membran durchlässig macht.
Ammoniumsalze und Harnstoff werden als Stickstoffquellen sowohl für das mikrobielle Wachstum als auch für die Produktbildung verwendet. Durch die Aufnahme von Ammoniumionen und die Bildung von L-Glutaminsäure wird das Kulturmedium sauer.
Gasförmiges Ammoniak wird vorteilhafterweise verwendet, um einen neutralen pH-Wert aufrechtzuerhalten und eine Verdünnung der Brühe zu vermeiden, da es weder Hydroxylionen noch Wasser enthält.
Da es sich bei der Biosynthese von L-Glutaminsäure um einen aeroben Prozess handelt, muss der Druck des gelösten Sauerstoffs durch Belüftung und Rühren im Fermenter unbedingt über 1 kPa gehalten werden.
Fortschritte in der Fermentationstechnologie haben es ermöglicht, die Anreicherung und Ausbeute an L-Glutaminsäure auf über 120 g/L bzw. 63 % zu steigern.
Der pH-Wert der Fermentationsbrühe wird auf 3,2 eingestellt, um L-Glutaminsäurekristalle zu gewinnen, die dann mit der gleichen Methode wie im Extraktionsprozess in MSG umgewandelt werden.
2. Eigenschaften von Natriumglutamat
L-Glutaminsäure bildet bei der Dehydratisierung eine intramolekulare Peptidbindung zwischen ihren α-Amino- und γ-Carboxylgruppen. Diese Reaktion bevorzugt die Bildung von 2-Pyrrolidon-5-carbonsäure (PCA) bei schwach sauren oder schwach basischen pH-Bedingungen.
Bei neutralem pH-Wert erfolgt die Dehydrierung langsamer. Umgekehrt fördern stark saure oder alkalische Bedingungen die Hydratation von PCA.
Die üblichen Kochbedingungen führen nicht zu Racemisierung oder Dehydratisierung.
Die minimal wahrnehmbare Konzentration von MSG beträgt 0,03 % und liegt damit unter den Grenzwerten von Natriumchlorid (0,2 %) oder Saccharose (0,5 %). Die geschmacksverstärkende Aktivität von MSG wird in Gegenwart von 5′-Inosinat und 5′-Guanylat synergistisch erhöht.
L-Glutaminsäure wird als nicht-essentielle Aminosäure eingestuft und spielt eine entscheidende Rolle im Stickstoffstoffwechsel von Aminosäuren. Glutamatdehydrogenase katalysiert die reduktive Aminierung von 2-Oxoglutarat zu L-Glutamat für den Einbau von anorganischem Stickstoff.
Viele Organismen verfügen über eine Vielzahl von Aminotransferasen, die Aminogruppen von Aminosäuren auf 2-Oxosäuren übertragen, und viele dieser Enzyme verwenden das Glutamat/2-Oxoglutarat-Paar als Aminodonor/-akzeptor.
L-Glutamat dient als direkte Vorstufe für verschiedene essentielle Substanzen, darunter L-Glutamin, den Neurotransmitter γ-Aminobuttersäure (GABA), γ-Carboxyglutamat in kalziumbindenden Proteinen und das Tripeptid Glutathion.
3. Verwendung von Mononatriumglutamat
Würze
Als bewährtes Würzmittel oder Geschmacksverstärker wird MSG häufig zur Verbesserung der Schmackhaftigkeit von Lebensmitteln eingesetzt. Der charakteristische Geschmack von MSG, Umami, unterscheidet es von den anderen vier Grundgeschmacksrichtungen: süß, salzig, sauer und bitter.
Jüngste Fortschritte in der Molekularbiologie haben die Proteine identifiziert, die als Umami-Geschmacksrezeptoren fungieren und in speziellen Zellen der Geschmacksknospen auf der Zunge und in der Mundhöhle exprimiert werden.
Glutamate sind in verschiedenen Lebensmitteln wie Muttermilch, Tomaten, Käse, Algen, Fisch, Fleisch und Gemüse enthalten. Andere Umami-Substanzen wie 5′-Ribonukleotide wie Inosinat und Guanylat kommen auch in Fleisch, Fisch und getrockneten Pilzen vor.
Mononatriumglutamat verbessert wirksam den Geschmack einer Vielzahl von Lebensmitteln, insbesondere von Fleisch, Meeresfrüchten, Gemüse, Suppen, Eintöpfen und Suppen.
Allerdings werden alkoholische Getränke, Früchte und Süßwaren durch die Zugabe von MSG nicht verbessert und die Auswirkung auf Geruch oder Aroma ist vernachlässigbar.
Industrielle Anwendungen
Abhängig vom pH-Wert wird Glutaminsäure für industrielle Anwendungen eingesetzt. Argininglutamat wird beispielsweise als Rohstoff für Arzneimittel und Kosmetika verwendet.
Als Magensäuremittel wird Glutaminsäurehydrochlorid verwendet, das durch Reaktion von Glutaminsäure mit Salzsäure entsteht.
Die amphoteren Elektrolyteigenschaften von Glutaminsäure werden in Chelatbildnern, Puffern und Buildern für Waschmittel genutzt.
Das durch Neutralisation der dehydrierten Glutaminsäure mit Natriumhydroxid gewonnene Natriumsalz der Pyroglutaminsäure ist sehr hygroskopisch und wird als Bestandteil natürlicher Feuchthaltefaktoren für die menschliche Haut sowie als Feuchthaltemittel in Kosmetika verwendet.
Ein Polymer aus Methylglutamat dient als Beschichtungsmittel für Kunstleder.
Ein Kondensat mit Formaldehyd wirkt als Verzögerer für Putz.
Die N-acylierte Verbindung, die durch die Reaktion mit einer langkettigen Fettsäure entsteht, ist ein anionisches Tensid, das aufgrund seiner Milde und hohen Sicherheit häufig in Haut- und Haarreinigungsmitteln verwendet wird.
Das Dibutylamid dieser N-Acylglutaminsäure gelatiniert unpolare Öle und kann als Rückgewinnungsmittel für ausgelaufenes Meeresöl verwendet werden.
Referenz
Monosodium Glutamate; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_711.pub2
