Maleïnezuuranhydride: eigenschappen, reacties, productie en toepassingen
Wat is Maleïnezuuranhydride?
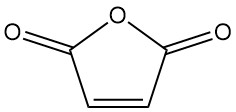
Maleïnezuuranhydride, ook bekend als 2,5-furandion, is een organische verbinding met de formule C4H2O3. Het is een kleurloze of witte vaste stof met een sterke, irriterende geur die industrieel belangrijker is in vergelijking met maleïnezuur.
Inhoudsopgave
1. Fysische eigenschappen van maleïnezuuranhydride
Maleïnezuuranhydride vormt orthorombische naaldkristallen. Het is oplosbaar in water, aceton, ethanol, xyleen, ethylacetaat, chloroform, benzeen, tolueen, tetrachloormethaan en vele andere organische oplosmiddelen.
Maleïnezuuranhydride is hygroscopisch en ontvlambaar en kan explosieve mengsels vormen met lucht. Het kan sublimeren. De pH van maleïnezuuranhydride-wateroplossingen is 2,42 bij 1×10-2 M, 2,62 bij 5×10-3 M en 3,10 bij 1×10-4 M.
De belangrijkste fysische eigenschappen van maleïnezuuranhydride worden samengevat in de volgende tabel.
| Eigenschap | Waarde |
|---|---|
| CAS-nummer | 108-31-6 |
| Chemische formule | C4H2O3 |
| Moleculaire massa | 98,06 g/mol |
| Smeltpunt | 52,85 °C |
| Kookpunt (101,3 kPa) | 202,0 °C |
| Dichtheid | 1,48 g/cm3 |
| Dampdichtheid | 3,40 |
| Verbrandingswarmte | -1391,2 kJ/mol |
| Soortelijke warmte (vloeistof) | -1,67 kJ mol-1 K-1 |
| Verdampingswarmte | 54,8 kJ/mol |
| Smeltwarmte | 13,66 kJ/mol |
| Vlampunt | 102 °C (gesloten beker) 110 °C (open beker) |
| Zelfontbrandingstemperatuur | 477 °C |
2. Reacties van Maleïnezuuranhydride
Maleïnezuuranhydride vertoont een hoge reactiviteit vanwege de aanwezigheid van een dubbele binding en zijn anhydridegroep.
Maleïnezuuranhydride ondergaat gemakkelijk hydrolyse met water om maleïnezuur te vormen. Deze reactie is exotherm.
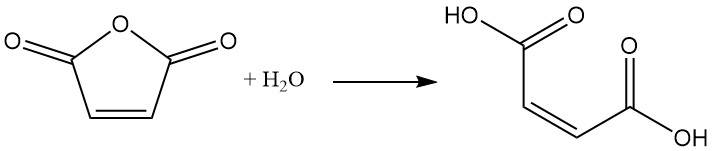
Reactie met alcoholen in aanwezigheid van een katalysator leidt tot de vorming van maleïnezuuresters. De keuze van de katalysator en de reactietemperatuur bepalen het product. Bij lagere temperaturen worden semi-esters gevormd, terwijl hogere temperaturen de vorming van diesters met watereliminatie bevorderen.
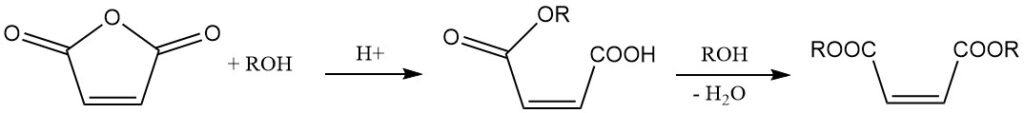
Maleïnezuuranhydride reageert met ammoniak of aminen om de overeenkomstige semiamiden te produceren. Verdere dehydratie leidt tot de vorming van cyclische imiden.
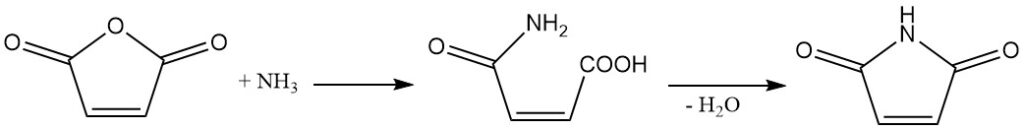
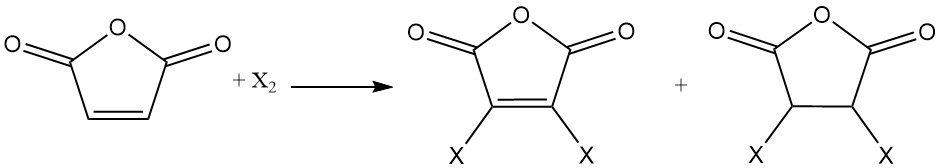
De dubbele binding van maleïnezuuranhydride ondergaat additiereacties met halogenen. Afhankelijk van de reactieomstandigheden kunnen mono- of dihalogeneerde maleïnezuuranhydriden of dihalogeneerde barnsteenzuuranhydriden worden gevormd.
De hydrogenering van maleïnezuuranhydride levert verschillende producten op, afhankelijk van de reactieomstandigheden. Deze producten omvatten barnsteenzuuranhydride, 1,4-butaandiol, tetrahydrofuraan of butyrolacton.

De toevoeging van olefinen leidt tot de vorming van alkenylbarnsteenzuuranhydriden.
Maleïnezuuranhydride neemt deel aan Diels-Alder-reacties met geconjugeerde diënen.
Maleïnezuuranhydride kan homopolymerisatie- en copolymerisatiereacties ondergaan.
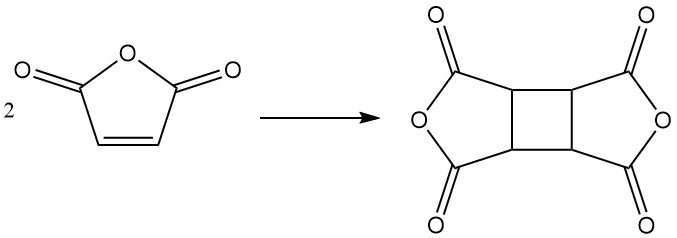
Onder specifieke omstandigheden kan maleïnezuuranhydride dimeriseren om cyclobutaantetracarbonzuurdianhydride te vormen, dat wordt gebruikt bij de productie van polyimiden.
3. Productie van maleïnezuuranhydride
Maleïnezuuranhydride wordt geproduceerd door de katalytische oxidatie van geschikte koolwaterstoffen in de gasfase. Traditioneel was benzeen de primaire grondstof. C4-koolwaterstoffen (zoals butaan) zijn echter de laatste jaren steeds belangrijker geworden.
3.1. Productie van maleïnezuuranhydride door oxidatie van benzeen
Om maleïnezuuranhydride te produceren (Figuur 1), wordt benzoë voorverwarmd en gemengd met een luchtstroom om een homogeen mengsel te vormen. Er worden buisvormige reactoren met verticale buizen gevuld met een katalysator zoals vanadium- en molybdeenoxiden op een inerte drager gebruikt.
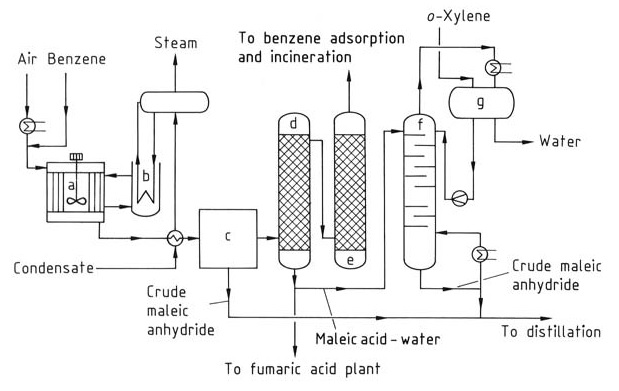
a) Reactor; b) Zoutbadkoeler; c) Gedeeltelijke condensor; d) Zuurwasser; e) Alkaliwasser; f) Dehydratatiekolom; g) Fasescheider
De reactie is exotherm en vereist controle over de bedrijfstemperatuur en een druk tussen 0,15-0,25 MPa om de opbrengst van maleïnezuuranhydride te optimaliseren en de verbranding tot CO2 en CO te minimaliseren. De warmte die tijdens de reactie wordt gegenereerd (ongeveer 27 MJ per ton benzeen) wordt verwijderd met behulp van circulerende gesmolten zouten, die vervolgens worden gekoeld met water.
De volgende reactie vertegenwoordigt de productie van maleïnezuuranhydride:
C6H6 + 4,5 O2 → C4H2O3 + 2 CO2 + 2 H2O (ΔH = -1875 kJ/mol)
Er vindt echter ook ongewenste verbranding plaats. Niet-gereageerde benzeen kan worden teruggewonnen met behulp van technieken zoals adsorptie en hergebruikt in het proces. Hoewel er patenten bestaan voor processen die een groter deel van het reactiegas recyclen na scheiding van maleïnezuuranhydride, zijn deze nog niet op grote schaal commercieel toegepast.
Scheiding van ruw maleïnezuuranhydride
Het reactoreffluent wordt eerst gekoeld om condensatie van maleïnezuuranhydride en water te voorkomen. Vervolgens kunnen twee methoden worden gebruikt voor verdere verwerking:
- Gedeeltelijke condensatie: Het gasmengsel wordt gekoeld tot ongeveer 55 °C, waardoor maleïnezuuranhydride kan condenseren en als vloeistof kan worden gescheiden. Langdurig contact met het waterhoudende gas kan echter leiden tot de vorming van maleïnezuur. Deze aanpak wint doorgaans 40-60% van het maleïnezuuranhydride terug.
- Waterreiniging: Deze methode vangt alle maleïnezuuranhydride in het reactiegas op als een maleïnezuuroplossing. De daaropvolgende dehydratatiestap om maleïnezuuranhydride terug te winnen is echter energie-intensief en heeft alleen de voorkeur voor reactiegassen met een hoog watergehalte (zoals die van C4-oxidatie).
3.2. Productie van maleïnezuuranhydride door dehydratatie van waterige maleïnezuuroplossingen
Maleïnezuuranhydride kan worden afgeleid uit de maleïnezuuroplossingen die worden verkregen door het reactiegas met water te wassen.
Bij temperaturen boven de 150 °C kunnen zelfs sporen van alkali in de wasoplossing de decarboxylatie van maleïnezuuranhydride veroorzaken. Daarom is alkalivrij waswater noodzakelijk.
Dehydratatie van maleïnezuur vereist temperaturen boven de 100 °C (ΔH = +34,88 kJ/mol). Het bereiken van een industrieel relevante reactiesnelheid vereist echter temperaturen boven de 130 °C. Dit systeem met hogere temperaturen bevordert ook de ongewenste isomerisatie van maleïnezuur tot fumaarzuur.
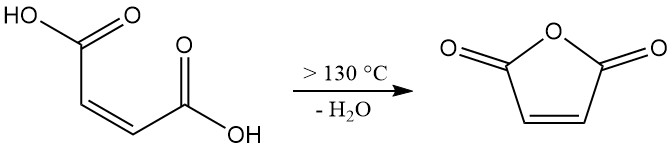
Hoewel fumaarzuur zelf niet significant afbreekt tot maleïnezuuranhydride onder 230 °C, vermindert de aanwezigheid ervan de totale opbrengst van het gewenste product. Om isomerisatie te minimaliseren, is een korte verblijftijd bij verhoogde temperaturen cruciaal tijdens het dehydratatieproces.
Er worden twee hoofdprocessen gebruikt voor het dehydrateren van waterige maleïnezuuroplossingen: de entrainagensmethode en het thermische proces zonder entrainagens.
3.2.1. Entrainagensmethode
In dit proces wordt de waterige maleïnezuuroplossing in het bovenste gedeelte van een destillatiekolom gevoerd, waar het zich mengt met een kokend mengsel van maleïnezuuranhydride en een entrainagens zoals xyleen.
De entrainagens (xyleen) vormen een azeotropisch mengsel met water, waardoor beide als een dampstroom uit de kolom kunnen worden verwijderd. Deze dampstroom wordt vervolgens in een decanter gescheiden in organische en waterige fasen.
De organische fase die xyleen bevat, wordt teruggevoerd naar het bovenste gedeelte van de destillatiekolom, terwijl de waterige fase wordt teruggevoerd naar de reactiegaswasser van de oxidatiefabriek.
De onderste productstroom van de destillatiekolom, die maleïnezuuranhydride (10-40%), xyleen (1-5%), maleïnezuur (1-3%) en fumaarzuur (1-3%) bevat, ondergaat verdere destillatie om zuiver maleïnezuuranhydride te isoleren. Dit proces kan continu of in batches worden uitgevoerd.
3.2.2. Thermisch proces zonder meeslepend middel
Deze methode maakt gebruik van dunnelaagverdampingstechnologie om thermische dehydratie van de waterige maleïnezuuroplossing te bereiken. De techniek zorgt voor efficiënte verwijdering van water als stoom, terwijl de verblijftijd van maleïnezuur bij hoge temperaturen (150-200 °C) wordt geminimaliseerd. Deze korte blootstellingstijd helpt isomerisatie tot fumaarzuur (slechts 1-3%) te onderdrukken.
Meerdere dunnelaagverdampereenheden worden vaak in serie geplaatst. Het vloeibare maleïnezuuranhydride dat uit de gedeeltelijke condensor wordt verkregen, kan ook naar de tweede fase van dit systeem worden gevoerd om eventueel overgebleven maleïnezuur (1–5%) te dehydrateren.
Dit continue proces produceert maleïnezuuranhydride met een hoge zuiverheid (99%) na een laatste destillatiestap. Het bodemproduct van de laatste verdamper bevat fumaarzuur en hoogkokende residuen, die worden weggegooid.
Deze continu werkende installaties vereisen periodieke stilstanden voor reiniging.
3.3. Productie van maleïnezuuranhydride door oxidatie van C4-koolwaterstoffen
De laatste jaren is oxidatie van C4-koolwaterstoffen, voornamelijk met behulp van n-butaan of n-butaan-n-buteenmengsels die rijk zijn aan paraffines, naar voren gekomen als een belangrijk alternatief voor traditionele benzeenoxidatie voor de productie van maleïnezuuranhydride.
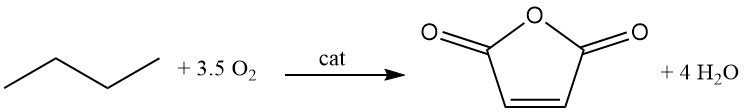
Er zijn verschillende soorten processen ontwikkeld, zoals fixed-bed-, fluidized-bed- en transport-bed-processen.
3.3.1. Fixed-bed-proces
Het fixed-bed-proces is een commercieel gevestigde methode die gebruikmaakt van vanadium-fosforoxide (V-P-O)-katalysatoren verpakt in buisvormige reactoren, vergelijkbaar met benzeenoxidatie. De reactie is zeer exotherm.
C4H10 + 3,5 O2 → C4H2O3 + 4 H2O (ΔH = -1260 kJ/mol)
Vergeleken met benzeenoxidatie worden echter lagere conversiepercentages van 80% en selectiviteiten (70%) waargenomen. Het terugwinnen van niet-gereageerde C4-koolwaterstoffen is een grotere uitdaging dan bij benzeen.
3.3.2. Fluidized-bedproces
Het fluidized-bedproces biedt een gelijkmatigere temperatuurregeling in de reactor, waardoor “hot spots” worden geminimaliseerd en de reactieselectiviteit mogelijk wordt verbeterd. Het fluidisatieproces omvat echter ook intensieve productremixing, wat het voordeel teniet kan doen.
Een andere uitdaging is mechanische spanning op de V-P-O-katalysator door slijtage en erosie. Ondanks deze nadelen kunnen fluidized beds werken bij hogere C4-concentraties (binnen het explosiebereik) vanwege hun effectiviteit als vlambarrières.
Het ALMA-proces (Alusuisse, Lummus) is een voorbeeld van een fluidized-bedreactor gekoppeld aan een niet-waterige verwerkingseenheid.
3.3.3. Transport-bedproces
Dit proces is ontwikkeld door Monsanto en DuPont en maakt gebruik van twee reactoren. De V-P-O-katalysator die wordt verbruikt bij de C4-oxidatie wordt geregenereerd met zuurstof in de eerste reactor. De geregenereerde katalysator reageert vervolgens met n-butaan in de tweede reactor onder bijna-stoichiometrische omstandigheden met minimale atmosferische zuurstof.
Dit proces bereikt een hoge selectiviteit voor de vorming van maleïnezuuranhydride (75 mol%) terwijl de remixing van het productgas wordt geminimaliseerd. Het is echter nog in ontwikkeling.
Vanwege de toegenomen watervorming in vergelijking met benzeenoxidatie is directe liquefactie van maleïnezuuranhydride uit C4-reactiegas via gedeeltelijke condensatie beperkt. Een groter deel (65-70%) moet worden teruggewonnen als maleïnezuur door waterwassen, gevolgd door dehydratie.
Een alternatieve zuiveringsmethode maakt gebruik van organische oplosmiddelabsorptie van maleïnezuuranhydride uit het reactiegas, wat scheiding mogelijk maakt zonder significante maleïnezuurvorming. Het oplosmiddel-maleïnezuuranhydridemengsel ondergaat vervolgens fractionele destillatie om zuiver maleïnezuuranhydride te isoleren.
3.4. Zuivering van ruw maleïnezuuranhydride
Er zijn twee hoofdmethoden voor het zuiveren van ruw maleïnezuuranhydride: batchgewijze destillatie en continue destillatie.
3.4.1. Batchgewijze distillatie
Batchgewijze distillatie wordt gebruikt voor het verwerken van direct gescheiden maleïnezuuranhydride of mengsels verkregen door dehydratie van entrainagens. Het ruwe maleïnezuuranhydride wordt in een batchdestillatiekolom geladen en aanvankelijk verhit onder volledige refluxomstandigheden. Dit bereikt een volledige dehydratie van alle resterende maleïnezuur.
De kleine hoeveelheid water die tijdens de dehydratie wordt geëlimineerd, condenseert en wordt gescheiden van het recirculerende entrainagens (meestal xyleen). Het xyleen wordt vervolgens verwijderd door distillatie. Ten slotte wordt het gezuiverde maleïnezuuranhydride gewonnen door distillatie onder vacuüm.
Batchstills met een capaciteit van 50 tot 150 kubieke meter en distillatiekolommen met 10–20 trays worden vaak gebruikt voor dit proces.
3.4.2. Continue distillatie
Continue distillatie is zuiniger voor grootschalige maleïnezuuranhydrideproductiefaciliteiten.
In dit proces (Figuur 2) wordt een continue stroom van het ruwe maleïnezuuranhydridemengsel naar het destillatiesysteem gevoerd. Residu-xyleen wordt eerst verwijderd in een speciale kolom (f). Tot slot wordt zuiver maleïnezuuranhydride geïsoleerd uit de bovenkant van een tweede kolom (g) via destillatie.
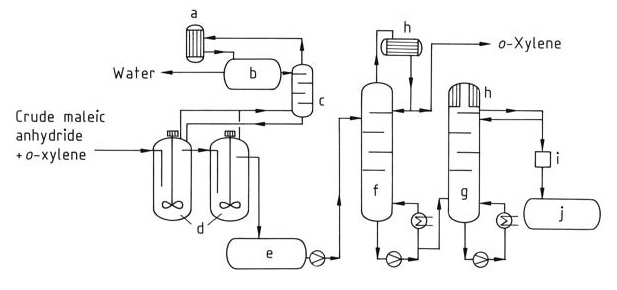
a) Condensor; b) Scheidingsvat; c) Kolom; d) Na-dehydratie; e) Tussentank; f) o-Xyleenkolom; g) Zuivere maleïnezuuranhydridekolom; h) Koeler; i) Colorimeter; j) Zuiver maleïnezuuranhydridevat
4. Toepassingen van maleïnezuuranhydride
De unieke eigenschappen van maleïnezuuranhydride als dicarbonzuuranhydride met een dubbele binding maken het een veelzijdige bouwsteen voor verschillende industriële toepassingen.
Maleïnezuuranhydride wordt voornamelijk gebruikt voor de productie van polyesters en alkydharsen, die worden gebruikt bij de productie van glasvezelversterkte kunststoffen voor de bouw, elektrische toepassingen, pijpleidingen en maritieme constructie. Het wordt ook gebruikt bij de formulering van smeermiddelen en weekmakers.
Maleïnezuuranhydride neemt gemakkelijk deel aan copolymerisatiereacties. Enkele industrieel belangrijke voorbeelden zijn maleïnezuuranhydride-styreencopolymeren die worden gebruikt voor technische kunststoffen en maleïnezuuranhydride-acrylzuurcopolymeren die worden gebruikt in de detergentenindustrie.
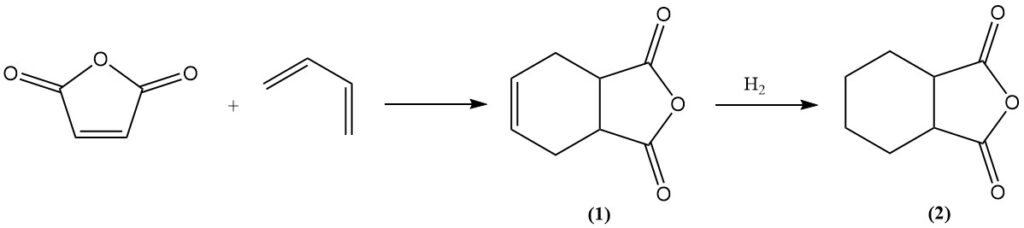
Maleïnezuuranhydride ondergaat Diels-Alder-reacties met diënen zoals butadieen om tetrahydroftaalzuuranhydride (1) te vormen. Verdere hydrogenering levert hexahydroftaalzuuranhydride (2) op, wat een waardevol uithardingsmiddel is voor epoxyharsen. Een soortgelijk proces met isopreen levert methylhexahydroftaalzuuranhydride op voor dezelfde toepassing.
Kleinere hoeveelheden maleïnezuuranhydride worden gebruikt bij de productie van pesticiden zoals captan en malathion, evenals groeiremmers zoals maleïnezuurhydrazide.
Maleïnezuuresters kunnen worden omgezet in oppervlakteactieve stoffen door reacties met natriumwaterstofsulfiet.
Maleïnezuuranhydride kan worden gebruikt als een droogversneller wanneer het wordt toegevoegd aan drogende oliën, waardoor de kwaliteit van lakken wordt verbeterd.
5. Toxicologie van maleïnezuuranhydride
Maleïnezuuranhydride kan hydrolyseren tot maleïnezuur in water, dus de toxicologische eigenschappen worden beïnvloed door de aanwezigheid van maleïnezuur.
Maleïnezuuranhydride vertoont matige acute toxiciteit op basis van LD50-waarden (481 mg (rat, oraal), 465 mg (muizen, oraal), 2620 mg (konijn, percutaan) en 390 mg (cavia, oraal) per kilogram lichaamsgewicht).
Het primaire acute toxische effect is de lokale irriterende en corrosieve werking op de huid, slijmvliezen en ogen. Blootstelling kan irritatie veroorzaken bij concentraties zo laag als 1,5–2 ppm, met ernstige irritatie boven 2,5 ppm.
Het inademen van maleïnezuuranhydride in concentraties hoger dan 1,2 ppm gedurende langere perioden kan astmatische symptomen veroorzaken.
Maleïnezuuranhydride is een sterke sensibilisator, wat betekent dat herhaalde blootstelling kan leiden tot allergische reacties bij zowel mensen als dieren.
Dierstudies hebben geen bewijs geleverd van carcinogene, teratogene (geboorteafwijkingen) of reproductieve toxiciteit door blootstelling aan maleïnezuuranhydride. Er werden echter geen systemische effecten waargenomen tot een blootstellingsniveau van 2,4 ppm, dus effecten bij hogere concentraties zijn niet volledig uitgesloten.
Beroepsmatige blootstellingslimieten zijn vastgesteld op basis van de irriterende en sensibiliserende eigenschappen:
- MAK (Duitse commissie voor onderzoek naar gezondheidsrisico’s van werkmaterialen): 0,2 ppm
- TLV-TWA (Amerikaanse conferentie van overheidsindustriële hygiënisten drempelwaarde – tijdgewogen gemiddelde): 0,25 ppm
Referenties
- Maleic and Fumaric Acids; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_053
- https://pubchem.ncbi.nlm.nih.gov/compound/Maleic-Anhydride
- Method for producing cyclobutane tetracarboxylic acid derivative. – https://patents.google.com/patent/WO2015108168A1/en
