4-Methyl-2-pentanon: productie, reacties en toepassingen

4-Methyl-2-pentanon is een kleurloze vloeistof met een minder waarneembaar ketonachtig aroma.
Het is slecht oplosbaar in waterige media, maar is compatibel met conventionele organische oplosmiddelen. Het kan een azeotroop vormen met water en met een aanzienlijk aantal oplosmiddelen.
Ter illustratie: de azeotroop die met water is gevormd (kookpunt van 87,9 °C) bevat 75,7 gew.% 4-methyl-2-pentanon, terwijl die gevormd met n-butanol (kookpunt van 114,4 °C) 70 gew.% 4-methyl-2-pentanon bevat.
Inhoudsopgave
1. Production of 4-Methyl-2-pentanone
De industriële synthese van 4-methyl-2-pentanon kan worden bereikt via twee processen met aceton of isopropylalcohol als uitgangsmateriaal:
1.1. Een proces in drie stappen, beginnend bij aceton via diacetonalcohol en mesityloxide, met de daaropvolgende hydrogenering
In de beginfase ondergaat aceton condensatie onder invloed van een alkalikatalysator. Vervolgens ondergaat de aldus gevormde diacetonalcohol dehydratie in de vloeibare fase over een zure katalysator, zoals fosforzuur of zwavelzuur, bij een temperatuurbereik van 90 – 130 °C, wat mesityloxide met een hoge selectiviteit oplevert.
Selectieve hydrogenering van de koolstof-koolstof dubbele binding aanwezig in mesityloxide kan worden uitgevoerd met behulp van verschillende katalysatoren zoals palladium in zowel de gas- als de vloeibare fase. Deze transformatie vertoont een uitzonderlijke selectiviteit.
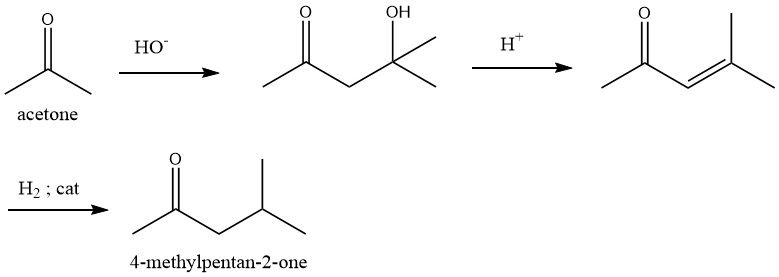
Dehydratatie- en hydrogeneringsprocessen kunnen worden gecombineerd tot één stap voor de synthese van 4-methyl-2-pentanon.
1.2. Een tweestapsproces met aceton via mesityloxide
Dit proces is van minder industriële betekenis, waarbij aceton in de eerste stap wordt omgezet in mesityloxide en vervolgens in de tweede stap wordt gehydrogeneerd tot 4-methyl-2-pentanon.
Koperchromiet of zirkoniumfosfaat zijn de voorkeurskatalysatoren voor de condensatiereactie en palladium op aluminiumoxide voor de hydrogeneringsreactie.
Bijproducten zoals 4-methyl-2-pentanol kunnen ook worden gevormd.
1.3. Een éénstapsproces van aceton en waterstof
De éénstapsproductie van 4-methyl-2-pentanon gebruikt een combinatie van kationenwisselaar met palladium als katalysator.
De reactie wordt uitgevoerd bij 130 °C en 0,5 – 5,0 MPa, waarbij aceton en waterstof worden gevoed over een palladium-beladen katalysator. Dit proces vertoont een selectiviteit van meer dan 95% bij een conversie van minder dan 50%.
De productie van 4-methyl-2-pentanon als bijproduct bij de dehydrogenering van isopropylalcohol, wat leidt tot een verhoogde productie van aceton, heeft de laatste tijd aan belang gewonnen.
2. Chemische reacties van 4-methyl-2-pentanon
4-Methyl-2-pentanon kan autoxidatie ondergaan om peroxiden te vormen. Studies hebben aangetoond dat bij verdamping van 4-methyl-2-pentanon-watermengsels onder lucht, de waterige fase een gevaarlijke en toenemende concentratie peroxide vertoont.
Peroxide kan ook direct worden verkregen door oxidatie met 50% waterstofperoxide in aanwezigheid van zuren.
Bij condensatiereacties met carbonylverbindingen zoals aceton is de α-methylgroep meestal reactief. Alleen formaldehyde kan echter condensatiereacties ondergaan met de α-methyleengroep.
Industriële processen zoals hydrogenering en reductieve aminering kunnen worden uitgevoerd met de ketogroep.
3. Toepassingen van 4-methyl-2-pentanon
De primaire toepassing van 4-methyl-2-pentanon is als oplosmiddel voor vinyl-, epoxy- en acrylharsen, natuurlijke harsen en nitrocellulose.
Bovendien is het een veelzijdig extractiemiddel dat wordt gebruikt bij de productie van antibiotica of de eliminatie van paraffines uit minerale olie om smeeroliën te genereren.
De betekenis van 4-methyl-2-pentanon als tussenproduct voor synthese is relatief laag. Het belangrijkste product dat uit deze verbinding wordt afgeleid, is 4-methyl-2-pentanol, dat wordt verkregen via hydrogenering van het keton.
Bovendien is 4-methyl-2-pentanonperoxide van belang als polymerisatie-initiator voor ethyleen en als verharder voor onverzadigde polyesterharsen.
Referentie
- Ketones; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a15_077
