Carbazolo: proprietà, produzione e usi

Il carbazolo è un idrocarburo aromatico eterociclico con formula chimica C12H9N. Fu isolato per la prima volta dal catrame di carbone nel 1872 da Graebe e Glaser. La sua struttura presenta un dibenzopirrolo costituito da un anello a cinque elementi contenente azoto fuso a due anelli benzenici.
sommario
1. Proprietà fisiche del carbazolo
Il carbazolo è un solido cristallino bianco-giallo pallido con un odore distinto. Le sue principali proprietà fisiche includono:
- Massa molare: 167,21 g/mol
- Punto di fusione: 246 °C
- Punto di ebollizione: 354,8 °C a 101,3 kPa
- Densità: 1,1035 g/cm3 a 18 °C
- Morfologia cristallina: piastre o tavole; sublimabile
- Solubilità:
- Altamente solubile: acetone, piridina
- Moderatamente solubile: etere dietilico, etanolo
- Leggermente solubile: cloroformio, acido acetico, tetracloruro di carbonio e disolfuro di carbonio
- Molto solubile: acido solforico concentrato
- Praticamente insolubile: acqua (≈ 1 mg/L a 25 °C)
- Proprietà termodinamiche:
- Calore di fusione: 176,3 kJ/kg
- Calore di combustione: 3,719 × 104 kJ/kg a 25 °C
2. Reattività chimica del carbazolo
Il carbazolo mostra una reattività diversa a causa della sua natura aromatica e della coppia solitaria sul suo atomo di azoto. Ecco una ripartizione delle sue principali reazioni chimiche:
1. N-sostituzione e alchilazione
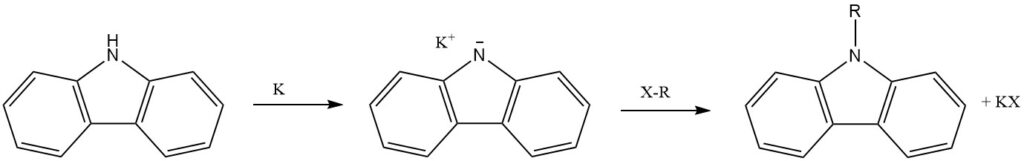
L’N-idrogeno del carbazolo, che agisce come un’ammina secondaria, subisce facilmente la sostituzione con metalli alcalini (Li, Na e K). Ciò porta all’introduzione di altri gruppi funzionali attraverso ulteriori reazioni.
L’atomo N del carbazolo può essere alchilato, introducendo sostituenti N-alchilici con proprietà variabili.
2. Alogenazione, nitrazione e solfonazione

Le reazioni di sostituzione elettrofila come alogenazione, nitrazione e solfonazione hanno come bersaglio preferenzialmente le posizioni 3 e 6 sull’anello del carbazolo a causa della loro maggiore densità elettronica. Sono necessarie condizioni difficili per un’ulteriore sostituzione nelle posizioni 1, 8 e altre, che portano ai derivati 1,3,6 e 1,3,6,8.
Può anche subire reazioni di alchilazione e acilazione sull’anello aromatico.
3. Idrogenazione
Il carbazolo subisce facilmente idrogenazione, producendo derivati parzialmente o completamente saturi. A seconda delle condizioni di reazione, si può formare 1,2,3,4-tetraidro-, esaidro- o persino dodecaidrocarbazolo.
4. Ossidazione
L’ossidazione con forti agenti ossidanti come cromati o permanganati scinde l’anello aromatico, formando diversi prodotti dicarbazilici a seconda del sito di scissione. Il 3,3′-dicarbazile si forma per ossidazione del cromato, mentre il 9,9′-dicarbazile si ottiene per ossidazione con permanganato.
5. Carbossilazione

Il trattamento con carbonati di metalli alcalini e anidride carbonica può introdurre gruppi di acido carbossilico sull’anello del carbazolo. La posizione del gruppo carbossilico (3- o 1-) dipende dalla temperatura di reazione.
3. Produzione di carbazolo
Punti chiave:
- Il carbazolo è facilmente disponibile nel catrame di carbone e può essere separato dall’antracene utilizzando vari metodi.
- Esistono percorsi di sintesi, ma sono attualmente meno competitivi dell’estrazione del catrame di carbone.
- La moderna cristallizzazione a fusione ad alta temperatura offre un approccio promettente per una produzione sostenibile di carbazolo
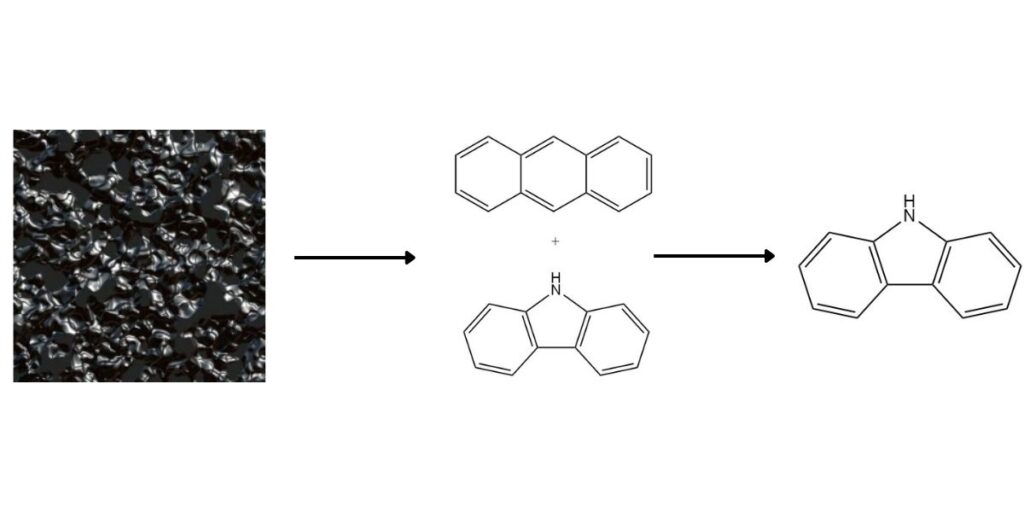
Il carbazolo, in quanto prezioso composto aromatico eterociclico, è presente nel catrame di carbone ad alta temperatura a una concentrazione media dello 0,9%. Sebbene tradizionalmente ottenuto come coprodotto durante la produzione di antracene, diversi metodi offrono un recupero dedicato del carbazolo.
1. Separazione dall’antracene:
Il punto di ebollizione più elevato del carbazolo e la solubilità differenziale facilitano la sua separazione dall’antracene. I metodi comuni includono:
- Estrazione o complessazione: Utilizzo di solventi come piridina, chetoni, miscele di benzene/metanolo o agenti specifici come N-metilpirrolidone, dimetilacetamide, dialchil solfossidi o dialchilformammidi.
- Distillazione azeotropica: Utilizzo di glicole etilenico per sfruttare la formazione di un azeotropo con carbazolo, consentendo la separazione mediante distillazione frazionata.
- Idrogenazione selettiva: Conversione dell’antracene in derivati idrogenati lasciando il carbazolo non influenzato.
2. Separazione chimica:
Storicamente, metodi come l’idrossido di potassio o la fusione di acido solforico concentrato venivano utilizzati per la separazione del carbazolo. Tuttavia, la loro redditività economica è diminuita.
3. Purificazione da liquori madri di piridina:
I liquori madri di piridina generati durante la purificazione dell’antracene possono essere concentrati e ricristallizzati dal clorobenzene per produrre carbazolo puro.
4. Percorsi di sintesi per il carbazolo
Esistono diversi metodi di sintesi per la produzione di carbazolo, ma la loro importanza industriale è limitata rispetto all’estrazione di catrame di carbone:
- Conversione di cicloesanone azina in ottaidrocarbazolo seguita da deidrogenazione.
- Ciclizzazione riduttiva di 2-nitrobifenile.
- Deidrogenazione e ciclizzazione di vari precursori come difenilammina, o-amminobifenile o N-cicloesilideneanilina.
Un metodo moderno ed efficiente per il recupero del carbazolo dal catrame di carbone è la cristallizzazione a fusione ad alta temperatura e senza solventi. Questo processo offre vantaggi in termini di impatto ambientale e di economicità.
4. Utilizzi del carbazolo
Nonostante venga estratto principalmente dal catrame di carbone (oltre 3.500 tonnellate all’anno), il carbazolo è utilizzato in vari settori, tra cui: coloranti e pigmenti, pesticidi e polimeri, materiali ottici e diodi ad emissione luminosa, nonché nell’edilizia e negli adesivi.
Coloranti e pigmenti:
- Blu idrogeno: la condensazione del carbazolo con p-nitrosofenolo e la successiva solforazione producono questo colorante blu di zolfo di importanza commerciale.
- Coloranti naftolo AS e antrachinone: il carbazolo funge da precursore per vari azo e coloranti antrachinonici utilizzati in applicazioni tessili e industriali.
- Coloranti stirilici: l’N-etilcarbazolo consente la sintesi di coloranti stirilici vivaci utilizzati in diversi materiali e prodotti.
- Coloranti e pigmenti diossazinici: l’N-etil-3-amminocarbazolo svolge un ruolo chiave nella creazione di questi preziosi coloranti per pigmenti organici e coloranti azinici.
- Il carbazolo contribuisce alla produzione di coloranti reattivi, noti per il loro forte legame con le fibre sintetiche.
Pesticidi e Polimeri:
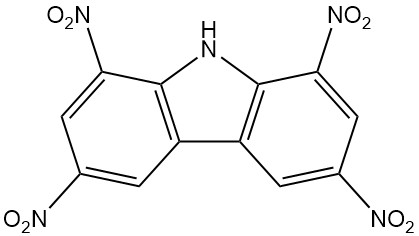
- Nirosan: 1,3,6,8-tetranitrocarbazolo, un insetticida efficace, è disponibile in commercio dal 1939.
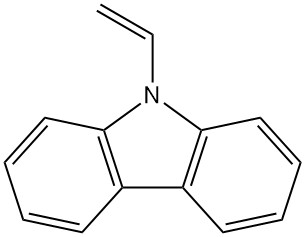
- Poli(vinilcarbazolo): la polimerizzazione dell’N-vinilcarbazolo produce questo polimero stabile termicamente e chimicamente (Luvican, Polectron) utilizzato per applicazioni elettriche grazie alla sua bassa perdita dielettrica e fotoconduttività.
Materiali ottici e diodi a emissione luminosa:
- Materiali fotorefrattivi: i polimeri di metacrilato carbazolo combinano fotoconduttività e proprietà elettroottiche, rendendoli ideali per l’archiviazione di dati ad alta densità, l’elaborazione di immagini e l’elaborazione dati.
- Emettitori di tripletto: i composti di carbazolo trovano impiego come materiali host per emettitori di tripletto nei diodi organici a emissione di luce (OLED), migliorandone l’efficienza e la luminosità.
Costruzione e adesivi:
- Resine Novolak: Il carbazolo reagisce con fenoli e formaldeide per formare questi polimeri resistenti al calore, preziosi per adesivi e rivestimenti.
- Plasticizzante per calcestruzzo: La co-condensazione del carbazolo con fenoli e formaldeide, seguita dalla solfonazione, produce plastificanti efficaci per calcestruzzo.
Polimeri ad alte prestazioni:
Poliammidi: La condensazione termica del 3,6-diaminocarbazolo con acidi dicarbossilici produce polimeri elastici e termicamente stabili poliammidi con diverse applicazioni.
5. Derivati del carbazolo

| Derivato | Numero CAS | Formula | Massa molare (g/mol) | Punto di fusione (°C) | Sintesi |
|---|---|---|---|---|---|
| N-etilcarbazolo | 86-28-2 | C14H13N | 195,27 | 68 | Etilazione del carbazolo con solfato di dietile |
| 1,3,6,8-tetranitrocarbazolo | 4543-33-3 | C12H5O8N5 | 347,20 | 312 | Nitrazione del carbazolo con acido nitrico e solforico |
| N-Vinilcarbazolo | 1484-13-5 | C14H11N | 193,25 | 65 | Da carbazolo-potassio con ossido di etilene o cloruro di vinile, oppure da carbazolo e acetilene |
6. Tossicologia del carbazolo
Il carbazolo presenta una bassa tossicità orale acuta, con valori di LD50 superiori a 5000 mg/kg nei ratti. Tuttavia, la somministrazione intraperitoneale nei topi rivela una LD50 significativamente inferiore di 200 mg/kg, suggerendo una tossicità dipendente dalla via di somministrazione.
L’esposizione professionale al carbazolo è stata associata a follicolite e comedoni, sebbene studi sugli animali dimostrino un potenziale minimo di irritazione cutanea e oculare, anche sotto fotoattivazione.
Il carbazolo subisce glucuronidazione e successiva escrezione urinaria nei ratti e nei conigli.
L’assunzione di carbazolo ad alto dosaggio (270-1050 mg/kg di peso corporeo/giorno) per 96 settimane ha indotto carcinomi epatici e prestomaci nei topi B6C3F1, ma non è stata osservata alcuna attività tumorigenica nei topi neonati dopo iniezioni intraperitoneali.
Sulla base di prove limitate, il carbazolo è classificato come Gruppo 3 (non classificabile per cancerogenicità per l’uomo) dall’Agenzia Internazionale per la Ricerca sul Cancro (IARC). Non ha mostrato attività mutagena in vari test batterici.
Il 9-etilcarbazolo, un derivato, ha mostrato un debole effetto mutageno in un ceppo batterico ma era inattivo in un altro, suggerendo un potenziale mutageno limitato.
L’applicazione cutanea di carbazolo fino a 250 mg/kg di peso corporeo/giorno durante la gravidanza non ha indotto anomalie nello sviluppo fetale del ratto.
Riferimenti
- Carbazole; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a05_059.pub2
- Carbazole; – https://www.sigmaaldrich.com/US/en/product/sigma/c5132
- https://en.wikipedia.org/wiki/Carbazole
