Acido adipico: proprietà, reazioni, produzione e usi
Cos’è l’acido adipico?
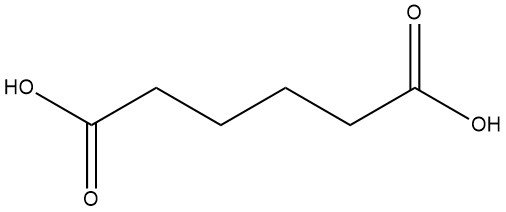
L’acido adipico, noto anche come acido esandioico o acido 1,4-butandicarbossilico, è un composto organico con formula C6H10O4. È un acido dicarbossilico alifatico ampiamente utilizzato che appare come un solido cristallino bianco.
Sebbene la sua presenza in natura sia limitata, viene sintetizzato su larga scala a livello globale. L’applicazione principale di questo composto è nella produzione di poliammide nylon 66, scoperta da W. H. Carothers della DuPont nei primi anni ’30.
Da allora, la produzione di fibre di poliammide nylon 66 è emersa come un processo dominante nell’industria delle fibre sintetiche su scala globale.
Sommario
1. Proprietà fisiche dell’acido adipico
L’acido adipico si ottiene sotto forma di cristalli incolori e inodori con un caratteristico sapore acido. Dimostra un’elevata solubilità in metanolo ed etanolo, ed è anche solubile in acqua e acetone.
Tuttavia, la sua solubilità in cicloesano e benzene è piuttosto limitata. Quando cristallizzato, l’acido adipico forma prismi monoclini quando si utilizzano acqua, acetato di etile o acetone/etere di petrolio come solventi.
Ecco alcune delle sue proprietà fisiche:
| Proprietà | Valore |
|---|---|
| Punto di fusione, °C | 152,1 |
| Punto di ebollizione, °C a 101,3 kPa | 337,5 |
| Punto di ebollizione, °C a 13,3 kPa | 265 |
| Punto di ebollizione, °C a 2,67 kPa | 222 |
| Punto di ebollizione, °C a 0,67 kPa | 191 |
| punto di ebollizione, °C a 0,133 kPa | 159,5 |
| Densità relativa (170 °C) | 1,085 |
| Densità apparente, kg/m³ | 600 - 700 |
| Solubilità, g/100 g di acqua a 15 °C | 1,42 |
| Solubilità, g/100 g di acqua a 40 °C | 4,5 |
| Solubilità, g/100 g di acqua a 60 °C | 18,2 |
| Solubilità, g/100 g di acqua a 80 °C | 73 |
| Solubilità, g/100 g di acqua a 100 °C | 290 |
| Costanti di dissociazione k1 | 4,6 × 10-5 |
| Costanti di dissociazione k2 | 3,6 × 10-6 |
| Calore specifico del liquido (200 °C), kJ kg⁻¹ K⁻¹ | 2,719 |
| Calore specifico del vapore (300 °C), kJ kg⁻¹ K⁻¹ | 1,680 |
| Calore di fusione, kJ/kg | 115 |
| Calore di vaporizzazione, kJ/kg | 549 |
| Calore di soluzione in acqua, kJ/kg a 10 - 20 °C | -214 |
| Calore di soluzione in acqua, kJ/kg a 90 - 100 °C | -241 |
| Viscosità di fusione, mPa · s a 160 °C | 4,54 |
| Viscosità di fusione, mPa · s a 193 °C | 2,64 |
2. Reazioni chimiche dell’acido adipico
L’acido adipico mostra stabilità in condizioni atmosferiche, ma riscaldando l’acido fuso oltre i 230-250 °C, si verifica un certo grado di decarbossilazione, che porta alla formazione di ciclopentanone, con un punto di ebollizione di 131 °C.
Questa reazione è notevolmente catalizzata da sali metallici, tra cui ferro, calcio e bario.
Rispetto agli acidi glutarico o succinico, l’acido adipico dimostra una tendenza molto minore a formare anidridi cicliche per perdita di acqua.
L’acido adipico mostra reattività a uno o entrambi i gruppi di acido carbossilico, impegnandosi nella formazione di sali, esteri, ammidi, nitrili e altri composti.
In genere resiste all’azione della maggior parte degli agenti ossidanti, come dimostrato dalla sua produzione in acido nitrico, ma quando esposto ad acido nitrico a temperature superiori a 180 °C, l’acido adipico subisce un attacco autocatalitico, producendo anidride carbonica, acqua e ossidi di azoto.
3. Produzione di acido adipico
Nelle fasi iniziali della produzione commerciale di acido adipico, un processo in due fasi prevedeva l’ossidazione ad aria del cicloesano. La prima fase era l’ossidazione del cicloesano a cicloesanolo e cicloesanone a bassa conversione, seguita da un processo ad alta conversione che ossidava ad aria la miscela per produrre acido adipico.
Tuttavia, a partire dall’anno 2000, tutta la produzione su larga scala di acido adipico utilizza l’ossidazione ad acido nitrico di cicloesanolo, cicloesanone o una miscela di entrambe le sostanze nota come olio chetone-alcol (KA).
Le principali differenze tra questi processi commerciali risiedono nel metodo di produzione dell’olio KA. In genere, i sei atomi di carbonio che formano la struttura portante dell’acido adipico provengono dal benzene, che viene idrogenato a cicloesano, o dal fenolo, che viene idrogenato a cicloesanolo.
Successivamente, il cicloesano viene ossidato con aria per produrre l’olio KA. Negli ultimi due decenni, si è assistito a un notevole spostamento verso il processo più conveniente basato sul cicloesano.
3.1. Produzione di acido adipico mediante ossidazione del cicloesanolo con acido nitrico
3.1.1. Meccanismo di reazione
Il secondo passaggio del processo di produzione convenzionale dell’acido adipico, sviluppato da DuPont alla fine degli anni ’40, prevede l’ossidazione del cicloesanolo, del cicloesanone o di una miscela di entrambi utilizzando acido nitrico. L’acido adipico si ottiene con una resa superiore al 90%.
Durante questo processo, si formano come sottoprodotti principali anidride carbonica, ossidi di azoto e alcuni acidi dicarbossilici a massa molecolare inferiore. Inoltre, vengono rilevati anche alcuni sottoprodotti derivanti da impurità presenti nell’olio KA di partenza.
Il meccanismo chimico di questa reazione è stato inizialmente discusso nel 1956, includendo considerazioni sulla cinetica e sulla progettazione del reattore. La Figura 1 fornisce un riepilogo dei risultati di queste indagini.
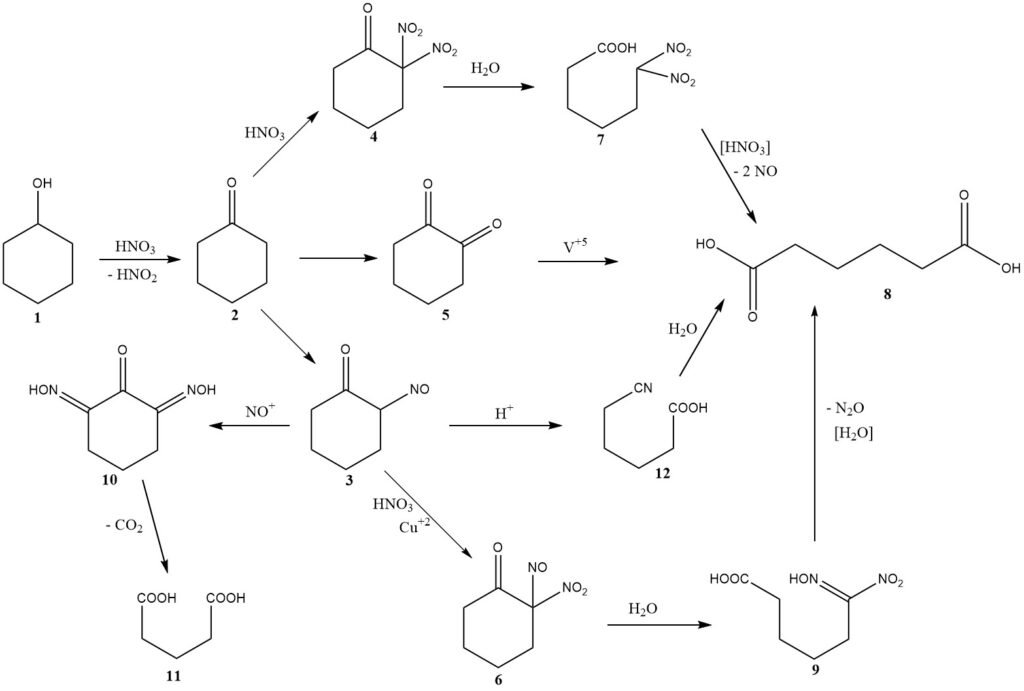
L’ossidazione del cicloesanolo (1) produce cicloesanone (2) generando acido nitroso. Quindi, il cicloesanone subisce uno dei tre possibili percorsi che portano alla formazione di acido adipico (8).
Il percorso principale coinvolge la nitrosazione per produrre 2-nitrosocicloesanone (3), che poi reagisce ulteriormente con l’acido nitrico per formare 2-nitro-2-nitrosochetone (6).
La scissione idrolitica di questo intermedio produce acido 6-nitro-6-idrossiminoesanoico, noto anche come acido nitrolico (9), che si scompone ulteriormente per dare acido adipico e protossido di azoto, i principali prodotti di riduzione dell’acido nitrico non recuperati.
In genere, 2,0 moli di acido nitrico vengono convertite in protossido di azoto per ogni mole di acido adipico prodotto.
A temperature più elevate, un secondo percorso diventa significativo, coinvolgendo la nitrazione, che porta alla formazione di dinitrochetone (4).
I primi ricercatori hanno proposto un terzo percorso, che coinvolge la formazione intermedia di 1,2-dichetone (5) o del suo dimero, in cui è richiesto l’uso di un catalizzatore al vanadio per ottenere una buona resa di acido adipico. La presenza di vanadio suggerisce il suo contributo significativo alla resa complessiva.
Il nitrosochetone intermedio (3) può subire due importanti reazioni collaterali. La nitrosazione multipla porta a un intermedio (10), che perde anidride carbonica per produrre acido glutarico (11) o acido succinico attraverso una successiva reazione con acido nitrico.
Il rame metallico viene aggiunto all’acido nitrico per inibire queste reazioni. In condizioni specifiche con una concentrazione allo stato stazionario relativamente elevata del nitrosochetone (3) o dell’ossiminochetone tautomerico, si verifica un riarrangiamento di tipo Beckmann, che porta alla formazione minore di acido 5-cianopentanoico (12), che viene lentamente idrolizzato in acido adipico.
3.1.2. Processi di ossidazione dell’acido nitrico commerciale
Il processo di ossidazione dell’acido nitrico per convertire il cicloesanolo-cicloesanone (KA) in acido adipico rimane simile alla prima letteratura brevettuale, ma sono stati fatti progressi nella rimozione dei sottoprodotti, nel recupero del catalizzatore e dell’acido nitrico e nella riduzione delle emissioni di protossido di azoto, un gas serra che veniva tradizionalmente rilasciato nell’atmosfera.
A causa della natura corrosiva dell’acido nitrico, gli impianti di produzione sono costruiti utilizzando materiali come acciaio inossidabile (tipo 304L o migliore) o titanio nelle aree ad alta esposizione.
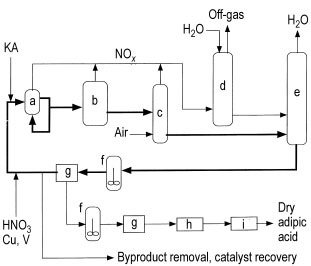
a) Reattore; b) Reattore di depurazione; c) Sbiancatore di NOx; d) Assorbitore di acido nitrico; e) Concentratore; f) Cristallizzatore; g) Filtro o centrifuga; h) Essiccatore; i) Refrigeratore
Il processo in genere prevede un reattore (a), che funziona come un grande scambiatore di calore, operando a 60 – 80 °C e 0,1 – 0,4 MPa di pressione. Il reattore riceve il liquore madre di acido nitrico riciclato (NML), il materiale di alimentazione KA, l’acido di reintegro con il 50 – 60% di acido nitrico e un catalizzatore rame-vanadio.
Il tempo di residenza nel reattore è inferiore a 5 minuti. Alcune strutture utilizzano un secondo reattore (b) a temperatura elevata (110 – 120 °C) per completare la reazione e ridurre le impurità prima di procedere alla cristallizzazione.
La reazione è altamente esotermica (6280 kJ/kg) e sono stati brevettati progetti di reattori innovativi per controllare il calore di reazione e ridurre al minimo l’uso di energia. Viene mantenuto un surplus di NML riciclato nel flusso di alimentazione KA (almeno 3:1 fino a 1000:1) per controllare la reazione e migliorare la resa.
Il flusso di prodotto subisce diverse fasi, tra cui il passaggio attraverso uno sbiancatore (c) per rimuovere gli ossidi di azoto disciolti in eccesso, che vengono poi recuperati come acido nitrico nell’assorbitore (d).
Il gas di scarico dall’assorbitore può essere utilizzato per avviare l’ossidazione a temperature più basse facendolo passare attraverso il flusso di alimentazione KA prima di alimentarlo all’ossidatore. L’acqua prodotta nel processo viene rimossa in un alambicco di concentrazione (e) azionato sotto vuoto.
Il flusso di prodotto concentrato viene riciclato nuovamente al reattore con una parte deviata per il recupero del prodotto o passato direttamente al recupero del prodotto prima di riciclare il filtrato NML. L’acido adipico grezzo viene estratto dal ciclo NML tramite cristallizzazione (f) e successivamente filtrato o centrifugato (g).
Questo flusso di effluenti, contenente concentrazioni più elevate di acido glutarico, acido succinico e sottoprodotti, viene ulteriormente elaborato per recuperare i catalizzatori di vanadio e rame e rimuovere gli acidi dei sottoprodotti. Il recupero del metallo viene in genere ottenuto tramite scambio ionico.
L’acido adipico grezzo dal primo cristallizzatore (g) subisce una o più fasi di ricristallizzazione prima di procedere a un essiccatore (h) e a un raffreddatore (i). In alternativa, se non è richiesto acido adipico secco, i cristalli dalla centrifuga/filtro (g) possono essere sciolti in acqua e aggiunti a una soluzione di 1,6-esandiammina acquosa per produrre sale di nylon.
Sono stati descritti ulteriori miglioramenti al processo convenzionale, in particolare per quanto riguarda la separazione e il recupero dei sottoprodotti dell’acido dibasico.
A seconda dell’uso finale, l’acido adipico grezzo può essere raffinato a diversi livelli, ma la ricristallizzazione dall’acqua è un approccio comune. Si è affermato che il riflusso dell’acido adipico grezzo in acido nitrico al 60% con vanadio disciolto produce un prodotto di alta qualità.
3.2. Produzione di acido adipico tramite percorsi basati sul butadiene
All’inizio degli anni ’70, la BASF avviò un vasto programma di ricerca per produrre dimetil adipato, un diestere che poteva essere successivamente idrolizzato in acido adipico. Il processo prevedeva la carbometossilazione del butadiene utilizzando monossido di carbonio e metanolo, catalizzata da cobalto e piridina ad alta pressione.
Questa reazione ha prodotto metil 3-pentenoato, che è stato separato dai sottoprodotti tramite distillazione. Successivamente, una seconda fase di carbometossilazione a pressione inferiore, con un rapporto piridina/cobalto ridotto, ha portato alla formazione di dimetil adipato.
L’idrolisi del diestere in acido adipico e metanolo è stata ottenuta tramite un processo catalitico ad alta resa. Nel complesso, il processo ha mostrato una resa approssimativa di circa il 70% dal butadiene. Sebbene dimostrato su scala di impianto pilota, non è stato ancora commercializzato.
A metà degli anni ’80, la DuPont ha anche avviato un programma significativo che prevedeva un percorso basato sul butadiene per l’acido adipico. Contrariamente all’approccio diestere della BASF, il metodo della DuPont prevedeva la diidrocarbossilazione diretta del butadiene in acido adipico (come mostrato nella Figura 3).
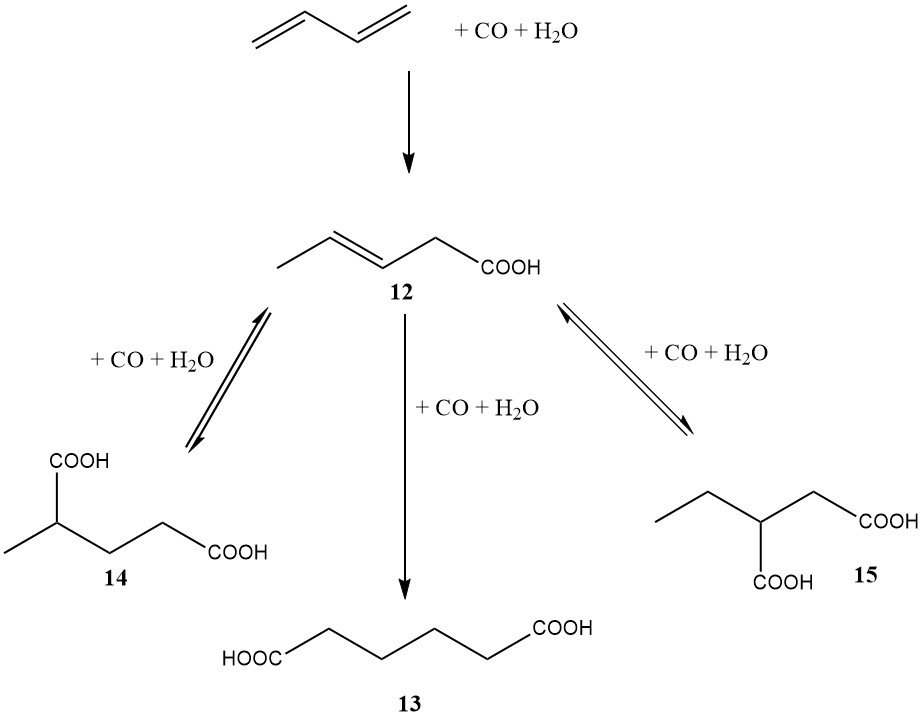
Il primo passaggio, catalizzato da palladio, rodio o iridio, ha portato principalmente all’acido 3-pentenoico. Il secondo passaggio, catalizzato da rodio o iridio, ha portato alla formazione di acido adipico (13), acido 2-metilglutarico (14) e acido 2-etilsuccinico (15).
Il vantaggio di questo processo era la capacità di isomerizzare gli acidi 2-metilglutarico e 2-etilsuccinico in acido adipico utilizzando lo stesso sistema catalizzatore. Il catalizzatore richiedeva un promotore alogenuro, come l’acido iodidrico.
L’acido pentanoico, un acido carbossilico saturo e un sottoprodotto del processo, serviva in genere come solvente. Dalla fine degli anni ’80, molte importanti aziende chimiche hanno ottenuto numerosi brevetti per varianti di questi percorsi basati sul butadiene.
3.3. Altri percorsi
Oltre alla convenzionale ossidazione in due fasi aria/acido nitrico del cicloesano e alla carbossilazione/carbometossilazione del butadiene, sono stati esplorati vari altri processi per la produzione di acido adipico.
Monsanto ha condotto ricerche sulla dicarbonilazione catalizzata da alogenuro di palladio di 2-buteni 1,4-disostituiti. Questo processo comporta la produzione di acido adipico da 1,4-dimetossi-2-butene, monossido di carbonio e cloruro di palladio a 100 °C, seguita da idrogenazione e idrolisi del risultante estere dimetilico insaturo.
È stata anche studiata l’ossidazione in una fase del cicloesano utilizzando acido nitrico, biossido di azoto o aria. L’ossidazione in una fase del cicloesano completamente in aria è particolarmente interessante dal punto di vista economico e ha ricevuto ampia attenzione da parte della ricerca.
I primi studi sono stati condotti da Gulf Research and Development, Asahi Chemical Industries e altri gruppi. Ad esempio, il cicloesano può essere ossidato in un unico passaggio ad acido adipico con una resa del 70-75% in presenza di un catalizzatore di acetato di cobalto in acido acetico come solvente.
Di recente, c’è stato un rinnovato interesse per questo approccio, che ha portato al rilascio di diversi brevetti ad aziende come Redox Corporation e Bayer.
L’acido adipico può anche essere prodotto dall’ozonolisi del cicloesene o aggiungendo un acido carbossilico al cicloesene e successivamente ossidando l’estere risultante con acido nitrico.
Inoltre, è stata descritta la formazione di derivati dell’acido adipico tramite l’accoppiamento elettrolitico di acrilati.
Questi processi alternativi rappresentano sforzi di ricerca in corso per sviluppare nuovi metodi per la sintesi dell’acido adipico.
4. Utilizzi dell’acido adipico
Circa l’80% del consumo globale di acido adipico è destinato alla produzione di fibre e resine di nylon 66.
Una quantità minore di acido adipico è ancora utilizzata in cattività per produrre adiponitrile.
Quantità significative di acido adipico vengono trasformate in esteri per varie applicazioni come plastificanti, lubrificanti e una gamma di resine poliuretaniche.
Gli esteri monomerici sono plastificanti essenziali per poli(cloruro di vinile) e altre resine, mentre gli esteri polimerici vengono utilizzati quando sono richiesti livelli di plastificante eccezionalmente elevati.
Le resine poliuretaniche che incorporano acido adipico sono create da poliisocianati e polioli poliestere (adipati) e trovano impiego in varie applicazioni.
L’acido adipico funge anche da acidificante nelle gelatine e nelle marmellate e agisce come agente tampone o neutralizzante in altri prodotti alimentari.
Inoltre, viene impiegato per modificare le proprietà dei poliesteri insaturi da utilizzare in plastiche rinforzate e rivestimenti alchidici.
L’acido adipico viene utilizzato nelle resine poliammidiche-epicloridrina per migliorare la resistenza all’umidità dei prodotti di carta.
Altre applicazioni varie includono il suo utilizzo in adesivi, insetticidi, concia, tintura e industrie tessili. Inoltre, l’acido adipico e gli acidi dibasici misti (DBA) vengono impiegati come tamponi nel trattamento di desolforazione dei gas di combustione nelle centrali elettriche.
5. Tossicologia e salute sul lavoro
L’acido adipico provoca una lieve irritazione e ha una bassa tossicità orale. Le dosi letali pubblicate (LDLo) sono 3600 mg/kg (ratto, orale), LD50 275 mg/kg (ratto o topo, i.p.) e LD50 1900 mg/kg (topo, orale).
Alcuni test di alimentazione cronica hanno mostrato aumenti ritardati del peso corporeo, alterazioni in alcuni enzimi e cambiamenti nei livelli di urea e cloruro nel sangue. Tuttavia, non è stata osservata alcuna attività teratogena negli studi che hanno coinvolto topi gravidi.
Studi sul metabolismo che hanno utilizzato ratti alimentati con acido adipico marcato con 14C hanno rivelato la presenza sia di acido adipico immodificato che di normali prodotti metabolici nelle urine.
L’esposizione all’acido adipico può causare irritazione alle mucose come gli occhi e le vie respiratorie, mentre l’esposizione prolungata alla pelle può causare secchezza o irritazione.
In caso di versamenti o perdite, il personale deve essere protetto dall’inalazione o dal contatto eccessivo con la pelle. La polvere deve essere controllata e devono essere prese misure per evitare scintille statiche. In caso di versamenti, l’area può essere lavata con acqua.
Sebbene non vi sia un TLV (Threshold Limit Value) o un MAK (Maximal Concentration Value) stabiliti, l’esposizione aerea all’acido adipico deve essere mantenuta al di sotto di quella di una polvere organica nociva: ACGIH (1979) raccomanda un TWA (Time-Weighted Average) di 8 ore di 10 mg/m³ per la polvere totale e 5 mg/m³ per la polvere respirabile. Il TLV OSHA per la polvere totale è di 15 mg/m3.
6. Derivati dell’acido adipico
6.1. Adiponitrile
Il principale derivato dell’acido adipico è l’adiponitrile, noto anche come 1,6-esanedinitrile o 1,4-dicianobutano, Mr 108.14 g/mol, punto di ebollizione 298 – 300 °C (a 101,3 kPa), 154 °C (a 1,3 kPa) e punto di congelamento 2,4 °C.
L’adiponitrile funge da intermedio nella produzione del componente principale del nylon 66, 1,6-esanediammina. I precedenti metodi di produzione prevedevano la conversione dell’acido adipico in dinitrile mediante disidratazione in fase liquida o vapore del sale di ammonio, utilizzando acido fosforico o un catalizzatore boro-fosforo. Tuttavia, questi metodi non sono più impiegati dai principali produttori di nylon 66.
Sono stati utilizzati vari metodi per la produzione di adiponitrile, tra cui i processi di Celanese, che hanno prodotto 1,6-esandiammina dall’ammonolisi di 1,6-esandiolo, ottenuta mediante idrogenazione dell’acido adipico.
6.2. Sali di acido adipico
L’acido adipico forma sali di metalli alcalini e di ammonio solubili in acqua, nonché sali alcalino-terrosi moderatamente solubili.
Le loro solubilità in 100 g di acqua sono le seguenti: sale di diammonio 40 g (14 °C), sale disodico 59 g di emiidrato (14 °C), sale dipotassico 65 g (15 °C), sale di calcio 4 g di monoidrato (13 °C) e 1 g di sale anidro (100 °C).
Il sale più comune è il poli(1,6-esandiammonio esanodioato), prodotto facendo reagire l’acido adipico con 1,6-esandiammina. Questo sale idrosolubile, un precursore del nylon 66, può essere comodamente spedito o immagazzinato prima della poliammidazione finale, durante la quale l’acqua viene rimossa.
6.3. Esteri e poliesteri dell’acido adipico
Gli esteri e i poliesteri dell’acido adipico costituiscono il più grande mercato non poliammidico per l’acido adipico. Gli esteri derivati da alcoli a catena lunga sono usati come plastificanti e lubrificanti, mentre quelli da alcoli a catena corta servono principalmente come solventi.
Il riflusso dell’acido adipico con metanolo in presenza di un catalizzatore acido produce monometil adipato, insieme al diestere. L’elettrolisi del sale del monoestere (sintesi di Kolbe) genera dimetil sebacato, un altro precursore della poliammide.
Gli esteri si dissolvono facilmente nella maggior parte dei solventi organici, con il dimetil adipato come solvente più comunemente usato e il di-2-etilesil adipato come plastificante più ampiamente usato. Altri plastificanti adipati semplici includono esteri n-ottilici, n-decilici, isodecilici e isoottilici.
I plastificanti polimerici più complessi, preparati da glicoli, rappresentano poco meno della metà dei plastificanti a base di acido adipico. I polioli poliestere a basso peso molecolare con gruppi terminali idrossilici sono usati con i poliisocianati per produrre resine poliuretaniche.
6.4. Anidridi dell’acido adipico
L’anidride dell’acido adipico è solitamente ottenuta disidratando l’acido adipico, con conseguente formazione della forma polimerica lineare. La distillazione dell’anidride polimerica può produrre la forma ciclica monomerica, che è altamente instabile e si converte facilmente nell’anidride polimerica lineare.
6.5. Amide dell’acido adipico
La diammide dell’acido adipico ha un punto di fusione di 228 °C ed è praticamente insolubile in acqua fredda. Tradizionalmente, è stata preparata trattando l’estere dimetilico con idrossido di ammonio concentrato o riscaldando il sale di diammonio dell’acido adipico in un flusso di ammoniaca. Varie ammidi sostituite possono essere sintetizzate dalle ammine utilizzando metodi di sintesi standard.
Riferimento
- Adipic Acid; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_269
