2-metil-2-propanolo: proprietà, produzione e usi
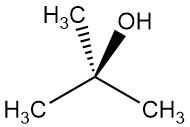
Il 2-metil-2-propanolo, noto anche come terz-butanolo, è l’alcol terziario più semplice con la formula chimica (CH3)3COH. È un cristallo solido incolore a temperatura ambiente. Tuttavia, fonde vicino alla temperatura ambiente (26 °C) per diventare un liquido viscoso con un odore simile alla canfora.
Sommario
1. Proprietà fisiche del 2-metil-2-propanolo
Il 2-metil-2-propanolo è un solido incolore a temperatura ambiente. È completamente miscibile con acqua, etanolo, etere dietilico e comuni solventi organici.
Le principali proprietà fisiche caratteristiche del 2-metil-2-propanolo sono presentate nella Tabella 1.
| Proprietà | Valore |
|---|---|
| Massa molare | 74,12 g/mol |
| Punto di fusione | 25,6 °C |
| Punto di ebollizione | 82,55 °C |
| Densità a 20 °C | 0,7867 g/cm³ |
| Indice di rifrazione a 20 °C | 1,3841 |
| Viscosità a 20 °C | 5,5 mPa⋅s |
| Calore specifico | 3,035 J g⁻¹ K⁻¹ |
| Calore di vaporizzazione | 535,78 J/g |
| Calore di fusione | 91,61 J/g |
| Calore di combustione | 35,694 kJ/g |
| Pressione critica | 39,7 hPa |
| Temperatura critica | 235 °C |
| Tensione superficiale a temperatura ambiente | 20,0 (25°C) mN/m |
| Costante dielettrica a temperatura ambiente | 11,4 |
| Solubilità in acqua | miscibile |
| Punto di infiammabilità | 11 °C |
| Limiti di accensione in aria, vol% | 2,3 - 8 % |
| Temperatura di accensione | 470 °C |
2. Reazioni chimiche del 2-metil-2-propanolo
Il 2-metil-2-propanolo subisce facilmente disidratazione per formare 2-metilpropene (isobutene) con acido solforico diluito e riscaldamento. Questa reazione non è importante a livello industriale a causa della disponibilità di 2-metilpropene dal petrolio crackizzato.
Non può essere deidrogenato selettivamente a causa della scissione delle molecole in condizioni estreme.
Il terz-butanolo può essere utilizzato in diverse reazioni di alchilazione con ammoniaca, ammine e composti aromatici.
Viene convertito in esteri terz-butilici con acidi inorganici e organici utilizzando catalizzatori acidi, ma è meno reattivo degli alcoli primari e secondari.
Il 2-metil-2-propanolo viene deprotonato con sodio o potassio metallico per produrre l’alcossido corrispondente. Il terz-butossido di potassio è un esempio comune di base non nucleofila nella chimica organica.
Rimuove i protoni acidi dai substrati basici, ma la sua struttura voluminosa impedisce la sua partecipazione a reazioni di sostituzione nucleofila come la sintesi dell’etere di Williamson o le reazioni SN2.
Il terz-butanolo reagisce con acido cloridrico e acido ipocloroso per produrre rispettivamente cloruro di terz-butile e ipoclorito di terz-butile.

3. Produzione di 2-metil-2-propanolo
Il 2-metil-2-propanolo viene prodotto industrialmente tramite due processi principali:
- Idratazione del 2-metilpropene
- Come sottoprodotto della produzione di ossido di propilene e metil terz-butil etere
3.1. Produzione di 2-metil-2-propanolo tramite idratazione del 2-metilpropene
Il 2-metil-2-propanolo viene prodotto principalmente tramite l’idratazione del 2-metilpropene (isobutene). Questo processo prevede i seguenti passaggi:

Preparazione del reagente: l’isobutene, la materia prima primaria, è spesso derivato dal cracking catalitico del petrolio o dalla deidrogenazione dell’n-butano. L’acqua, che funge da agente di idratazione, è in genere fornita come acqua purificata o riciclata dalle fasi precedenti. Il terz-butanolo stesso può essere presente nella materia prima o aggiunto intenzionalmente alla reazione.
Catalisi: le resine a scambio cationico funzionalizzate con acido solfonico fungono da catalizzatori preferiti grazie alla loro elevata attività, selettività verso la formazione di 2-metil-2-propanolo e facilità di rigenerazione. Le condizioni di reazione, tra cui temperatura (tipicamente tra 30-120 °C) e pressione (atmosferica o leggermente elevata), sono meticolosamente controllate per ottimizzare la conversione e ridurre al minimo le reazioni collaterali indesiderate.
Formazione di reazione e prodotto: la reazione di idratazione, un processo reversibile, converte isobutene e acqua in tert-butanolo. Spesso vengono impiegati reattori multistadio per utilizzare in modo efficiente il catalizzatore e massimizzare la conversione. Il controllo preciso dei rapporti dei reagenti, della temperatura e del caricamento del catalizzatore è fondamentale per garantire un’elevata selettività.
Separazione del prodotto: la distillazione separa efficacemente il prodotto tert-butanolo desiderato dall’isobutene non reagito, dagli idrocarburi inerti e dall’acqua. L’isobutene non reagito e l’acqua possono essere riciclati nel processo per migliorare l’efficienza delle risorse.
3.2. Sottoprodotto della produzione di ossido di propilene e metil terz-butil etere
Il 2-metil-2-propanolo si forma come prezioso sottoprodotto in diversi processi industriali, in particolare quelli che coinvolgono ossido di propilene e metil terz-butil etere.
1. Produzione di ossido di propilene:
Durante la produzione di ossido di propilene dal 2-metilpropano (isobutano), vengono generate circa 1,2 tonnellate di terz-butanolo per tonnellata di ossido di propilene prodotto. Il processo prevede una fase intermedia in cui il t-butil idroperossido si forma dall’isobutano.
2. Elaborazione del metil terz-butil etere:
La scissione del metil terz-butil etere in 2-metilpropene puro o 2-metil-2-propanolo può produrre terz-butanolo come sottoprodotto. Analogamente, la sintesi del metil terz-butil etere con tracce di acqua nella materia prima (metanolo e C4-olefine) genera anche terz-butanolo come sottoprodotto indesiderato.
La presenza di terz-butanolo come sottoprodotto richiede ulteriori passaggi di separazione e purificazione, aumentando i costi di produzione. Tuttavia, come vantaggi, fornisce una fonte facilmente disponibile di 2-metil-2-propanolo per applicazioni a valle, riducendo al minimo la dipendenza da metodi di produzione dedicati e migliorando l’efficienza del processo.
Sebbene non utilizzato commercialmente, il terz-butanolo può anche essere prodotto tramite reazione di Grignard facendo reagire acetone con cloruro di metilmagnesio.
4. Utilizzi del 2-metil-2-propanolo
Rispetto ad altri butanoli, il 2-metil-2-propanolo (t-BuOH) detiene una quota minore nel consumo globale. Tuttavia, il suo utilizzo è cresciuto costantemente dal 1990 prima di raggiungere un plateau negli ultimi anni.
- Il 2-metil-2-propanolo trova il suo utilizzo principale come solvente grazie alle sue proprietà favorevoli, tra cui la miscibilità con acqua e composti organici.
- Il terz-butanolo è utilizzato come reagente per introdurre il gruppo terz-butile in molecole organiche. Questa modifica è impiegata in varie applicazioni, come la sintesi di resine solubili in olio (ad esempio, terz-butilfenolo) e antiossidanti (ad esempio, trinitro-terz-butiltoluene).
- È anche un importante materiale di partenza per la produzione di perossidi organici, che servono come catalizzatori di polimerizzazione essenziali in vari processi industriali.
Il 2-metil-2-propanolo compete con il 2-propanolo come additivo nella benzina per prevenire la formazione di ghiaccio nel carburatore. Il suo metil etere è emerso brevemente come un booster di ottano e un sostituto del piombo negli anni ’80 e ’90, sperimentando un aumento significativo dei consumi (da 0,17 a 19 milioni di tonnellate tra il 1982 e il 1997). Tuttavia, le preoccupazioni ambientali hanno portato alla sua sostituzione finale con la miscelazione diretta di bioetanolo con benzina.
5. Tossicologia del 2-metil-2-propanolo
Il 2-metil-2-propanolo presenta una tossicità acuta relativamente bassa. I valori LD50 più bassi documentati sono 2.740 mg/kg (orale, ratti) e 2.000 mg/kg (cutaneo, conigli).
Effetti dell’esposizione:
- Acuto: a livelli di esposizione elevati, il tert-butanolo ha un effetto narcotico, caratterizzato da mal di testa, nausea, affaticamento e vertigini.
- Pelle: il contatto prolungato con 2-metil-2-propanolo nei conigli non ha causato irritazione cutanea. Negli esseri umani, a seguito del contatto con la pelle possono verificarsi lievi eritemi e iperemia.
- Ha un odore distinto e sgradevole.
Limiti di esposizione:
- Valore limite di soglia (TLV): 100 ppm (media ponderata nel tempo), 150 ppm (limite di esposizione a breve termine).
- Valore MAK (concentrazione massima sul posto di lavoro): 20 mL/m³.
- TRGS 900 (Regelwerk tecnico tedesco per sostanze pericolose): 20 mL/m³.
Riferimenti
- Butanols; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_463.pub3
- Process for production of tertiary butyl alcohol. – https://patents.google.com/patent/US4307257A/en
- Process for the preparation of tert-butanol. – https://patents.google.com/patent/EP1431264A1/en
- https://en.wikipedia.org/wiki/Tert-Butyl_alcohol
