Kaneelzuur: eigenschappen, productie en toepassingen
Wat is kaneelzuur?
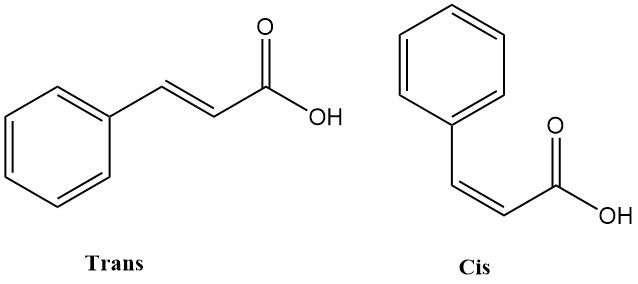
Kaneelzuur, ook bekend als 3-fenylpropeenzuur, is een organische verbinding met de chemische formule C6H5CH=CHCOOH die in de natuur voorkomt en commercieel verkrijgbaar is. Het bestaat in twee isomere vormen: cis en trans. De trans-isomeer is stabieler en is de overheersende vorm die van nature en commercieel wordt aangetroffen.
In 1780 werd kaneelzuur als kristallen uit kaneelolie geïsoleerd door Trommsdorf, die het aanzag voor benzoëzuur. Later, in 1835, identificeerden Dumas en Péligot het. Bertagnini synthetiseerde in 1856 met succes kaneelzuur uit benzaldehyde en acetylchloride.
Inhoudsopgave
1. Fysieke eigenschappen van kaneelzuur
De fysieke eigenschappen van trans-kaneelzuur zijn als volgt:
- CAS-nummer: 140-10-3
- Moleculair gewicht: 148,16 g/mol
- Fysiek uiterlijk: Kleurloze kristallen met een zwakke balsemgeur
- Smeltpunt: 133 °C
- Kookpunt: 300 °C (101,3 kPa) en 173 °C (13,3 kPa)
- Dichtheid: 1,2475 g/cm³ bij 4 °C en 1,0270 g/cm³ bij 180 °C
- pKa bij 25 °C: 4,46
- Verbrandingswarmte: 30,5 kJ/g
- Oplosbaarheid: Licht oplosbaar in water, zeer oplosbaar in polaire organische oplosmiddelen zoals ethanol, methanol, chloroform en aceton.
Het cis-kaneelzuur [102-94-3] bestaat in drie kristallijne vormen: cis-allocinnaminezuur (smeltpunt 68 °C) en twee cis-isocinnaminezuren (smeltpunt 58 °C en 42 °C).
Het lager smeltpunt cis-isocinnaminezuur is zeer onstabiel en wordt gemakkelijk omgezet in cis-allocinnaminezuur. Interconversie tussen de drie vormen is mogelijk door hun smelten te enten.
2. Chemische reactie van kaneelzuur
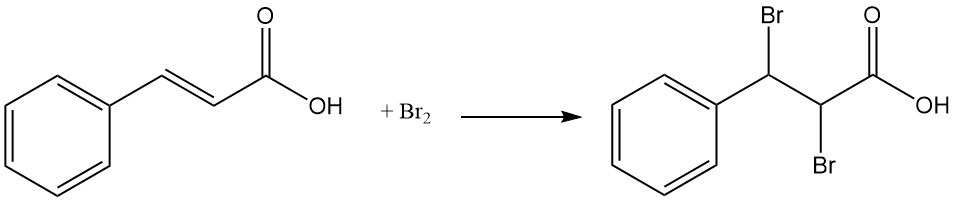
Kaneelzuur vertoont reactiviteitskenmerken van zowel zijn carboxylgroep als de olefinische dubbele binding.
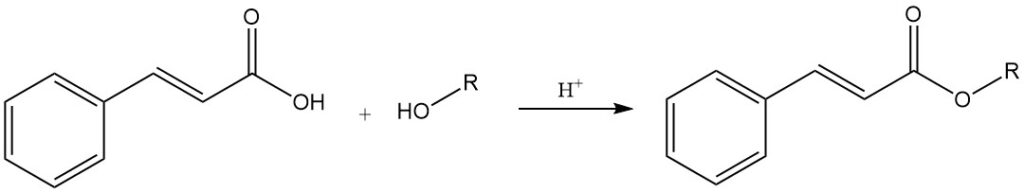
Kaneelzuur reageert met alcoholen om cinnamaatesters te vormen, waarvan sommige aanzienlijke smaak- en geureigenschappen bezitten. Het reageert met anorganische zuurchloriden (thionylchloride en fosforchloriden) om cinnamoylchloride te verkrijgen.
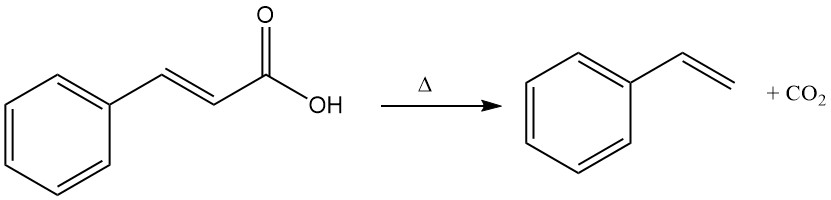
Kaneelzuur ondergaat thermische ontleding (decarboxylering) waarbij styreen en koolstofdioxide ontstaan.
Benzaldehyde kan worden geproduceerd door de dubbele binding te splitsen met oxidatiemiddelen of door verhitting met alkali.
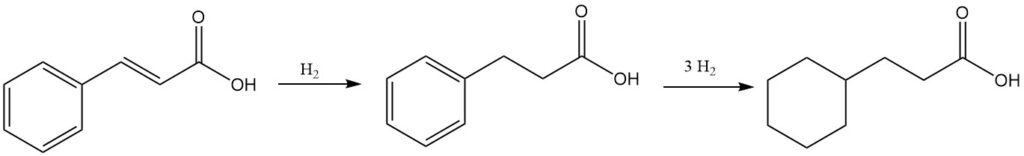
Kaneelzuur kan worden gehydrogeneerd om 3-fenylpropionzuur of 3-cyclohexylpropionzuur te geven, afhankelijk van de reactieomstandigheden.
Onder zonlicht vormt kaneelzuur dimeren, waaronder truxininezuur en α-truxillinezuur.
Substitutiereacties op de benzeenring van kaneelzuur worden zelden gebruikt om nieuwe derivaten te produceren.
3. Voorkomen in de natuur
Kaneelzuur, voornamelijk in zijn transvorm, wordt van nature aangetroffen in zowel vrije als veresterde vormen (cinnamaten) in verschillende plantaardige materialen.
De vrije vorm is te vinden in:
- Cassia-olie
- Olie uit Populus balsamifera extraheren
- Essentiële oliën uit bladeren en schillen van Citrus bigaradia
Verschillende cinnamaatesters worden aangetroffen in plantaardige materialen, waaronder methylcinnamaat dat wordt aangetroffen in de oliën van Alpinia-soorten en Ocimum canum-variëteiten en benzyl-, cinnamyl- en hydrocinnamylcinnamaten, die aanwezig zijn in Peru, Tolu, en storaxbalsemoliën. Siam- en Sumatra-benzoëharsen bevatten ook cinnamaten.
4. Productie van kaneelzuur
De commerciële productie van kaneelzuur bevoordeelt voornamelijk het trans-isomeer via verschillende gevestigde processen:
4.1. Productie van kaneelzuur door de Perkin-reactie
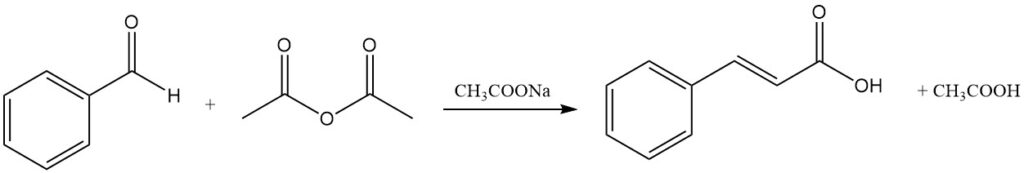
De Perkin-reactie is de traditionele commerciële methode voor het produceren van kaneelzuur door condensatie van benzaldehyde met azijnzuuranhydride in aanwezigheid van een katalysator, meestal natriumacetaat. Andere katalysatoren, zoals kaliumacetaat, tertiaire aminen, kaliumfosfaat en trimethylboraat, kunnen ook worden gebruikt.
4.2. Productie van kaneelzuur door Claisen-condensatie
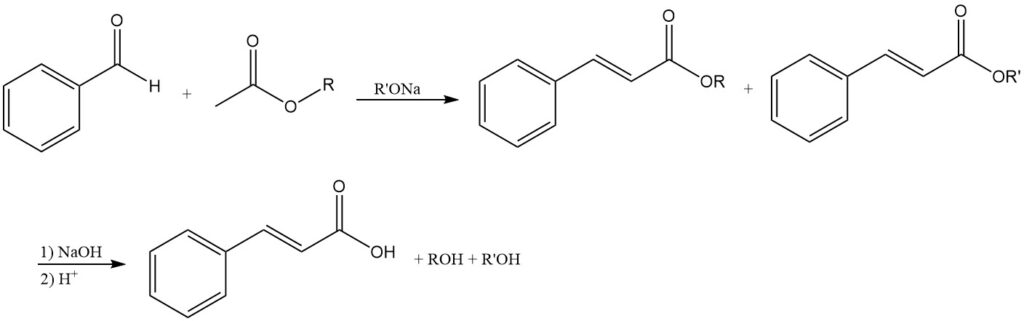
De condensatie van benzaldehyde met azijnzuuresters met behulp van alkalialcoholaten produceert kaneelzuuresters als de initiële producten, die na verzeping kaneelzuur opleveren.
4.3. Productie van kaneelzuur uit benzalchloride
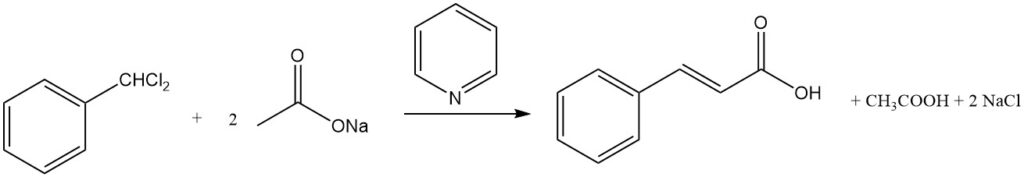
Kaneelzuur kan in hoge opbrengsten worden gesynthetiseerd door de reactie van benzalchloride en alkaliacetaat in een alkalisch medium. De aanwezigheid van aminen zoals pyridine kan de opbrengst verder verhogen tot meer dan 80%.
4.4. Productie van kaneelzuur door oxidatie van kaneelaldehyde
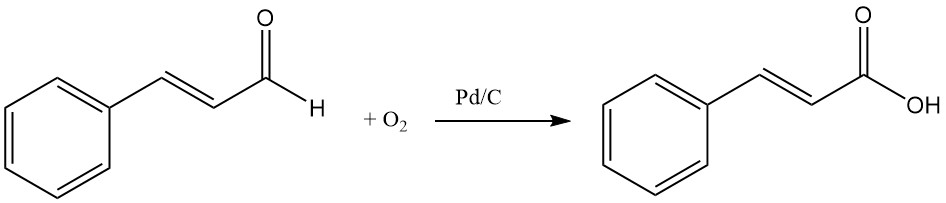
Kaneelzuur kan worden geproduceerd door de oxidatie van kaneelaldehyde met behulp van zuurstof en katalysatoren zoals zilver of palladium op houtskool.
4.5. Bereiding van kaneelzuur uit zijn esters
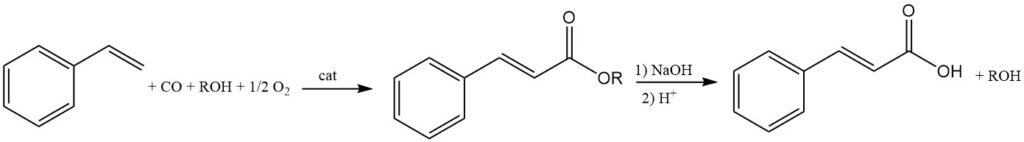
Kaneelzuuresters worden gevormd door de reactie van styreen, alcoholen, koolmonoxide en zuurstof met behulp van platina- of palladiumkatalysatoren. Het gewenste kaneelzuur kan vervolgens worden verkregen uit de hydrolyse van deze esters.
5. Toepassingen van kaneelzuur
Kaneelzuur wordt gebruikt als voorloper voor de productie van kunstmatige zoetstoffen (aspartaam) en smaakstoffen in voedingsmiddelen en dranken en heeft potentiële toepassingen in cosmetica en farmaceutica vanwege de antimicrobiële en ontstekingsremmende eigenschappen.
Kaneelzuuresters, afgeleid van kaneelzuur, worden veel gebruikt in parfums en cosmetica vanwege hun aangename aroma’s.
Kaneelzuur wordt gebruikt als tussenproduct bij de enzymatische productie van L-fenylalanine, een belangrijk onderdeel van peptidezoetstoffen (aspartaam).
Natriumcinnamaat remt effectief corrosie en vindt gebruik in verschillende toepassingen.
Kaneelzuur werkt als corrosieremmer tijdens het galvaniseren van zink (zonder cyanide) en het verwijderen van aanslag van zinkoppervlakken en in spuitbussen.
Kaneelzuur wordt gebruikt als een hittestabilisator met een lage toxiciteit voor PVC, als een vernettingsmiddel voor verschillende polymeren, waaronder polyurethanen en dimethyltereftalaat-ethyleenglycolcopolymeren, en als een brandvertrager voor polycaprolactam.
Het wordt ook gebruikt bij de productie van wasbestendige polyurethaanlijmen voor polyestervezels en voor het verbeteren van de opslagstabiliteit van drogende-olie-gemodificeerde alkydharscoatings.
6. Toxicologie van kaneelzuur
Acute toxiciteit
- Oraal (ratten): LD50 = 2,5 g/kg (relatief laag, wat duidt op matige orale toxiciteit)
- Dermaal (konijnen): LD50 > 5 g/kg (relatief hoog, wat duidt op lage dermale toxiciteit)
Huidirritatie
Puur kaneelzuur veroorzaakt lichte irritatie aan intacte of afgesleten konijnenhuid na 24 uur blootstelling.
Huidgevoeligheid
Een 4% oplossing van kaneelzuur in petrolatum veroorzaakte geen gevoeligheid bij menselijke proefpersonen.
Referentie
- Cinnamic Acid; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a07_099
