Gelatine: eigenschappen, productie en toepassingen

Gelatine is een doorschijnend, kleurloos, bros (wanneer droog), smaakloos, eetbaar, multifunctioneel eiwitpolymeer, heet water geëxtraheerd uit “collageen” verkregen uit verschillende dierlijke en visbijproducten.
De grondstoffen die worden gebruikt bij de productie van gelatine zijn afkomstig van verschillende dierlijke bronnen, zoals varkenshuiden, runderhuiden, runder- en varkensbotten (osseïne) en vishuiden.
De ouderproteïnen die aanleiding geven tot gelatine, bekend als “collageen”, behoren tot de collageenfamilie van proteïnen die ongeveer 30% van het totale eiwitgehalte van het dierlijk lichaam uitmaken.
Collageenen zijn essentiële structurele proteïnen die worden aangetroffen in verschillende bindweefsels, waaronder huiden, botten, pezen, ligamenten, hoornvliezen, kraakbeen, bloedvaten en darmen. Tijdens het productieproces van gelatine worden deze collageenproteïnen gedeeltelijk gehydrolyseerd.
De primaire materialen die worden gebruikt bij de productie van gelatine zijn dierlijke en visbijproducten, waaronder varkenshuiden, runderhuiden, runder- en varkensbotten (osseïne) en vishuiden.
Inhoudsopgave
1. Productie van gelatine
Gelatine is een commercieel verkrijgbaar eiwit dat afkomstig is van dierlijk collageen dat voorkomt in huiden en botten. De primaire bronnen van grondstoffen die worden gebruikt voor de productie van gelatine zijn runderhuiden, runder- en varkensbotten en varkenshuiden.
Om het collageen oplosbaar te maken in heet water, vereist elk ruw materiaal een specifiek voorbehandelingsproces.
Tijdens de voorbehandelingsprocedure ondergaat het collageenbevattende materiaal een reeks veranderingen, zoals opzwellen en verzachten, crosslinking en hydrolyse van de peptidebindingen van niet-collageenachtige eiwitten. Daarnaast worden verschillende onzuiverheden uit het materiaal geëxtraheerd.
Er zijn twee hoofdtypen gelatine: type A, dat wordt geproduceerd door met zuur voorbehandelde grondstoffen, en type B, dat wordt geproduceerd door alkalische verwerking.
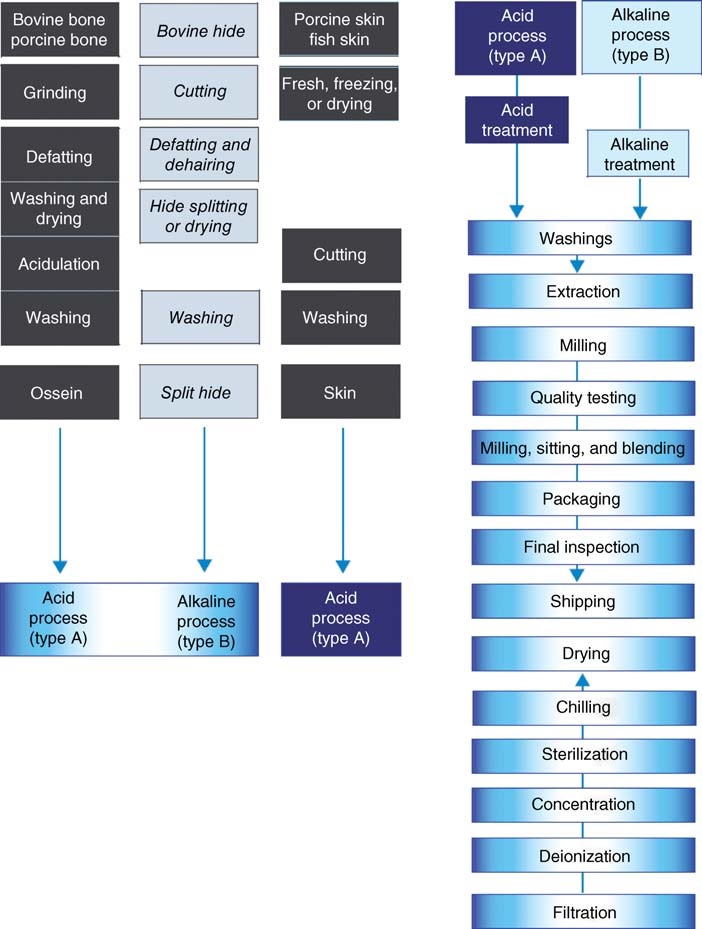
1.1. Productie van gelatine door het zuurproces
Het zuurproces wordt doorgaans gebruikt voor varkenshuid en, af en toe, voor specifieke soorten osseïne. Gewassen varkenshuiden worden behandeld met verdunde minerale zuren bij lage temperaturen gedurende ongeveer 24 uur.
Deze voorbehandeling is voldoende om zuur-labiele peptidebindingen in varkenshuidcollageen te splitsen. Na gedeeltelijke neutralisatie wordt de gelatine geëxtraheerd met heet water.
De extractie van gelatine vindt gewoonlijk stapsgewijs plaats, met opeenvolgende verhogingen in temperatuur en tijd. Gelatine uit opeenvolgende extracties vertoont verschillende fysieke en chemische eigenschappen.
Het eerste extract heeft de hoogste gelsterkte en moleculaire massa en is zeer kleurloos.
Latere extracties, verkregen bij verhoogde temperaturen, bevatten een hoger percentage peptiden met een laag moleculair gewicht, wat resulteert in een lagere gelsterkte, en zijn intenser van kleur en wazigheid.
1.2. Productie van gelatine door het Alkali-proces
Type B-gelatine wordt geproduceerd door runderhuiden, runder- en varkensosseïne voor te behandelen met alkali, zoals kalk of natriumhydroxide, bij kamertemperatuur.
Het kalkproces varieert van enkele weken tot enkele maanden en verwijdert onzuiverheden, kruisverbindingen en peptiden, voornamelijk die van niet-collageenoorsprong.
De kalktijd is een kritische factor bij verdere verwerking. Verdunde oplossingen met 3-10% gelatine worden verkregen door extractie met heet water.
De oplossingen worden gefilterd om zwevende stoffen te verwijderen, gedeïoniseerd om anorganische ionen te elimineren en vervolgens geconcentreerd tot 25-35 gew.% door ultrafiltratie en vacuümverdamping, gefilterd en gesteriliseerd.
De geconcentreerde oplossing wordt snel afgekoeld om een gel te vormen en geëxtrudeerd als noedels, die op een roestvrijstalen net worden geplaatst om te drogen met hete, schone lucht.
Het net gaat langzaam door een droogkamer met talrijke zones met gecontroleerde temperatuur en vochtigheid. Het typische temperatuurbereik varieert van ongeveer 30 °C tot 70 °C in de laatste zone.
De gedroogde gelatine, met een vochtgehalte van ongeveer 10%, wordt gebroken en gemalen.
2. Chemische eigenschappen van gelatine
Tijdens de productie van gelatine wordt het dierlijke ruwe materiaal onderworpen aan een behandeling met verdund zuur (type A-proces) of alkali (type B-proces) om de interketen-crosslinks die de thermische tolerantie van collageenfibrillen bepalen, gedeeltelijk te splitsen.
Deze afbraak resulteert in de vorming van “in heet water oplosbaar collageen”, of gelatine, dat wordt geëxtraheerd met heet water dat de collageenfibrillen smelt in hun individuele α-ketens.
Gelatine is een polydispers mengsel van eiwitfragmenten met verschillende moleculaire massa’s, variërend van 15.000 tot >400.000 Dalton.
De samenstelling ervan hangt af van het niveau van chemische/thermische hydrolyse van de α-ketens en het niveau van interketen-crosslinkhydrolyse. Behalve glutamines en asparagines komt de aminozuursamenstelling overeen met die van het post-translationeel verwerkte collageen waarvan het is afgeleid.
Zuur- en base-gekatalyseerde deamideringsreacties zetten sommige glutamines/asparagines voor een type A-verwerkte gelatine en de meeste glutamines en bijna alle asparagines voor een type B-verwerkte gelatine om in hun zure tegenhangers.
Gelatine afkomstig van varkens- of rundergrondstoffen bevat doorgaans minimaal 11% hydroxyproline, wat wordt gebruikt voor identificatie- en kwantificeringsdoeleinden.
Kwantitatieve analyse van gelatine toont ongeveer 50,5% koolstof, 25,2% zuurstof, 17,0% stikstof en 6,8% waterstof. Het asgehalte varieert afhankelijk van de oorsprong van de grondstof en de verwerkingsmethode.
Van varkenshuid afkomstige gelatine bevat kleine hoeveelheden chloriden en sulfaten van zuurbehandeling vóór extractie, terwijl van bot en huid afkomstige gelatine calcium- en natriumzouten bevat van de kalk die wordt gebruikt bij de voorbehandeling.
Droge gelatine die in luchtdichte containers bij kamertemperatuur wordt bewaard, blijft lange tijd stabiel, maar er kan afbraak optreden in oplossing als gevolg van extreme pH-waarden, temperatuur en proteolytische enzymen zoals papaïne of trypsine.
Gelatine kan chemisch worden gemodificeerd om de eigenschappen ervan te veranderen, zoals door acylatie, carbamylatie, succinylatie, ftalatie of carbamylatie. Deze gemodificeerde producten worden gebruikt voor gespecialiseerde farmaceutische en fotografische toepassingen.
Gemethacryleerde gelatine is een nieuw derivaat dat geschikt is voor technische toepassingen. Gelatine kan ook permanent worden vernet door het te laten reageren met aldehyden zoals formaldehyde, glyoxal of glutaraldehyde.
3. Toepassingen van gelatine
Gelatine, hoewel voornamelijk een voedingsmiddel, wordt niet alleen gewaardeerd om zijn nutritionele bijdrage, maar ook om zijn functionele eigenschappen. De toepassingen ervan reiken verder dan de voedingsindustrie en zijn belangrijk in de farmaceutische, cosmetische, fotografische en technische velden.
Vanwege zijn moleculaire structuur en structuur-functierelatie vertoont gelatine een reeks eigenschappen, waaronder gelvorming, waterbinding, verdikking, emulsievorming en -stabilisatie, schuimvorming en -stabilisatie, filmvorming, adhesie/cohesie, beschermende colloïdefunctie en remming van ijskristalvorming.
3.1. Voedingsindustrie
In de voedingsindustrie zijn eetbare gelatine en gelatinehydrolysaat veelgebruikte ingrediënten voor de productie van verschillende voedingsproducten.
Verschillende eigenschappen en toepassingen vereisen de productie van specifieke gelatinetypen.
Bladgelatine wordt veel gebruikt voor huishoudelijke doeleinden vanwege het gemak van meten.
Speciale instant gelatines zijn beschikbaar voor het bereiden van slagroomtaarten en desserts zonder verhitting, terwijl poedergelatine en gelatinehydrolysaat worden gebruikt bij de verwerking van zoetwaren, zuivelproducten, desserts, vleesproducten, dranken en meer.
3.2. Farmaceutische toepassingen
In de farmaceutische industrie wordt gelatine veel gebruikt voor de productie van zachte en harde capsules, als vulmiddel, voor het coaten van in water onoplosbare vitaminen, als primair bestanddeel voor chirurgische sponzen en als bindmiddel in tabletten.
Gelatine wordt ook aanbevolen als voedingssupplement voor het verminderen van gewrichtspijn, het verbeteren van de botgezondheid en het verbeteren van de schoonheid van de huid.
3.3. Cosmetica
Gelatine en zijn hydrolysaten worden veel gebruikt in huid- en haarverzorgingsproducten vanwege hun niet-toxische en niet-irriterende aard.
In huidreinigende preparaten verminderen ze de kans op irritatie veroorzaakt door anionische oppervlakteactieve stoffen.
In haarverzorgingsproducten beschermen gelatinehydrolysaten de structuur van het haar en minimaliseren ze schade aan de haarstructuur en biochemie die wordt veroorzaakt door permanenten, bleken of kleuren.
3.4. Fotografie
Gelatine is een essentieel onderdeel van fotografische materialen en vult een groot deel van foto-emulsiefilms.
De unieke eigenschappen, zoals sol-geltransformatie, interactiviteit met zilverionen, cross-linkbaarheid en waterzwelbaarheid, maken het een onmisbaar ingrediënt voor de ontwikkeling van latente beelden en kleurstofvorming tijdens de verwerking van fotografisch materiaal.
Referentie
- Gelatin; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a12_307.pub2
