Ethylbenzeen: eigenschappen, productie, toepassingen en toxicologie
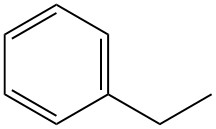
Wat is ethylbenzeen?
Ethylbenzeen, ook bekend als fenylethaan, is een enkelvoudige alkylaromatische koolwaterstof met de formule C8H10. Het is een zeer ontvlambare, kleurloze vloeistof met een karakteristieke aromatische geur.
Het wordt voornamelijk (>99%) gebruikt als tussenproduct bij de productie van styreenmonomeer, een van de belangrijkste grootschalige chemische grondstoffen ter wereld.
De commerciële productie van ethylbenzeen begon in de jaren 30 door Dow Chemical (VS) en BASF (Duitsland). De ethylbenzeen/styreenindustrie bleef relatief onbelangrijk tot de Tweede Wereldoorlog.
De stijgende vraag naar synthetisch styreen-butadieenrubber (SBR) tijdens de oorlogsjaren versnelde snelle technologische ontwikkelingen en aanzienlijke capaciteitsuitbreiding. Deze oorlogsinspanning leidde tot de bouw van talloze grootschalige fabrieken en de styreenproductie ontwikkelde zich snel tot een belangrijke industrie.
In 1999 had de wereldwijde jaarlijkse productiecapaciteit voor ethylbenzeen bijna 25 miljoen ton bereikt. Opvallend is dat de jaren 90 de grootste capaciteitsgroei lieten zien in landen in het Verre Oosten (exclusief Japan), waar de fundamentele petrochemische industrieën een substantiële ontwikkeling en uitbreiding ondergingen.
Inhoudsopgave
1. Fysieke eigenschappen van ethylbenzeen
Onder normale omstandigheden is ethylbenzeen een kleurloze vloeistof met een aromatische geur. Het is onoplosbaar in water, maar oplosbaar in alle verhoudingen in ethanol en ethylether. Ethylbenzeen is irriterend voor de huid en ogen en is matig giftig bij inname, inademing en huidabsorptie.
Enkele fysieke eigenschappen van ethylbenzeen staan in de volgende tabel.
| Eigenschap | Waarde |
|---|---|
| CAS-nummer | [100-41-4] |
| Chemische formule | C6H5CH2CH3 |
| Moleculaire massa | 106,168 g/mol |
| Dichtheid |
|
| Smeltpunt | -94,949 °C |
| Kookpunt (101,3 kPa) | 136,2 °C |
| Breukindex |
|
| Dampdichtheid | 3,66 |
| Kritische druk | 3609 kPa (36,09 bar) |
| Kritische temperatuur | 344,02 °C |
| Vlampunt (gesloten beker) | 15 °C |
| Zelfontbrandingstemperatuur | 460 °C |
| Brandbaarheidsgrens |
|
| Latente warmte |
|
| Verwarmingswaarde |
|
| Kinematische viscositeit |
|
| Oppervlaktespanning | 28,48 mN/m |
| Soortelijke warmtecapaciteit |
|
| Acentrische factor | 0,3026 |
| Kritische samendrukbaarheid | 0,263 |
2. Chemische reacties van ethylbenzeen
De belangrijkste commerciële reactie van ethylbenzeen is de dehydrogenering tot styreen. Deze reactie vindt plaats bij hoge temperaturen (600–660 °C) en gebruikt doorgaans een kalium-gepromoteerde ijzeroxidekatalysator met stoom als verdunningsmiddel.
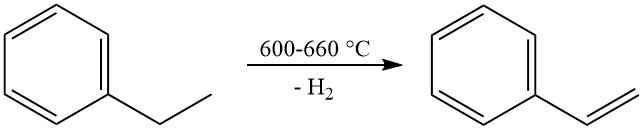
Industriële productie bereikt styreenselectiviteiten variërend van 90 tot 97 mol% met per-pass conversies van 60-70%. De primaire nevenreactie is de dealkylering van ethylbenzeen tot benzeen en tolueen.
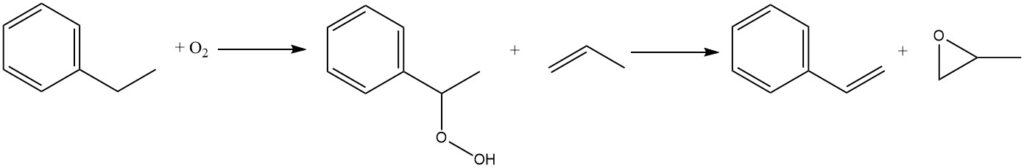
Een andere reactie die commercieel steeds belangrijker wordt, is de luchtoxidatie van ethylbenzeen tot ethylbenzeenhydroperoxide. Het is een niet-gekatalyseerd proces dat plaatsvindt in de vloeibare fase. Vanwege de inherente instabiliteit van hydroperoxiden moet blootstelling aan hoge temperaturen echter worden geminimaliseerd om de ontledingssnelheid te verminderen.
Het hydroperoxide wordt vervolgens behandeld met propyleen om styreen en propyleenoxide te coproduceren. In 1999 werd ongeveer 15% van de wereldwijde ethylbenzeenproductie gericht op de coproductie van styreenmonomeer en propyleenoxide via deze route.
Net als tolueen kan ethylbenzeen worden gedealkyleerd tot benzeen door middel van katalytische of thermische processen. Ethylbenzeen ondergaat ook verschillende andere reacties die kenmerkend zijn voor alkylaromatische verbindingen, zoals alkylering, acylering, nitrering en sulfonering.
3. Industriële productie van ethylbenzeen
Historisch gezien was de dominante methode voor de productie van ethylbenzeen gedurende meerdere decennia de Friedel-Crafts-alkylering van benzeen met ethyleen met behulp van opgeloste Lewis-zuren, voornamelijk aluminiumchloride, als katalysatoren in de vloeibare fase. Deze methode wordt nog steeds gebruikt voor ongeveer 40% van de wereldwijde productie van ethylbenzeen.
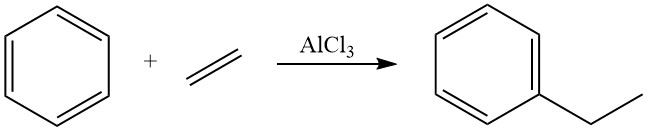
Hoewel de aluminiumchloridemethode economisch concurrerend kan zijn, genereert dit proces afvalstromen die steeds duurder worden om te verwijderen vanwege milieuvoorschriften. Bovendien is aluminiumchloride zeer corrosief, wat leidt tot aanzienlijke onderhoudsbehoeften voor apparatuur en leidingen.
Sinds het begin van de jaren 80 zijn heterogene zeolietkatalysatoren de voorkeurstechnologie geworden voor nieuwe ethylbenzeenproductie-installaties. De oorspronkelijke zeoliettechnologie werkte in de dampfase, wat een verbeterde procesefficiëntie opleverde in vergelijking met aluminiumchloride in de vloeibare fase.
Meer recent zijn er zeolietprocessen in de vloeibare fase ontwikkeld, die extra flexibiliteit bieden. Deze technologie genereert minder gevaarlijk afval in vergelijking met de aluminiumchlorideroute.
Toenemende zorgen over het milieu en vooruitgang in zeoliettechnologie hebben veel producenten die aluminiumchloride-eenheden gebruiken, gestimuleerd om hun installaties te moderniseren met zeoliettechnologie. Tussen 1997 en 1999 werd ongeveer 106 ton aan capaciteit omgebouwd van aluminiumchloride naar zeolietprocessen.
Vanaf 2000 bevonden verdere conversies zich in de engineeringfase en de bouw van nieuwe fabrieken die aluminiumchloridetechnologie gebruiken, is in het afgelopen decennium vrijwel gestopt.
Een paar fabrieken produceren een kleine hoeveelheid ethylbenzeen door superfractionering van gemengde C8-aromatische stromen.
3.1. Ethylbenzeenproductie met aluminiumchloride en andere Lewiszuurkatalyse
Gedurende meerdere decennia domineerden vloeibare aluminiumchlorideprocessen de ethylbenzeenproductie. Verschillende bedrijven, waaronder Dow, BASF, Shell en Monsanto, ontwikkelden variaties van deze technologie. Tegenwoordig gebruikt ongeveer 40% van de wereldwijde ethylbenzeenproductie nog steeds AlCl3.
De alkylering van benzeen met ethyleen is zeer exotherm, waarbij een aanzienlijke hoeveelheid warmte vrijkomt (ΔH = -114 kJ/mol). Het gebruik van aluminiumchloride als katalysator in deze reactie bevordert een snelle reactie met bijna-stoichiometrische opbrengsten van ethylbenzeen.
Andere Lewis-zuren zoals AlBr3, FeCl3, ZrCl4 en BF3 kunnen ook worden gebruikt. Processen met AlCl3 bevatten vaak promotoren zoals ethylchloride of waterstofchloride. Deze promotoren verminderen de hoeveelheid AlCl3 die nodig is voor de reactie.
Het conventionele AlCl3-proces (Figuur 1) gebruikt drie fasen in de reactor: aromatische vloeistof (benzeen), ethyleengas en een rode oliekatalysatorcomplexfase. De reactie vindt plaats nabij thermodynamisch evenwicht, waarbij één reactor nodig is voor zowel alkylering als transalkylering.
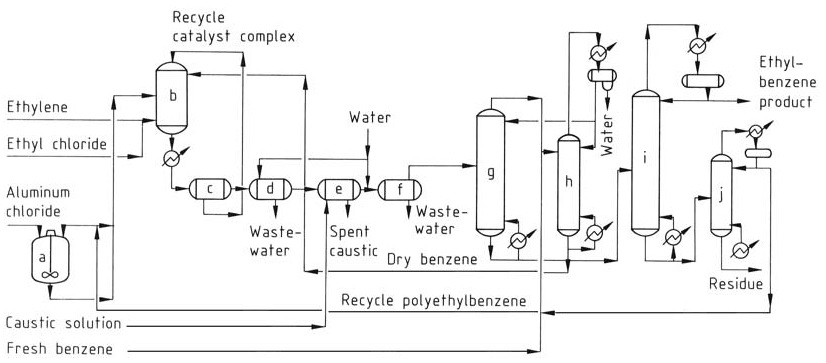
a) Katalysatormengtank; b) Alkyleringsreactor; c) Bezinktank; d) Zuurscheider; e) Bijtende scheider; f) Waterscheider; g) Benzeenterugwinningskolom; h) Benzeendehydratorkolom; i) Ethylbenzeenterugwinningskolom; j) Polyethylbenzeenkolom
Het katalysatorcomplexmengsel, droge benzeen en gerecyclede polyalkylbenzenen worden continu in de reactor gevoerd. Ethyleen en een katalysatorpromotor (bijv. ethylchloride) worden in het reactiemengsel geïnjecteerd.
De bedrijfstemperaturen zijn beperkt tot 130 °C om deactivering van de katalysator en vorming van bijproducten te voorkomen, en er wordt voldoende druk gehandhaafd om reactanten in de vloeibare fase te houden.
Het verbeterde Monsanto-proces (Figuur 2) biedt voordelen ten opzichte van conventionele AlCl3-processen en is in veel oudere fabrieken geïmplementeerd.
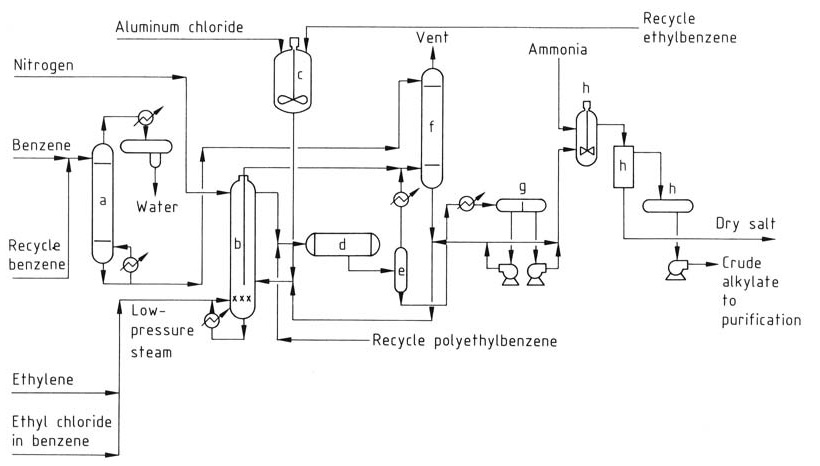
a) Benzeendroogkolom; b) Alkyleringsreactor; c) Katalysatorbereidingstank; d) Transalkylator; e) Flash-drum; f) Ontluchtingsgasreinigingssysteem; g) Decanteervat; h) Neutralisatiesysteem
Dit proces werkt bij hogere temperaturen (160–180 °C) en gebruikt een homogene vloeibare fase. De hogere temperatuur maakt het mogelijk om restwarmte terug te winnen als stoom. Er is echter een aparte transalkyleringsreactor nodig vanwege de lagere katalysatorconcentratie.
Door de temperatuur en de toevoeging van ethyleen te optimaliseren, vermindert het proces de hoeveelheid AlCl3-katalysator die nodig is aanzienlijk, waardoor afvalverwijderingsproblemen worden geminimaliseerd en omdat het werkt in een enkele, homogene vloeibare fase, elimineert het de complexe katalysatorfase die aanwezig is in traditionele methoden.
Zowel conventionele als Monsanto-processen gebruiken vergelijkbare zuiveringsstappen met meerdere destillatiekolommen om niet-omgezette benzeen-, ethylbenzeen- en polyalkylbenzeenfracties te scheiden. Organisch residu (fluxolie) wordt doorgaans gebruikt als brandstof.
Het Alkar-proces, ontwikkeld door UOP, gebruikte boortrifluoride als een Lewis-zuurkatalysator. Hoewel het voordelen biedt zoals een ethylbenzeenproduct met een hoge zuiverheid en de mogelijkheid om verdunde ethyleengrondstof te gebruiken, is het proces niet gunstig vanwege de hoge onderhoudskosten en de gevoeligheid van de katalysator voor zelfs een kleine hoeveelheid water.
3.2. Productie van ethylbenzeen door dampfase-alkylering over zeolieten
De Mobil-Badger-dampfasetechnologie, die gebruikmaakt van Mobil’s ZSM-5 synthetische zeolietkatalysator, ontstond in de jaren 70. Deze technologie is in verschillende configuraties aangeboden.
Het ontwerp van de eerste generatie, dat in 1980 op de markt werd gebracht, voerde alkylering en transalkylering uit in één reactor, vergelijkbaar met aluminiumchlorideprocessen. De nieuwste technologie van de derde generatie scheidt deze processen, wat voordelen biedt op het gebied van opbrengst, zuiverheid en kapitaalkosten.
Het dampfase-zeolietproces is met name geschikt voor verdunde ethyleenstromen, zoals die afkomstig zijn van vloeistofkatalytische kraakunits in raffinaderijen.
Tot de introductie van vloeibare-fase zeoliettechnologieën in de jaren 90 domineerde dit proces nieuwe fabrieksinstallaties vanwege het vermogen om de waterige afvalstromen te vermijden die worden gegenereerd door aluminiumchloridetechnologie.
Mobil-Badger heeft sinds 1980 31 eenheden gelicentieerd en de technologie blijft relevant voor verdunde ethyleengrondstoffen.
De vaste-bed ZSM-5-katalysator bevordert dezelfde alkyleringsreactie als andere processen. Ethyleenadsorptie op de Brønsted-zuurlocaties van de zeoliet activeert echter het ethyleenmolecuul, waardoor de binding met benzeen wordt vergemakkelijkt. Dit mechanisme leidt tot een ander bijproduct vergeleken met Friedel-Crafts-processen.
Koolstofstaal is het primaire bouwmateriaal vanwege de afwezigheid van zeer corrosieve componenten. Het ontwerp van de derde generatie is afgebeeld in Figuur 3.
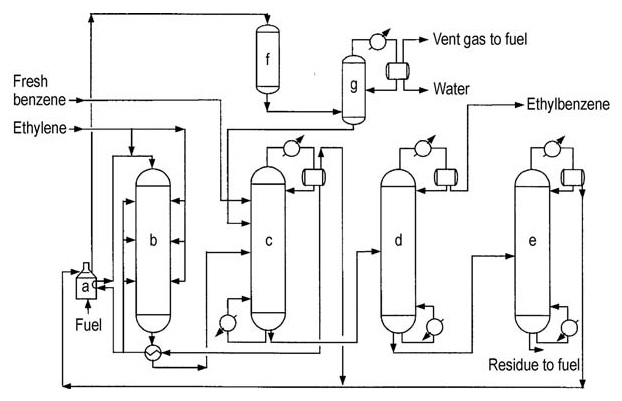
a) Reactor-voedingsverwarmer; b) Alkyleringsreactor; c) Benzeenterugwinningskolom; d) Ethylbenzeenterugwinningskolom; e) Polyethyleenbenzeenterugwinningskolom; f) Secundaire reactor; g) Stabilisator
De alkyleringsreactor werkt bij 350–450 °C en 1-3 MPa, waardoor de meeste proceswarmte als stoom kan worden teruggewonnen. De reactor gebruikt een configuratie met meerdere bedden met een gestookte verwarmer en warmteterugwinningsapparatuur.
Overtollig benzeen wordt gehandhaafd ten opzichte van ethyleen. De katalysator deactiveert geleidelijk door cokesvorming, wat periodieke in-situ regeneratie vereist (ongeveer elke 18–24 maanden), wat ongeveer 36 uur duurt.
Vergeleken met vloeibare-fase zeolieten en Lewis-zuurkatalysatoren, vertoont deze technologie een grotere tolerantie voor water, zwavel en andere potentiële vergiften.
Het verdampte reactoreffluent ondergaat zuivering. Benzeen wordt teruggewonnen via destillatie in de eerste kolom en gerecycled. De tweede kolom scheidt ethylbenzeen van de onderste stroom, die vervolgens naar een laatste kolom wordt geleid voor de scheiding van recyclebare alkylbenzeen- en polyalkylbenzeenfracties van het zware, niet-recyclebare residu.
Dit laagviskeuze residu, voornamelijk samengesteld uit difenylmethaan en difenylethaan, wordt gebruikt als brandstof. De gescheiden recyclebare hogere alkylbenzenen en polyalkylbenzenen worden naar de dampfasetransalkylator gevoerd, waar ze reageren met overtollig benzeen over een zeolietkatalysator.
De transalkylator werkt bij een lagere druk maar bij een hogere temperatuur vergeleken met de alkylator, wat de dealkylering van hogere alkylbenzenen bevordert terwijl di-ethylbenzeen wordt getransalkyleerd tot ethylbenzeen. Deze mogelijkheid tot dealkylering minimaliseert de totale residuproductie.
De eerdere processen van de eerste en tweede generatie verschilden voornamelijk in de locatie van de recycle-polyethylbenzeenstroom, wat leidde tot lagere prestaties vergeleken met het ontwerp van de derde generatie.
3.3. Ethylbenzeenproductie door vloeibare-fase-alkylering over zeolieten
Vloeibare-fase-zeoliettechnologie voor ethylbenzeenproductie ontstond begin jaren negentig. De eerste commerciële fabriek, die in Oita, Japan, opereerde, gebruikte ultrastabiele zeoliet Y of zeoliet bèta-katalysatoren, gelicentieerd door ABB Lummus Global en Unocal (later overgenomen door ABB).
Een ander proces, EBMax van Mobil-Badger, gebruikte Mobil MCM-22-katalysator. In 1999 waren er wereldwijd twaalf fabrieken operationeel.
Vergeleken met eerdere technologieën die polymeer-grade ethyleen gebruikten, vereisen vloeibare-fase zeolietprocessen minder investeringen en leveren ze een ethylbenzeenproduct van hogere kwaliteit op.
Damp-fasetechnologie wordt nu voornamelijk gelicentieerd door Mobil-Badger voor toepassingen met verdunde ethyleengrondstoffen.
Vloeistof-faseprocessen vereisen zeolieten met bredere poriën, vergeleken met ZSM-5 dat wordt gebruikt in damp-faseprocessen, om diffusiebeperkingen te overwinnen. Off-site katalysatorregeneratie wordt over het algemeen aanbevolen vanwege langere katalysatorcyclustijden, waardoor de apparatuurbehoeften ter plaatse en investeringskosten worden verminderd.
Beide grote licentiegevers (ABB Lummus en Mobil-Badger) bieden vergelijkbare processtroomschema’s (figuren 4 en 5).
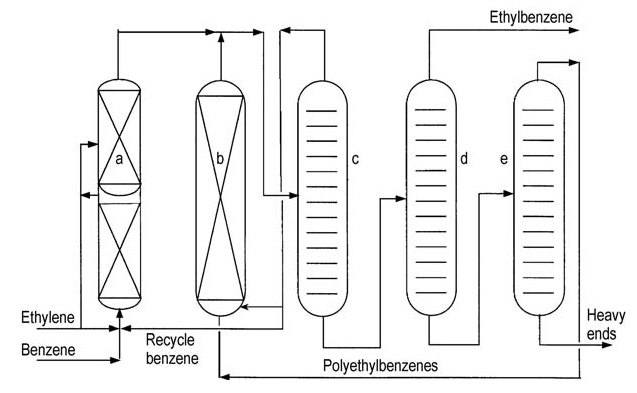
a) Alkyleringsreactor; b) Transalkyleringsreactor; c) Benzeenkolom; d) Ethylbenzeenkolom; e) Polyethylbenzeenkolom
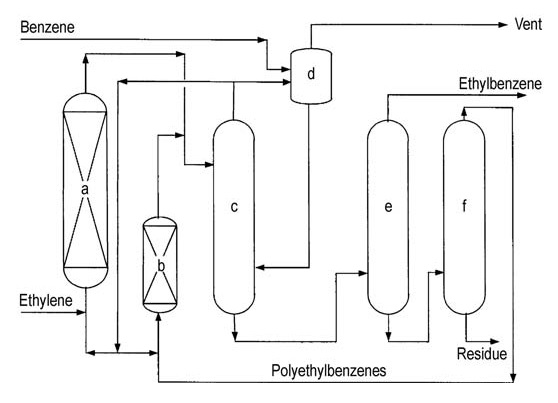
a) Alkyleringsreactor; b) Transalkyleringsreactor; c) Benzeenkolom; d) Vent-gaskolom; e) Ethylbenzeenkolom; f) Polyethylbenzeenkolom
Ethyleen wordt in een meertraps vastbedreactor gebracht die overtollig benzeen bevat. De reactortemperaturen worden onder de kritische temperatuur van benzeen (289 °C) gehouden. Hoge drukken van ongeveer 4 MPa zijn nodig om lichte gassen in oplossing te houden.
Overtollig benzeen wordt gescheiden van het reactoreffluent en teruggevoerd naar de alkyleringsfase.
Een reeks destillatiekolommen zuivert het ruwe ethylbenzeen. Benzeendestillatie verwijdert overtollig benzeen voor recycling. Ethylbenzeendestillatie scheidt het gewenste product en polyethylbenzeendestillatie wint hogere alkylbenzenen en polyethylbenzenen uit residu.
De gewonnen hogere alkylbenzenen en polyethylbenzenen worden naar een transalkyleringsreactor gevoerd voor verdere conversie. De belangrijkste onzuiverheden in het uiteindelijke ethylbenzeen kunnen niet-aromaten, tolueen en hogere alkylbenzenen omvatten, afkomstig van de toevoer- of productieprocessen.
3.4. Productie van ethylbenzeen door een gemengd-fase zeoliet-gebaseerd proces
CDTech, een samenwerking tussen ABB Lummus Global en Chemical Research and Licensing, bood een gemengd-fase zeoliet-gebaseerd ethylbenzeenproductieproces. De eerste commerciële fabriek werd in 1994 in gebruik genomen en in 1999 waren er drie van dergelijke fabrieken in gebruik.
Het innovatieve kenmerk van dit proces is de alkyleringsreactor, die een zeolietkatalysator in een reactieve destillatiekolom verwerkt.
Zowel ethyleen (gas) als benzeen (vloeistof) worden naar de reactieve destillatiekolom gevoerd. Deze mogelijkheid stelt het proces in staat om verdunde ethyleenstromen te gebruiken die worden geproduceerd tijdens stoomkrakerdestillatie. Dit proces kan ook worden aangepast voor polymeer-grade ethyleengrondstof.
De processtroom wordt weergegeven in Figuur 6.
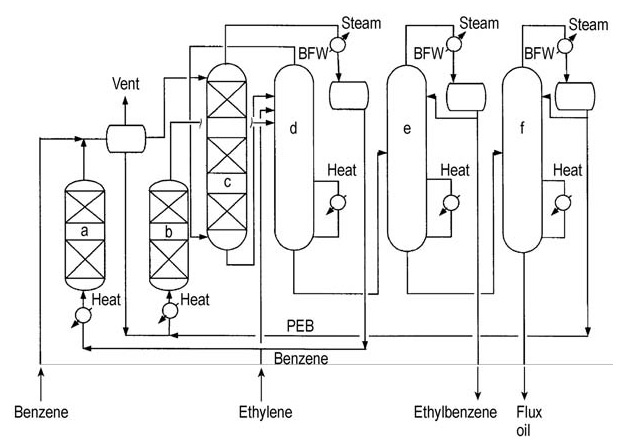
a) Afwerkingsreactor; b) Transalkylator; c) Alkylator; d) Benzeenstripper; e) Ethylbenzeenkolom; f) Polyethylbenzeenkolom. BFW = ketelvoedingswater, PEB = polyethylbenzeen
De alkylering en benzeenstripping vinden gelijktijdig plaats in dezelfde reactieve destillatiekolom. Niet-omgezet ethyleen en overtollig benzeen worden afgetapt als overheadproducten en naar een afwerkreactor geleid voor verdere verwerking.
Het ethylbenzeenproduct wordt gescheiden van de onderste stroom in de overheadproductkolom. Het resterende residu wordt verder verwerkt om transalkyleerbare polyethylbenzenen te winnen.
De geïsoleerde polyethylbenzenen worden vervolgens naar een aparte vloeistoffase-transalkyleringsreactor gestuurd, samen met overtollig benzeen. Het product uit deze transalkyleringsfase wordt teruggestuurd naar de fractioneringstrein voor verdere zuivering.
3.5. Scheiding van ethylbenzeen uit gemengde C8-stromen
Minder dan 1% van de wereldwijde ethylbenzeenproductie is afkomstig van de scheiding van gemengde C8-aromatische stromen, die doorgaans plaatsvindt naast de productie van xyleen uit reformaat. Hoewel adsorptieprocessen zoals EBEX van UOP bestaan, blijft destillatie de primaire methode voor het winnen van ethylbenzeen uit deze bron.
De moeilijkheid om ethylbenzeen uit deze stromen te scheiden, vereist een proces dat bekend staat als superfractionering. Het werd in 1957 geïntroduceerd door Cosden Oil & Chemical Company en omvat een reeks van drie destillatiekolommen, elk met meer dan 100 fasen.
In de jaren 60 werden er in de Verenigde Staten, Europa en Japan verschillende superfractioneringseenheden gebouwd. Stijgende energiekosten en hoge bouwkosten hebben deze methode echter economisch niet concurrerend gemaakt. Als gevolg hiervan is superfractionering grotendeels verlaten ten gunste van efficiëntere methoden.
4. Toepassingen van ethylbenzeen
Bijna alle commercieel geproduceerde ethylbenzeen wordt intern gebruikt in raffinaderijen of chemische fabrieken voor de productie van styreenmonomeer, wat een cruciale bouwsteen is voor de productie van polystyreen. In sommige gevallen wordt ethylbenzeen samen met propyleenoxide geproduceerd.
Minder dan 1% ethylbenzeen wordt gebruikt als verfoplosmiddel of als tussenproduct voor de synthese van di-ethylbenzeen, acetofenon en ethylantrachinon.
5. Toxicologie van ethylbenzeen
Ethylbenzeen wordt gemakkelijk opgenomen na inhalatie, orale en dermale blootstelling. Het ondergaat primair metabolisme door oxidatie van de zijketen, met kleine metabolieten van aromatische ringhydroxylatie. Minder dan 5% wordt onveranderd uitgescheiden in de urine als 2- en 4-ethylfenol.
De belangrijkste geïdentificeerde metabolieten zijn:
- 1-fenylethanol (belangrijkste urinemetaboliet bij ratten)
- Amandelzuur (belangrijkste urinemetaboliet bij mensen)
- Fenylglyoxylzuur (belangrijkste urinemetaboliet bij mensen)
- Benzoëzuur
- Fenylazijnzuur (kleine metaboliet)
Experimentele studies wijzen op een lage acute toxiciteit bij dieren. Orale LD50-waarden bij ratten variëren van 3,5 tot 4,7 g/kg lichaamsgewicht. Er is een dermale LD50-waarde van ongeveer 15 g/kg lichaamsgewicht gerapporteerd.
Inhalatieblootstelling bij ratten resulteerde in irritatie van de luchtwegen vanaf 1000 ppm. Hogere concentraties veroorzaakten wankelheid, waggelende gang en uiteindelijk bewusteloosheid en overlijden bij 5000 ppm. Menselijke vrijwilligers die 7,5 uur werden blootgesteld aan 25 ppm, meldden milde irritatie van de slijmvliezen, die bij 100 ppm duidelijker werd.
Herhaaldelijk huidcontact met onverdunde ethylbenzeen kan leiden tot erytheem, oedeem en oppervlakkige necrose. Soortgelijke effecten worden verwacht bij mensen vanwege ontvetting van de huid bij herhaalde blootstelling.
Studies die herhaalde blootstelling aan doses onderzochten, lieten zien dat significante nadelige effecten bij dieren alleen optraden bij relatief hoge doses ethylbenzeen.
Er werden geen effecten waargenomen bij ratten bij 100 ppm en muizen bij 500 ppm gedurende een inhalatiestudie van drie maanden; echter, verhoogde long-, nier- en levergewichten werden waargenomen vanaf 250 ppm bij ratten en 750 ppm bij muizen. Er werden geen histopathologische veranderingen opgemerkt.
Twee jaar durende inhalatiestudies lieten geen effecten zien bij ratten en muizen bij 75 ppm. Lichte veranderingen werden waargenomen bij 250 ppm, met verhoogde lever- en longtumoren bij muizen en niertumoren bij mannelijke ratten bij 750 ppm (beschouwd als rat-specifiek en niet relevant voor mensen).
Wat betreft de reproductietoxiciteit van ethylbenzeen zijn er tegenstrijdige resultaten gerapporteerd in verschillende onderzoeken. Sommige onderzoeken suggereren potentiële foetotoxiciteit bij hoge blootstellingsniveaus bij drachtige muizen en ratten, maar er werden geen duidelijke effecten waargenomen bij konijnen bij 1000 ppm met een dagelijkse blootstelling van 7 uur.
Het algehele resultaat van verschillende onderzoeken suggereert dat ethylbenzeen geen mutageen gevaar vormt. Beperkte in-vitrogegevens die beschikbaar zijn voor de meeste metabolieten suggereren ook geen duidelijk genotoxisch potentieel.
Een inhalatieonderzoek van twee jaar toonde een verhoogde tumorincidentie bij mannelijke ratten (nier), mannelijke muizen (long) en vrouwelijke muizen (lever) bij het hoogste blootstellingsniveau (750 ppm). In een oraal onderzoek met ratten en muizen die werden blootgesteld aan xyleenmengsels met 17% ethylbenzeen, werden geen blootstellingsgerelateerde tumoren waargenomen.
Ethylbenzeen is niet genotoxisch in vivo, wat duidt op een niet-genotoxische werkingswijze voor de waargenomen tumoren in de studie met hoge dosis inhalatie. Verhoogde tumorvorming kan verband houden met door ethylbenzeen geïnduceerde celproliferatie in de nieren (ratten) en longen/lever (muizen).
Verder onderzoek is nodig om de relevantie ervan voor mensen te bepalen en een veilige grenswaarde voor beroepsmatige blootstelling vast te stellen.
IARC classificeert ethylbenzeen als “mogelijk kankerverwekkend voor mensen” (Groep 2B) vanwege voldoende bewijs bij dieren en onvoldoende bewijs bij mensen.
De Duitse MAK-commissie classificeert ethylbenzeen als een categorie 3A-carcinogeen vanwege gegevens over carcinogeniciteit. Ze wachten op verdere mechanistische gegevens voordat ze een grenswaarde voor beroepsmatige blootstelling vaststellen.
ACGIH classificeert ethylbenzeen als een A3-carcinogeen (“bevestigd dierlijk carcinogeen met onbekende relevantie voor mensen”) en beveelt een TLV-TWA van 100 ppm en een TLV-STEL van 125 ppm aan. Ze definiëren ook een biologische blootstellingsindex (BEI) voor amandelzuur in urine van 1,5 g/g creatinine.
In de EU wordt ethylbenzeen geclassificeerd als “zeer ontvlambaar” (F) en “schadelijk bij inademing” (Xn).
Referentie
- Ethylbenzene; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a10_035.pub2
