Appelzuur: eigenschappen, productie en toepassingen
Wat is appelzuur?
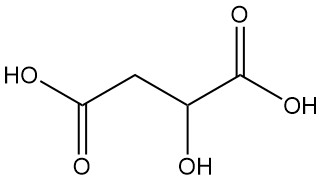
Appelzuur, ook bekend als hydroxysuccinezuur of hydroxybutaandizuur, is een dicarbonzuur met de chemische formule C4H6O5. Het is een natuurlijk voorkomende organische verbinding die wordt gekenmerkt door een zure smaak.
Het werd voor het eerst beschreven door Sheele die in 1785 dit zuur isoleerde uit onrijpe appels.
Appelzuur is een bestanddeel van verschillende soorten fruit, met name appels. In biologische systemen dient appelzuur, in zijn geïoniseerde vorm, malaat, als een tussenproduct in de tricarbonzuurcyclus. Dit metabolische pad is cruciaal voor de energieproductie.
De L-isomeer van appelzuur is de overheersende vorm die in de natuur wordt aangetroffen en bezit biologische activiteit. Hoewel het voornamelijk bekend staat om zijn rol in het op smaak brengen van voedsel, suggereert nieuw bewijsmateriaal mogelijke voordelen voor de menselijke gezondheid.
Appelzuur is betrokken bij energiemetabolisme, met name bij hypoxie. Studies tonen aan dat het de fysieke prestaties kan verbeteren en symptomen kan verlichten die geassocieerd worden met fibromyalgie.
Appelzuurmetabolisme wordt beïnvloed door enzymen zoals appelzuurenzym. Dit enzym katalyseert de oxidatieve decarboxylering van malaat tot pyruvaat. Het gegenereerde pyruvaat kan verdere metabolische transformaties ondergaan, waaronder omzetting in glucose of oxaloacetaat.
Appelzuur vertoont antimicrobiële eigenschappen. De zure aard ervan draagt bij aan het conserveren van voedsel door microbiële groei te remmen. De effectiviteit ervan wordt echter beïnvloed door factoren zoals pH en specifieke microbiële soorten.
Inhoudsopgave
| Eigenschap | Waarde |
|---|---|
| CAS-nummer | [617-48-1] |
| Chemische formule | C4H6O5 |
| Moleculaire massa | 134,09 g/mol |
| Smeltpunt | 131 °C |
| Dichtheid | 1,60 g/cm3 |
| Viscositeit van 50% waterige oplossing bij 25 °C | 6,5 mPa.s |
| Verbrandingswarmte bij 20 °C | -1,340 MJ/mol |
| pKa1 bij 20 °C | 3,51 |
| pKa2 bij 20 °C | 5,03 |
| Eigenschap | Waarde |
|---|---|
| CAS-nummer | [97-67-6] |
| Smeltpunt | 100 °C |
| Dichtheid bij 20 °C | 1,595 g/cm3 |
| Specifieke rotatie bij 18 °C (7 gew.% in H2O) | -2,3° |
| Oplosbaarheid in water bij 20 °C | 36,4 g/100 g |
2. Chemische reacties van appelzuur
Door de aanwezigheid van carbonzuur en hydroxylfunctionele groepen in appelzuur, kan het een verscheidenheid aan chemische reacties ondergaan.
Als carbonzuur reageert appelzuur met basen om zouten te vormen, zoals natriummalaat of kaliummalaat.
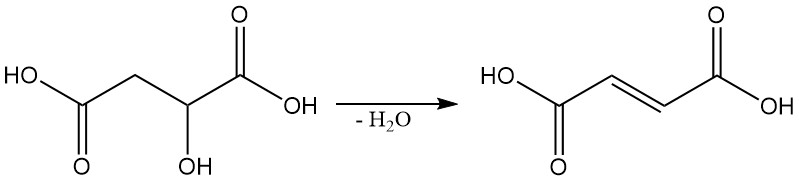
Onder specifieke omstandigheden kan appelzuur worden gedehydrateerd om fumaarzuur te produceren.
De decarboxylatie van appelzuur levert pyrodruivenzuur op.
Appelzuur kan reageren met alcoholen om esters te vormen, die vaak worden gebruikt als smaakstoffen.
Appelzuur kan worden geoxideerd om verschillende producten te produceren, zoals oxaalazijnzuur, oxaalzuur en koolstofdioxide, afhankelijk van de omstandigheden.
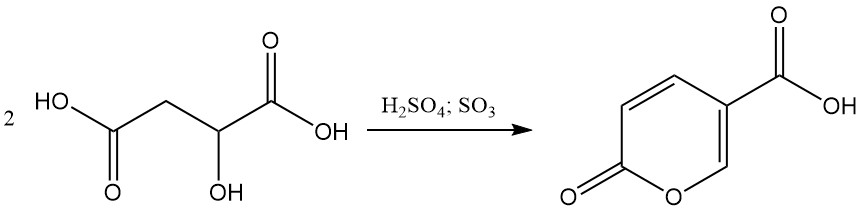
In aanwezigheid van 20%–30% rokend zwavelzuur ondergaat appelzuur zelfcondensatie om coumalinezuur te vormen.
Appelzuur kan complexen vormen met metaalionen zoals calcium en magnesium.
Malolactische fermentatie is een veelvoorkomend proces bij het maken van wijn waarbij appelzuur door bacteriën wordt omgezet in melkzuur. Het is ook een tussenproduct in de Krebs-cyclus, waarin het wordt geoxideerd tot oxaalazijnzuur.
3. Productie van appelzuur
3.1. Chemische productie van appelzuur
De synthese van appelzuur is voornamelijk gebaseerd op chemische processen, waarbij racemisch D,L-appelzuur ontstaat. De voorloper, maleïnezuuranhydride, is afkomstig van fossiele koolwaterstoffen, voornamelijk n-butaan. Benzeen, een voormalige grondstof, wordt nog steeds gebruikt, met name in Aziatische landen.
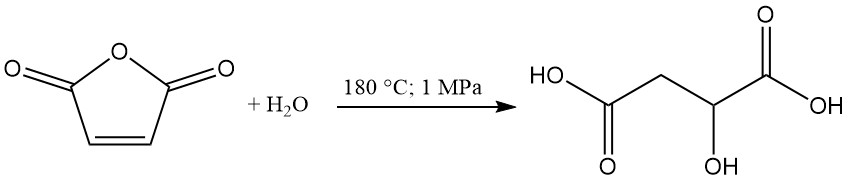
(R,S)-Appelzuur wordt industrieel geproduceerd in de Verenigde Staten en Canada door maleïnezuuranhydride hydratatie. Alberta Gas is de enige Amerikaanse fabrikant met een productiecapaciteit van ongeveer 5000 metrische ton per jaar.
In dit proces wordt maleïnezuuranhydride verhit tot 180 °C onder 1 MPa druk om appelzuur te vormen als het primaire product. Maleïnezuur en fumaarzuur worden gegenereerd als bijproducten. Fumaarzuur is, vanwege de lage oplosbaarheid in water, scheidbaar door filtratie en gerecycled.
Vervolgens geeft concentratie van het filtraat appelzuur. Het ruwe zuur wordt gezuiverd door herhaaldelijk wassen, verdampen en herkristalliseren om fumaarzuur- en maleïnezuurverontreinigingen te reduceren tot respectievelijk 7,5 en <500 ppm.
Om farmaceutische kwaliteit appelzuur te verkrijgen, zijn extra zuiveringsstappen nodig.
3.2. Enzymatische L-appelzuurproductie
Enantiomeerzuiver L-appelzuur, dat de voorkeur heeft voor farmaceutica en polymeren, is lastig te verkrijgen via racemische D,L-appelzuurresolutie. Enzymatische synthese biedt een selectief en milder alternatief.
Fumarase-gekatalyseerde hydratatie van fumaarzuur tot L-appelzuur is het belangrijkste enzymatische proces. Dit kan worden bereikt met behulp van gezuiverde enzymen, gepermeabiliseerde of gevriesdroogde cellen of hele cellen.
Micro-organismen zoals Saccharomyces cerevisiae, Brevibacterium flavus, Brevibacterium ammoniagenes en Rhizopus oryzae vertonen hoge conversiepercentages tussen 80% en ≈100% in hele-celkatalyse. Immobilisatie maakt het proces economischer doordat de katalysator herbruikbaar is.
3.3. Biosynthese van appelzuur door micro-organismen
Microbiële appelzuurproductie biedt voordelen ten opzichte van chemische synthese, waaronder exclusieve L-appelzuurvorming en het gebruik van diverse, hernieuwbare substraten.
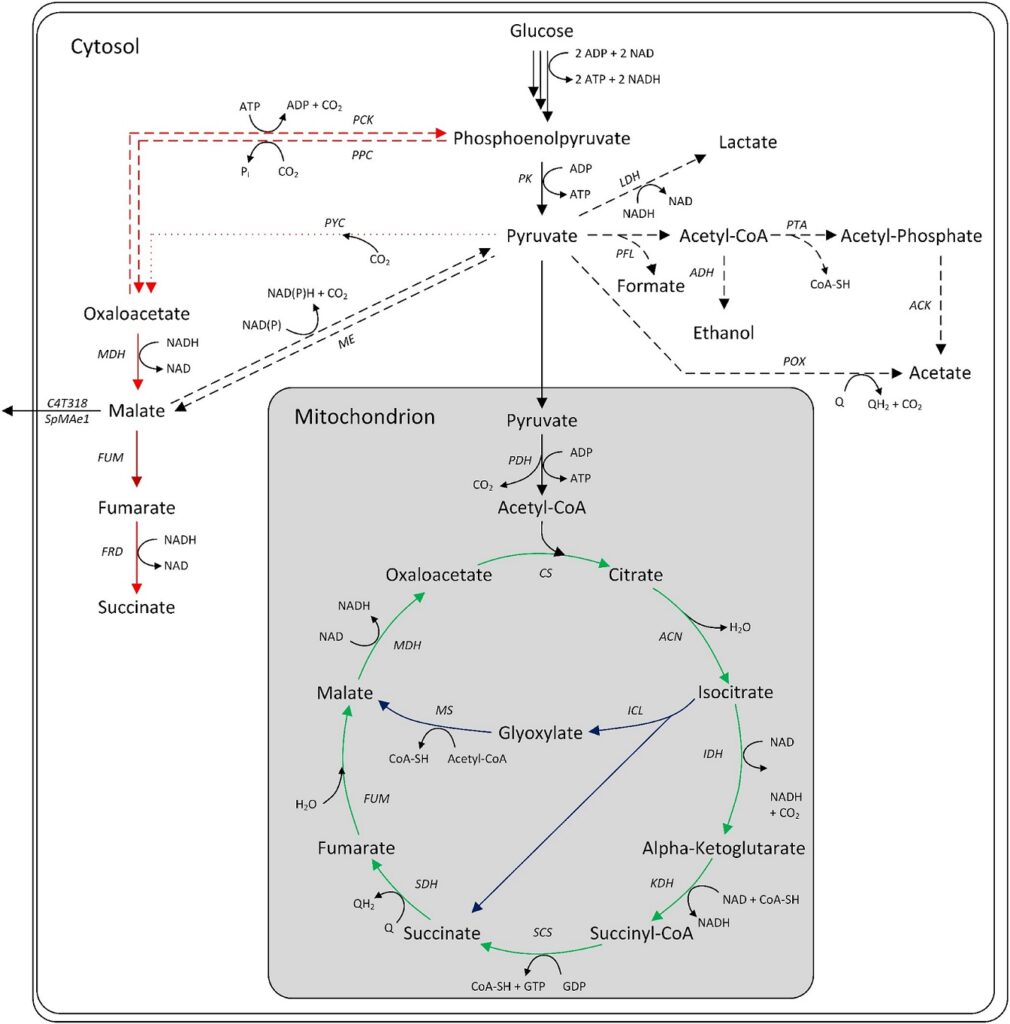
Er bestaan drie primaire intracellulaire routes voor de productie van microbiële appelzuur: oxidatieve tricarbonzuur (TCA) cyclus, reductieve TCA (rTCA) cyclus en glyoxylaatcyclus. De oxidatieve TCA, gelegen in de mitochondriën, zet acetyl-CoA om in citraat, dat vervolgens wordt geoxideerd tot L-malaat met verlies van koolstofdioxide.
De maximale theoretische opbrengst is 1 mol/mol. Sommige Aspergillus-soorten bezitten cytosolaire TCA-isovormen, wat een reductieve TCA-route mogelijk maakt. Deze ATP-neutrale route carboxyleert pyruvaat tot oxaloacetaat, dat wordt omgezet in L-malaat door malaatdehydrogenase. Een theoretische opbrengst van 2 mol/mol glucose is mogelijk.
De glyoxylaatcyclus zet citraat om in succinaat en glyoxylaat, met daaropvolgende condensatie tot L-malaat. De maximale opbrengst is 1 mol/mol, wat kan toenemen tot 1,33 mol/mol als het verbruikte oxaloacetaat wordt aangevuld door de carboxylering van pyruvaat.
Micro-organismen die worden gebruikt bij de productie van L-appelzuur omvatten natuurlijke micro-organismen (zoals Aspergillus flavus, Aspergillus oryzae, Ustilago trichophora en Rhizopus delemar) en genetisch gemodificeerde schimmels en bacteriën.
4. Toepassingen van appelzuur
(R,S)-Appelzuur deelt fysicochemische eigenschappen met citroenzuur en wijnsteenzuur, maar heeft een milder smaakprofiel. Deze eigenschap bevordert de toepassing ervan in voedingsproducten waar de zuurtegraad van citroenzuur ongewenst is. Voorbeelden hiervan zijn voedselverpakkingen en bakken.
In de voedingsindustrie wordt appelzuur veel gebruikt (ongeveer 85–90%) als zuurteregelaar en zuurteregelaar. De smaak verschilt van die van citroenzuur en biedt een minder intense maar langer aanhoudende zuurheid. Deze eigenschap helpt bij het maskeren van de nasmaak van kunstmatige zoetstof en het creëren van evenwichtige smaakprofielen in dranken.
Synergetische interacties tussen appelzuur en zoetstoffen maken een vermindering van zoetstof tot 20% en potentiële kostenbesparingen mogelijk. Het gebruik van watervrij appelzuurpoeder biedt extra economische voordelen.
Primaire toepassingen zijn onder meer zoetwaren, jam, gelei en ingeblikt fruit en groenten. De regelgeving voor levensmiddelenadditieven in de meeste landen staat het gebruik ervan toe.
Enantiomere appelzuren, (R)-(+)-appelzuur en (S)-(-)-appelzuur, kunnen worden verkregen uit (R,S)-appelzuurresolutie of door microbiële fermentatie van fumaarzuur.
Buiten de voedingsindustrie wordt appelzuur gebruikt als buffer en chelerend middel in persoonlijke verzorgings- en schoonmaakproducten. Farmaceutische toepassingen omvatten het gebruik als een medicijncomponent, terwijl de productie van halfgeleiders het gebruikt in polijst- en reinigingsprocessen.
Daarnaast wordt appelzuur gebruikt in diervoeder en als een component in mengsels met lage overgangstemperaturen.
Appelzuur is een dicarbonzuur, wat het gebruik ervan als een polymeerbouwsteen mogelijk maakt. Copolymeren en homopolymeren van appelzuur vertonen eigenschappen zoals hydrofiliteit, biocompatibiliteit en biologische afbreekbaarheid, en vinden potentiële toepassingen in vakgebieden zoals medicijnafgifte en materiaalkunde.
De belangrijkste fabrikanten van appelzuur zijn Bartek (Canada), de Japanse bedrijven Fuso Chemical en Mitsubishi Corporation Life Sciences, Isegen (Zuid-Afrika), Polynt (Italië), Thirumalai Chemicals (India), de Chinese bedrijven Changmao Biochemical Engineering Company, Anhui Sealong Biotechnology en Jinhu Lile Biotechnology Industry, evenals Tate & Lyle (VK) en Yongsan Chemicals (Korea).
5. Toxicologie van appelzuur
Appelzuur vertoont een lage acute toxiciteit in dierproeven. Orale LD50-waarden variëren van 1,6 tot 5 g/kg tussen soorten. Intraveneuze en intraperitoneale LD50-waarden zijn aanzienlijk lager.
Chronische orale studies bij ratten en honden lieten minimale bijwerkingen zien, voornamelijk kleine veranderingen in lichaamsgewicht en voerconsumptie. Onderzoeken naar reproductietoxiciteit leverden negatieve resultaten op.
Dermatologische onderzoeken wijzen op matige huidirritatie bij konijnen en ernstige oogirritatie bij konijnen. Appelzuur is een sterke irriterende stof voor de huid van cavia’s.
Mutageniciteitsbeoordelingen leverden inconsistente resultaten op. Appelzuur zelf was niet-mutageen in verschillende testen, maar de pyrolysaten en gechloreerde derivaten vertoonden mutagene eigenschappen.
Onderzoeken naar huidirritatie meldden dosisafhankelijke effecten, waarbij een hogere pH correleerde met toegenomen irritatie. Voorspellende testen bij patiënten met atopische dermatitis gaven aan dat de huid mogelijk reactief was op diëten met veel appelzuur. Appelzuur had ook invloed op de snelheid van celvernieuwing, afhankelijk van de pH-waarden.
Klinische werkzaamheids- en veiligheidsonderzoeken meldden geen toxiciteit.
Chronische toxiciteitsonderzoeken naar appelzuur bij ratten en honden stelden No Observed Effect Levels (NOEL) vast van respectievelijk 5000 ppm en 50000 ppm.
Gegevens over chronische toxiciteit van fumaarzuur bij ratten duiden op een No Observed Adverse Effect Level (NOAEL) van ongeveer 600 mg/kg lichaamsgewicht/dag. Gezien de metabolische omzetting van fumaarzuur in appelzuur binnen de Krebs-cyclus, wordt extrapolatie tussen soorten als geldig beschouwd.
De beoordeling van de blootstelling aan appelzuur van de voedingsconcentratie tot mg/kg/dag leverde onzekere resultaten op. Geschatte bereiken varieerden tussen 2–200 mg/kg/dag en 25–2500 mg/kg/dag. Door EFSA-conversiefactoren toe te passen, werd deze onzekerheid aangepakt, wat resulteerde in een NOAEL van 260 mg/kg/dag.
Referenties
- Hydroxycarboxylic Acids, Aliphatic; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a13_507
- https://scijournals.onlinelibrary.wiley.com/doi/10.1002/jctb.6269
- https://pubmed.ncbi.nlm.nih.gov/11358110/
- https://onlinelibrary.wiley.com/doi/10.1002/0471743984.vse9535
- https://onlinelibrary.wiley.com/doi/10.1002/9780470995327.ch157
- https://echa.europa.eu/registration-dossier/-/registered-dossier/11511/7/6/1
- https://www.orgsyn.org/demo.aspx?prep=cv4p0201
