Processo di produzione dell’acetaldeide
Come viene prodotta l’acetaldeide?
L’acetaldeide viene prodotta dalle seguenti materie prime: etanolo ottenuto tramite la fermentazione di carboidrati o l’idratazione di etilene, acetilene, etilene, idrocarburi inferiori, monossido di carbonio e idrogeno e metanolo.
La redditività economica dei processi commerciali dipende dalla disponibilità e dai prezzi delle materie prime. Nelle nazioni altamente industrializzate, dove mantenere prezzi elevati per l’etanolo tramite misure fiscali era difficile o dove l’etanolo petrolchimico non era disponibile (come nel caso di Germania o Giappone prima del 1939), l’acetilene è diventato il materiale di partenza preferito per l’acetaldeide.
Il processo dell’acetilene continua a essere utilizzato in alcuni paesi dell’Europa orientale e da aziende che hanno accesso ad acetilene poco costoso. Tuttavia, in altri paesi, l’etanolo prodotto petrolchimicamente è diventato la materia prima preferita, mentre l’etanolo derivato dalla fermentazione era ed è ancora utilizzato in misura minore nei paesi con un’industria chimica meno significativa.
Nei paesi occidentali, tra cui il Giappone, questi processi sono stati ampiamente sostituiti dal processo di ossidazione diretta sviluppato alla fine degli anni ’50 da Wacker-Chemie e Hoechst. Questo cambiamento è avvenuto perché l’etilene è disponibile a un costo inferiore rispetto all’acetilene.
Anche i processi a due stadi che impiegano etanolo derivato dall’etilene come materiale di partenza non sono più competitivi a causa della diminuzione di importanza dell’acetaldeide come intermedio organico.
In generale, i processi basati su acetilene, etilene ed etanolo hanno una selettività maggiore rispetto all’ossidazione di idrocarburi saturi. Questo perché, in quest’ultimo caso, si formano prodotti di ossidazione aggiuntivi insieme all’acetaldeide.
Tuttavia, questi processi sono economicamente sostenibili solo in operazioni su larga scala in cui vengono utilizzati tutti i prodotti primari e secondari ottenuti durante il processo, poiché la separazione della miscela di prodotti può essere costosa.
Sommario
1. Produzione di acetaldeide dall’etanolo
Per produrre acetaldeide, ci sono due metodi che coinvolgono l’etanolo: la deidrogenazione e l’ossidazione in presenza di ossigeno. Tra il 1918 e il 1939, la deidrogenazione era favorita a causa della produzione simultanea di idrogeno. Tuttavia, in seguito, l’ossidazione catalitica in fase di vapore dell’etanolo divenne il processo preferito, probabilmente a causa della durata prolungata del catalizzatore e del potenziale di recupero energetico.
1.1. Deidrogenazione dell’etanolo
Gli studi iniziali sulla deidrogenazione dell’etanolo, documentati nel 1886, prevedevano il passaggio dell’etanolo attraverso tubi di vetro a 260 °C.
CH3CH2OH → CH3CHO + H2 ΔH = +82.5 kJ/mol
Rese migliori si ottengono con catalizzatori come platino, rame o ossidi di zinco, nichel o cobalto. Brevetti successivi menzionano catalizzatori di zinco e cromo, ossidi di terre rare e miscele di rame e ossidi di cromo. I catalizzatori di rame producono la quantità minima di prodotti di decomposizione, ma è necessaria una frequente rigenerazione del catalizzatore.
1.1.1. Descrizione del processo
Il vapore di etanolo viene diretto attraverso un reattore tubolare contenente un catalizzatore composto da spugna di rame o rame attivato con ossido di cromo a temperature di 260-290 °C. Ogni ciclo determina un tasso di conversione del 25-50%.
Acetaldeide ed etanolo vengono separati dai gas di scarico, composti principalmente da idrogeno, tramite lavaggio con alcol e acqua. L’acetaldeide pura viene ottenuta tramite distillazione, mentre l’etanolo viene separato dall’acqua e dai prodotti a punto di ebollizione più elevato tramite distillazione e riportato al reattore.
La resa finale di acetaldeide è di circa il 90%. I sottoprodotti includono acido butirrico, crotonaldeide e acetato di etile.
1.2. Ossidazione dell’etanolo
L’ossidazione dell’etanolo è il metodo di laboratorio più antico ed efficace per sintetizzare l’acetaldeide. Nel processo commerciale, l’etanolo viene ossidato cataliticamente con ossigeno (o aria) nella fase di vapore.
CH3CH2OH + 0.5 O2 → CH3CHO + H2O ΔH = -242 kJ/mol
Rame, argento e i loro ossidi o leghe sono catalizzatori comunemente usati.
1.3. Processo Veba-Chemie
Nel processo Veba-Chemie, l’etanolo viene combinato con aria e fatto passare su un catalizzatore d’argento a temperature comprese tra 500 e 650 °C. La temperatura specifica dipende dal rapporto alcol/aria e dalla portata del gas attraverso il catalizzatore.
La conversione dell’alcol varia dal 50% al 70%, mentre la resa varia tra il 97% e il 99%, a seconda delle condizioni di reazione. L’acetaldeide e l’alcol non convertito vengono separati dal gas di scarico tramite lavaggio con alcol a freddo e distillazione frazionata.
Dopo la concentrazione, l’alcol ritorna al reattore. Il calore generato durante la reazione viene utilizzato per la produzione di vapore utilizzando un sistema di recupero del calore di scarto subito dopo la zona di reazione.
Il gas di scarico è costituito principalmente da azoto, idrogeno, metano, monossido di carbonio e anidride carbonica e viene bruciato come gas povero a basso potere calorifico nei generatori di vapore. Piccole quantità di acido acetico vengono prodotte come sottoprodotto.
2. Produzione di acetaldeide dall’acetilene
L’uso di composti di mercurio funge da catalizzatore primario per il processo di aggiunta di acqua industriale (idratazione) nella produzione di acetilene.
Per ottenere un’implementazione industriale di successo di questo metodo, è importante eliminare i prodotti di polimerizzazione e condensazione dell’acetaldeide formati in un ambiente acido.
Nel 1912, il Consortium für elektrochemische Industrie propose un processo che utilizzava l’acetilene in eccesso a una temperatura elevata. Comportava l’immediata rimozione del prodotto di acetaldeide dal liquido di reazione.
Contemporaneamente, il calore generato durante la reazione è stato dissipato distillando una quantità appropriata di acqua. Reazioni secondarie, come l’ossidazione dell’acetaldeide per formare acido acetico e anidride carbonica, hanno portato alla riduzione di Hg2+ a mercurio metallico. La produzione di acetaldeide dall’acetilene è stata ora interrotta nei paesi occidentali.
2.1. Processo di ossidazione a umido (Hoechst)
Il processo di ossidazione a umido ha offerto una soluzione per evitare la manipolazione diretta di composti tossici del mercurio. È stato impiegato da Wacker-Chemie, tra gli altri, fino al passaggio all’etilene come materiale di partenza nel 1962.
In questo metodo, è stato aggiunto solfato di ferro (III) per riossidare il mercurio metallico al sale di mercurio (II), garantendo concentrazioni adeguate del catalizzatore attivo. L’acetilene ha reagito con la soluzione acquosa del catalizzatore a 90-95 °C.
Circa il 30-50% dell’acetilene iniettato ha subito una reazione in ogni ciclo. Il gas che usciva dal reattore è stato raffreddato, portando alla separazione principalmente di acqua e tracce di mercurio, che sono state poi restituite al reattore.
L’acetaldeide e l’acqua sono state condensate in ulteriori refrigeratori e l’acetaldeide è stata infine lavata via con acqua dal gas del ciclo raffreddato. Questo processo ha prodotto una soluzione acquosa di acetaldeide all’8-10%.
L’azoto è stato introdotto con il gas di alimentazione, mentre l’anidride carbonica è stata prodotta come sottoprodotto. Per evitare un accumulo eccessivo, questi gas sono stati rimossi prelevando un piccolo flusso del gas del ciclo.
Il solfato di ferro (II) è stato formato durante la reazione e ossidato in un reattore separato con acido nitrico al 30% a 95 °C. L’acetaldeide pura è stata ottenuta tramite distillazione frazionata della soluzione acquosa a circa 200 kPa.
2.2. Processo Chisso
Il processo Chisso impiegava una soluzione di acido solforico/solfato di mercurio come catalizzatore. L’acetilene reagiva completamente con la soluzione catalizzatrice a 68-78 °C e una pressione relativa di 140 kPa.
Una combinazione di fasi di processo a pressione e sotto vuoto, condotte a basse temperature e senza acetilene in eccesso, consentiva l’isolamento e la distillazione dell’acetaldeide pura, utilizzando il calore generato durante la reazione.
Similmente al processo Hoechst, il catalizzatore poteva essere rigenerato con acido nitrico. Tuttavia, la produzione di acetaldeide utilizzando questo metodo è stata interrotta presso la Chisso Corp. oltre un decennio fa.
2.3. Produzione tramite etere vinilico
REPPE presso BASF ha introdotto un metodo che utilizza etere vinilico, evitando completamente l’uso di composti tossici di mercurio. Il metanolo è stato aggiunto all’acetilene a 150-160 °C e 1600 kPa in presenza di idrossido di potassio, con conseguente formazione di metilviniletere. Il metilviniletere è stato quindi idrolizzato con acido diluito.
2.4. Produzione tramite diacetato di etilidene
L’aggiunta di acido acetico all’acetilene in presenza di sali di mercurio(II) ha prodotto diacetato di etilidene (CH3CH(OCOCH3)2). Questo composto si decomponeva in acetaldeide e anidride acetica a 130-145 °C con l’ausilio di catalizzatori acidi come ZnCl2.
Sebbene questo processo fosse stato inizialmente sviluppato dalla Societe Chimique des Usines du Rhone su scala industriale nel 1914, negli ultimi tempi ha perso importanza.
3. Produzione da etilene
L’etilene è diventato la materia prima principale per la produzione di acetaldeide, con il processo Wacker come metodo dominante per l’ossidazione diretta dell’etilene.
3.1. Ossidazione diretta dell’etilene
Il processo Wacker, sviluppato da Wacker-Chemie e Hoechst tra il 1957 e il 1959, prevede la seguente reazione:
CH4 + 0,5 O2 → CH3CHO ΔH= -244 kJ/mol
Viene utilizzata una soluzione di catalizzatore contenente PdCl2 e CuCl2. Si è scoperto che la reazione tra etilene e cloruro di palladio acquoso produce acetaldeide quasi quantitativamente:
C2H4 + PdCl2 + H2O → CH3CHO + Pd + 2 HCl
Nel processo Wacker-Hoechst, il palladio metallico viene riossidato da CuCl2, che viene poi rigenerato con ossigeno:
Pd + 2 CuCl2 → PdCl2 + 2 CuCl
2 CuCl + 0,5 O2 + 2 HCl → 2 CuCl2 + H2O
Pertanto, è necessaria solo una piccola quantità di PdCl2 per la conversione dell’etilene e la fase che determina la velocità è la reazione dell’etilene con il cloruro di palladio.
Il processo può essere eseguito in una o due fasi. Nel metodo a una fase, una miscela di etilene e ossigeno reagisce con la soluzione del catalizzatore. Viene stabilito uno stato stazionario in cui la formazione di acetaldeide e la riduzione di CuCl2 avvengono alla stessa velocità. Il grado di ossidazione del catalizzatore, espresso come rapporto di CCu2+/(CCu2++CCu+), determina questo stato stazionario.
Nel processo a due fasi, etilene e ossigeno reagiscono separatamente in reattori diversi e la soluzione del catalizzatore viene alternativamente ridotta e ossidata. In genere, per l’ossidazione del catalizzatore viene utilizzata aria al posto dell’ossigeno puro.
3.1.1. Processo in una fase
Nel processo in una fase, etilene e ossigeno vengono introdotti in una torre di reazione. La soluzione del catalizzatore viene fatta circolare e miscelata con il gas utilizzando il principio del sollevamento aereo. La reazione avviene a circa 130 °C e 400 kPa.
La miscela risultante di acetaldeide, vapore acqueo e gas non convertito viene separata, raffreddata e lavata per separare i prodotti di reazione.
Il gas non convertito viene riciclato nel reattore, con una piccola parte scaricata come gas di scarico per evitare l’accumulo di gas inerte. L’acetaldeide grezza ottenuta dal lavaggio viene quindi distillata in due fasi per ottenere acetaldeide purificata.
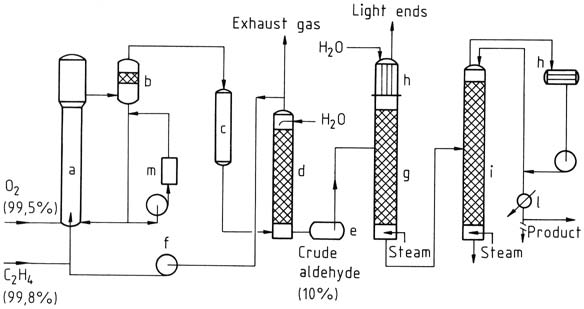
a) Reattore; b) Recipiente di separazione; c) Refrigeratore; d) Scrubber; e) Serbatoio di aldeide grezza; f) Compressore del gas di ciclo; g) Distillazione delle estremità leggere; h) Condensatori; i) Colonna di purificazione; l) Refrigeratore del prodotto; m) Rigenerazione
3.1.2. Processo a due stadi
Il processo a due stadi prevede l’uso di reattori tubolari sia per la reazione che per le fasi di ossidazione. I gas reagiscono quasi completamente in presenza del catalizzatore. L’etilene reagisce a temperature e pressioni più basse e la soluzione del catalizzatore contenente acetaldeide viene quindi espansa in una torre flash.
La miscela di acetaldeide e vapore acqueo viene distillata e il catalizzatore viene riciclato per la reazione con l’etilene. L’acqua di processo viene riutilizzata e una parte viene utilizzata per la depurazione dell’aria e del gas di scarico per rimuovere le impurità. L’acetaldeide grezza viene sottoposta a distillazione a due stadi per ottenere acetaldeide pura.
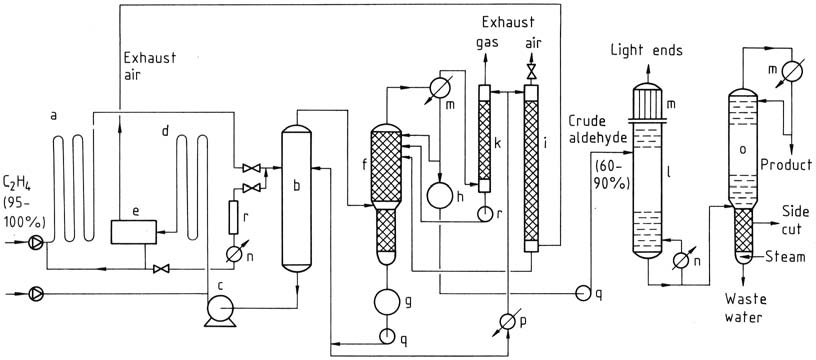
a) Reattore; b) Torre flash; c) Pompa catalizzatrice; d) Reattore di ossidazione; e) Separatore aria di scarico; f) Colonna di aldeide grezza; g) Serbatoio dell'acqua di processo; h) Contenitore di aldeide grezza; i) Depuratore aria di scarico; k) Depuratore gas di scarico; l) Distillazione delle estremità leggere; m) Condensatori; n) Riscaldatore; o) Colonna di purificazione; p) Refrigeratore; q) Pompe; r) Rigenerazione
Sia il processo a uno stadio che quello a due stadi hanno una resa di acetaldeide simile di circa il 95% e costi di produzione comparabili. La scelta tra i metodi dipende da fattori quali la disponibilità di materie prime, considerazioni energetiche e il costo dell’ossigeno.
3.2. Formazione di acetaldeide come sottoprodotto
La generazione di acetaldeide avviene durante il processo di produzione di acetato di vinile da etilene o acetilene. La distillazione viene impiegata per separare l’acetaldeide, che viene successivamente convertita in acido acetico per scopi di riciclaggio.
In una variante specifica del metodo a partire dall’etilene, sia l’acetato di vinile che l’acetaldeide vengono ottenuti in proporzioni molari uguali di 1:1. Questa caratteristica rende il processo quasi autosufficiente in termini di produzione di acido acetico.
3.3. Isomerizzazione dell’ossido di etilene
Prima che l’ossidazione diretta dell’etilene diventasse il metodo preferito, sono state condotte ampie ricerche su questo processo. Sono stati impiegati catalizzatori come Al2O3, SiO2 e sali acidi derivati da acidi minerali come acido solforico, acido fosforico o acido molibdico. Sebbene siano state segnalate rese del 90-95%, questo approccio non ha acquisito una significativa importanza industriale.
4. Produzione da fonti C1
In seguito agli aumenti del prezzo del petrolio nel 1973/74 e nel 1977, i materiali C1 hanno suscitato interesse come materia prima per prodotti chimici organici e come alternative ai prodotti petrolchimici. Tuttavia, in termini di produzione di acetaldeide, i materiali C1 sembrano avere un’importanza limitata poiché la maggior parte dei derivati tradizionali dell’acetaldeide può essere sintetizzata da fonti C1.
4.1. Produzione diretta da gas di sintesi
L’acetaldeide si forma con una selettività relativamente bassa, producendo circa il 30% dal gas di sintesi. La miscela risultante contiene anche acido acetico, etanolo e idrocarburi saturi, principalmente metano. Vengono utilizzati catalizzatori comprendenti composti di cobalto e rodio attivati da composti di iodio o cloruro di magnesio, supportati su un supporto di silicato. Ad oggi, questo processo non ha trovato applicazioni industriali.
4.2. Produzione tramite metanolo, acetato di metile o anidride acetica
L’idroformilazione del metanolo mediante CO/H2, nota come processo oxo, è stata ben consolidata. Questa reazione avviene in presenza di catalizzatori di idroformilazione quali sali di cobalto, nichel e ferro (ad esempio, CoBr2, CoI2) o i corrispondenti carbonili metallici.
Viene condotta a temperature elevate (180-200 °C) e ad alta pressione (30-40 MPa). È stata segnalata una selettività dell’acetaldeide pari o superiore all’80% utilizzando catalizzatori ferro-cobalto carbonile o cobalto-nichel in combinazione con ammine terziarie, fosfine o nitrili.
Analogamente, è stata rivendicata un’elevata selettività per l’idrocarbonilazione dell’acetato di metile utilizzando catalizzatori al palladio o al rodio, accompagnati da fosfine terziarie e composti di iodio, o catalizzatori cobalto-rutenio, in presenza di ioduri di metile e sodio.
Alcuni brevetti descrivono la generazione di acetaldeide tramite la riduzione dell’anidride acetica con idrogeno su catalizzatori al palladio o al platino supportati su un supporto, operando a basse pressioni e temperature moderate. Se il futuro dovesse ridurre l’importanza dell’acetaldeide come intermedio organico, questo metodo potrebbe rivelarsi interessante per produrre economicamente piccole quantità di acetaldeide.
5. Produzione da idrocarburi
L’acetaldeide è un sottoprodotto incidentale nella produzione di acroleina, acido acrilico e ossido di propene dal propene. Inoltre, si forma tramite l’ossidazione di idrocarburi saturi (ad esempio, propano o butano) nella fase gassosa, come implementato da Celanese negli Stati Uniti.
Riferimento
- Acetaldehyde; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_031.pub2
