Piperidina: proprietà, reazioni, produzione e usi
Cos’è la piperidina?
La piperidina, nota anche con altri nomi come esaidropiridina, pentametilenimmina, azacicloesano, ciclopentimmina, cipentil ed esazano, è un’ammina ciclica secondaria con formula chimica C5H11N. Si presenta come un liquido incolore dall’odore forte e sgradevole tipico delle ammine.
La piperidina prende il nome dalla piperina, che contiene piperidina nella sua struttura molecolare come piperidide dell’acido piperico. La piperidina è il composto responsabile del sapore del pepe.
Si trova in natura, soprattutto in alcuni alcaloidi (composti naturali con proprietà medicinali).
Sommario
1. Proprietà fisiche della piperidina
La piperidina è un liquido incolore con odore di ammoniaca, igroscopico e che emette fumi nell’aria. È molto solubile in acqua, alcoli inferiori e chetoni, eteri, idrocarburi alifatici e aromatici, acetato di etile e DMF. La piperidina forma un azeotropo con l’acqua.
La Tabella 1 riassume alcune delle proprietà fisiche della piperidina.
| Proprietà | Valore |
|---|---|
| Numero CAS | [110-89-4] |
| Formula molecolare | C5H11N |
| Massa molecolare | 85,15 g/mol |
| Punto di fusione | -10,5 °C |
| Punto di ebollizione | 106,4 °C (a 101,3 kPa) |
| Densità | 0,8613 g/cm3 |
| Indice di rifrazione | 1,4532 |
| pKa | 11,1 |
| pKb a 25 °C | 2,80 |
| Pressione di vapore a 25 °C | 4,0 kPa |
| Densità di vapore | 3 |
| Calore di combustione a 25 °C | 3453,2 kJ/mol (liquido) |
| Punto di infiammabilità | 4 °C |
2. Reazioni chimiche della piperidina
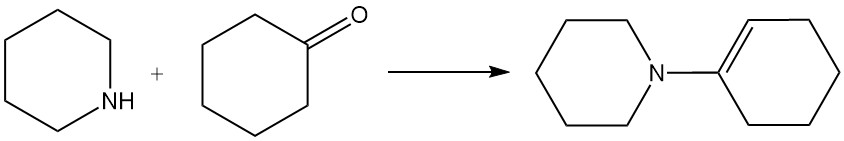
La piperidina reagisce con i chetoni per formare enammine. Ad esempio, reagisce con il cicloesanone per produrre 1-(cicloes-1-en-1-il)piperidina.
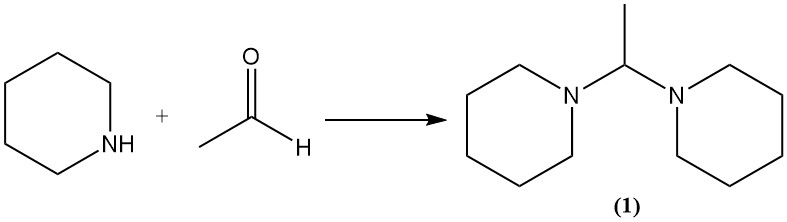
A differenza delle ammine a catena aperta, la piperidina reagisce con le aldeidi per dare amminali come intermedi. Ad esempio, reagisce con l’acetaldeide per formare 1,1′-(etan-1,1-diil)dipiperidina (1).
La piperidina subisce anche reazioni tipiche delle ammine secondarie, come la formazione di sali con acidi, la N-alchilazione, la formazione di ammidi e altre.
La piperidina reagisce con alogenuri alchilici e anidridi acide per formare rispettivamente N-alchilpiperidine e ammidi.
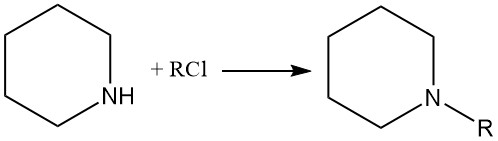
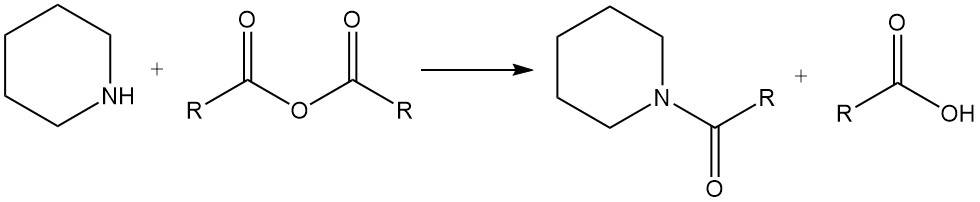
3. Produzione di Piperidina
La piperidina viene prodotta mediante idrogenazione della piridina utilizzando catalizzatori al platino, palladio o nichel Raney in reazioni in fase liquida. La completa saturazione dell’anello piridinico è ottenibile utilizzando una lega nichel-alluminio in ambiente alcalino (0,5 M KOH) a temperatura ambiente con rese dal 51 al 90%.
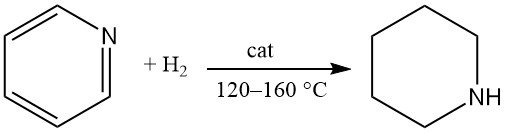
La piridina prodotta dalla distillazione del catrame di carbone è contaminata da composti solforati, che richiedono un processo in due fasi. In primo luogo, la piridina grezza viene idroraffinata utilizzando un catalizzatore metallico solfuro a 280-310 °C; successivamente, viene idrogenata a piperidina utilizzando un catalizzatore nichel-allumina a 120-160 °C.
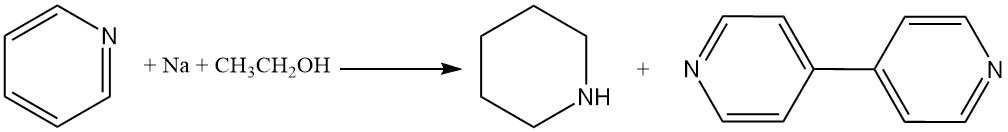
La piperidina può anche essere prodotta trattando la piridina con sodio metallico in etanolo; tuttavia, la reazione di dimerizzazione produce 4,4′-bipiridina come sottoprodotto.
La sintesi della piperidina è possibile anche tramite amminolisi dell’1,5-pentandiolo o dell’alcol tetraidrofurfurilico in condizioni di idrogenazione utilizzando catalizzatori al cobalto o al nichel. Inoltre, l’idrogenazione di glutarati, acido glutarico o glutaraldeide in presenza di un eccesso di ammoniaca produce piperidina.
4. Usi della piperidina
La piperidina è utilizzata come precursore per prodotti farmaceutici, agrochimici, additivi per gomma, tensioattivi e altri composti organici. Grazie alla sua elevata reattività, è spesso utilizzata come intermedio per prodotti farmaceutici e per agenti fitosanitari.
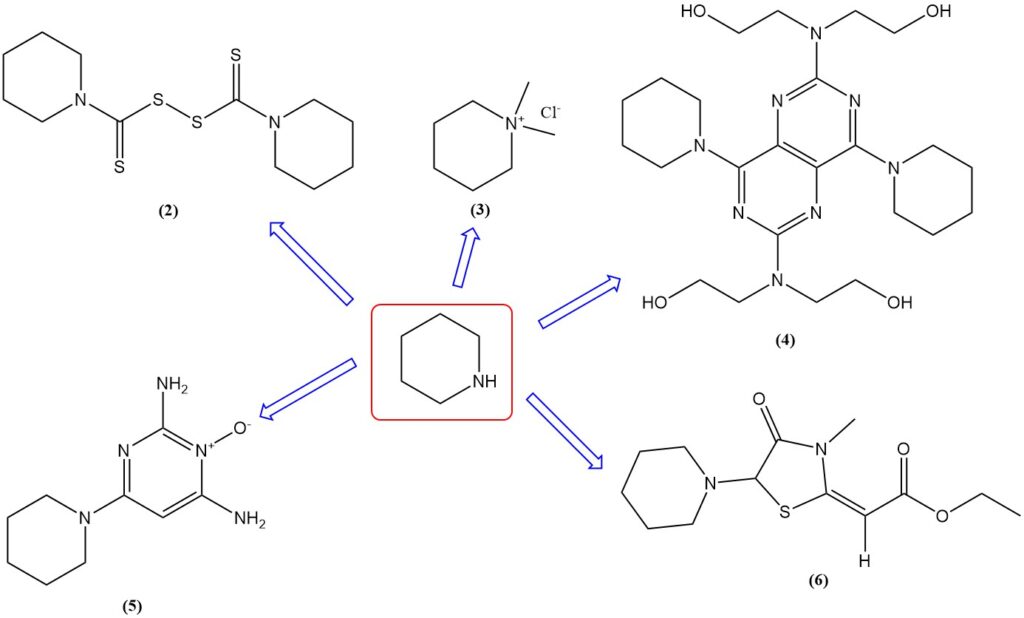
Nell’industria della gomma, la piperidina viene impiegata per produrre acceleratori di vulcanizzazione come il disolfuro di tiurame (2); e viene utilizzata come additivo per oli o carburanti.
Piperidina e acetato di piperidina sono utilizzati come catalizzatori in reazioni di condensazione come la reazione di Knoevenagel, le condensazioni aldoliche e le condensazioni nitroparaffina-aldeide. La piperidina è preferita alle basi più forti in presenza di reagenti o prodotti instabili.
Il dicloruro di mepiquat (3), il sale quaternario dimetilico della piperidina, è utilizzato come regolatore di crescita per le piante di cotone. La piperidina viene utilizzata per produrre vasodilatatori come il dipiridamolo (4) e il minoxidil (5) e diuretici come l’etozolina (6). Viene anche utilizzata come solvente.
La piperidina e alcuni sali di piperidina sono regolamentati negli Stati Uniti dalla Drug Enforcement Agency.
5. Tossicologia della piperidina
La piperidina induce tossicità cutanea acuta, caratterizzata da grave irritazione e ustioni. L’esposizione oculare provoca grave irritazione e potenziali danni alla cornea. L’inalazione può causare irritazione delle vie respiratorie, che si manifesta con tosse e respiro sibilante.
Disturbi gastrointestinali, tra cui nausea, vomito, salivazione e dolore addominale, possono verificarsi a seguito dell’esposizione alla piperidina. Inoltre, la piperidina può causare sintomi neurologici come mal di testa, vertigini, debolezza muscolare, affaticamento, depressione e irritabilità.
Studi a lungo termine sulla piperidina non mostrano prove di cancerogenicità negli studi sugli animali. I dati sulla tossicità riproduttiva indicano un potenziale rischio per il feto. L’esposizione a lungo termine può indurre epatotossicità e nefrotossicità.
Non sono stati stabiliti limiti di esposizione professionale per la piperidina. Tuttavia, ciò non significa che questa sostanza non sia nociva. È importante notare che la piperidina può essere assorbita attraverso la pelle, aumentando così l’esposizione.
La piperidina è una sostanza pericolosa che richiede rigorose misure di sicurezza. Per ridurre al minimo l’esposizione e i potenziali danni, attuare quanto segue:
- Indossare adeguati dispositivi di protezione individuale, inclusi guanti, occhiali protettivi e indumenti protettivi.
- Garantire un’adeguata ventilazione nelle aree di lavoro.
- Mantenere una buona igiene personale, incluso il frequente lavaggio delle mani.
- Predisporre postazioni lavaocchi e docce di sicurezza.
- Conservare la piperidina in un luogo fresco, asciutto e ben ventilato, lontano da sostanze incompatibili.
- Utilizzare tecniche di manipolazione appropriate per prevenire fuoriuscite e perdite.
- Predisporre un piano di intervento in caso di fuoriuscita.
- Smaltire la piperidina e i rifiuti contaminati secondo le normative vigenti.
- Fornire una formazione completa al personale sui pericoli, sulla manipolazione e sulle procedure di emergenza.
Riferimenti
- Amines, Aliphatic, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_001.pub2
- Pyridine and Pyridine Derivatives. – https://onlinelibrary.wiley.com/doi/10.1002/0471238961.1625180919031809.a01.pub2
- https://onlinelibrary.wiley.com/doi/10.1002/14356007.a22_399
- https://www.sciencedirect.com/science/article/abs/pii/B9780123852359000059
- https://nj.gov/health/eoh/rtkweb/documents/fs/1543.pdf
- https://pubchem.ncbi.nlm.nih.gov/compound/Piperidine
