Acido fumarico: proprietà, produzione e usi
Cos’è l’acido fumarico?
L’acido fumarico, noto anche come acido trans-butenedioico, è un acido dicarbossilico con formula C4H4O4. È ampiamente presente in natura e si presenta come un solido cristallino bianco dal sapore fruttato.
L’acido fumarico fu isolato per la prima volta dalla fumaria (Fumaria officinalis) da Winckler nel 1832. Successivamente fu identificato con vari nomi, tra cui acido boletico, acido glaucina, acido lichenico e acido paramaleico.
L’acido fumarico è ora prodotto industrialmente, sebbene sia meno importante rispetto all’anidride maleica.
Sommario
1. Proprietà fisiche dell’acido fumarico
L’acido fumarico cristallizza sotto forma di prismi monoclini. È solubile in etanolo e acido solforico concentrato, leggermente solubile in etere etilico e acetone e insolubile in cloroformio e benzene. Una soluzione acquosa allo 0,05% di acido fumarico a 25 °C ha un pH compreso tra 3,0 e 3,2.
Le principali proprietà fisiche dell’acido fumarico sono riassunte nella tabella seguente.
| Proprietà | Valore |
|---|---|
| Numero CAS | [110-17-8] |
| Formula chimica | C4H4O4 |
| Peso molecolare | 116,07 g/mol |
| Punto di fusione | 286–287 °C (tubo chiuso) |
| Sublimazione temperatura | 200 °C |
| Densità (solido) | 1,635 g/cm3 |
| Calore di sublimazione (92 °C) | 136,1 kJ/mol |
| pKa1 | 3,02 |
| pKa2 | 4,38 |
| Solubilità in 100 g di acqua | 0,428 g (a 15,5 °C) |
| 9,97 g (a 100 °C) | |
| Punto di infiammabilità | 273 °C (vaso aperto) 230 °C (vaso chiuso) |
| Temperatura di autoaccensione | 375 °C (polvere) |
2. Proprietà chimiche dell’acido fumarico
L’acido fumarico sublima senza decomposizione a temperature pari o leggermente superiori a 200 °C, ma se riscaldato a temperature superiori a 230 °C, si decompone formando anidride maleica, acqua e una quantità significativa di residuo. La presenza di anidride fosforica catalizza la formazione di anidride maleica.
L’acido fumarico è l’isomero trans dell’acido maleico e condivide con esso molte proprietà chimiche. Tuttavia, le reazioni dell’acido fumarico procedono generalmente lentamente, in parte a causa della sua minore solubilità in acqua.
A differenza dell’acido maleico, l’acido fumarico può formare un cloruro acilico. (Per maggiori dettagli sulle reazioni, consultare l’articolo sull’acido maleico.)
3. Produzione dell’acido fumarico
L’acido fumarico viene prodotto principalmente per isomerizzazione dell’acido maleico o dell’anidride maleica (Figura 1). Questi materiali di partenza provengono spesso da flussi di acqua di lavaggio generati durante la produzione di anidride maleica o anidride ftalica, con una concentrazione minima preferita di acido maleico del 30%.
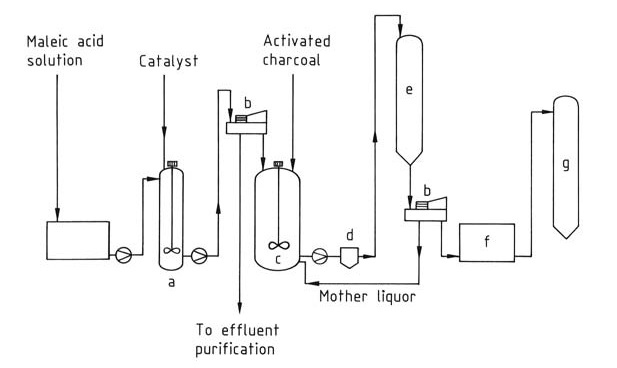
a) Recipiente di isomerizzazione; b) Centrifuga; c) Vasca di dissoluzione; d) Filtro; e) Cristallizzatore; f) Essiccatore; g) Silo
Il processo di isomerizzazione converte l’acido maleico in modo quasi quantitativo nell’acido fumarico, meno solubile, che viene poi separato per filtrazione. Questa conversione può essere ottenuta mediante trattamento termico o con l’ausilio di catalizzatori. Sono stati esplorati diversi catalizzatori, tra cui:
- Acidi minerali (ad esempio, acido cloridrico)
- Composti a base di zolfo come tiocianati, tiazoli, tiosemicarbazidi e tiourea
- Composti del bromo combinati con perossidi (ad esempio, persolfato)
Tra questi, la tiourea è il catalizzatore più comunemente utilizzato nel settore.
L’acqua di lavaggio del materiale di partenza può contenere impurità che influiscono sulla qualità e sulla resa del prodotto. Questo problema può essere evitato pretrattando termicamente l’acqua di lavaggio, aggiungendo urea insieme alla tiourea come catalizzatore, oppure aggiungendo solfiti o anidride solforosa gassosa, seguiti da acidi minerali.
L’acido fumarico grezzo ottenuto viene purificato mediante ricristallizzazione dall’acqua e trattamento con carbone attivo. Questi processi di purificazione comportano una perdita di prodotto di circa il 10%.
La produzione di acido fumarico è solitamente un’operazione a lotti, sebbene esistano processi in continuo. Si raccomanda la scelta di apparecchiature in acciaio austenitico resistente alla corrosione, soprattutto se il processo non prevede l’uso di acido cloridrico.
Lo smaltimento delle acque madri residue dalla fase di isomerizzazione rappresenta una sfida a causa della presenza di impurità solubili e del catalizzatore utilizzato. La combustione rappresenta una potenziale soluzione per questo flusso di rifiuti.
Un metodo di produzione alternativo, impiegato negli Stati Uniti, utilizza la fermentazione di monosaccaridi o amidi con ceppi fungini specifici come Mucor, Aspergillus e Rhizopus.
4. Usi dell’acido fumarico
L’acido fumarico è un comune additivo alimentare (E297) utilizzato come acidificante o agente acidificante per esaltare il sapore di prodotti come bevande, prodotti da forno (in particolare pane di segale e a lievitazione naturale) e ripieni. Inoltre, agisce come conservante prolungando la durata di conservazione di prodotti come le tortillas di grano.
L’acido fumarico è stato utilizzato in farmaci orali ed è oggetto di studio per il suo potenziale ruolo nel trattamento della psoriasi.
Viene utilizzato come intermedio nella produzione di vari prodotti chimici e in cosmetici (ad esempio, sali da bagno e detergenti per protesi dentarie).
L’acido fumarico è spesso preferito all’acido maleico per la produzione di poliesteri e copolimeri. Durante il processo di produzione di questi prodotti, l’isomerizzazione porta a una miscela pressoché equivalente di isomeri trans e cis degli acidi dicarbossilici, indipendentemente dal materiale di partenza (acido maleico o fumarico).
Tuttavia, l’acido fumarico è preferito per il suo profilo di sicurezza (natura innocua). In alcuni casi, l’uso di acido fumarico può portare a effetti specifici, come l’aumento della durezza in alcune resine.
L’acido fumarico (fumaril) e il fumarato di ferro (II) sono utilizzati come additivi specializzati nei mangimi per animali.
5. Tossicologia dell’acido fumarico
L’acido fumarico è un prodotto naturale con un profilo di sicurezza favorevole (non tossico) basato su diversi studi.
Studi su animali indicano una bassa tossicità acuta. I valori di LD50 orale nei ratti superano i 10 g/kg di peso corporeo e l’applicazione cutanea nei conigli fino a 20 g/kg non si è rivelata letale.
La somministrazione a lungo termine di acido fumarico alla dose di 8 mg/kg di peso corporeo al giorno per un anno nell’uomo non ha causato alterazioni della funzionalità ematica, urinaria o epatica.
Non sono state osservate prove di effetti genotossici (danni al DNA), cancerogenicità (causa di cancro) o tossicità riproduttiva negli esperimenti.
Tuttavia, l’acido fumarico può agire come irritante locale. È classificato come leggermente irritante per la pelle e moderatamente irritante per gli occhi e le mucose in caso di contatto.
Riferimenti
- Maleic and Fumaric Acids; ULLMANN’S Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_053
- https://pubchem.ncbi.nlm.nih.gov/compound/Fumaric-Acid
