Nitrobenzoëzuur: eigenschappen, reacties en productie
Nitrobenzoëzuren zijn derivaten van benzoëzuur met de algemene formule C7H5NO4. Twee isomeren (meta en para) zijn commercieel belangrijk. Nitrobenzoëzuren zijn ongeveer tien keer zuurder dan benzoëzuur vanwege de aanwezigheid van de nitrogroep.
Inhoudsopgave
2-Nitrobenzoëzuur of o-nitrobenzoëzuur

2-Nitrobenzoëzuur is mononitrobenzoëzuur waarbij de nitrogroep zich op positie ortho ten opzichte van de carboxylgroep bevindt. Het is een vaste stof die onoplosbaar is in water en oplosbaar in alcohol zoals methanol.
Fysische eigenschappen van 2-nitrobenzoëzuur
De fysische eigenschappen van 2-nitrobenzoëzuur worden hieronder vermeld:
- Molaire massa = 167,12 g/mol
- Smeltpunt = 148 °C
- Dichtheid = 1,575
- Oplosbaarheid in water = 0,75 g/100 ml (bij 25 °C)
- Oplosbaarheid in methanol = 42,72 g/100 ml (bij 10 °C)
- Oplosbaarheid in benzeen = 0,294 g/100 ml (bij 10 °C)
- Dissociatieconstante, Ka (bij 18 °C) = 6,1 × 10-3
- Decarboxyleringstemperatuur = 180 °C
Chemische reacties van 2-nitrobenzoëzuur
2-nitrobenzoëzuur ondergaat de typische reactie van aromatische carbonzuren en nitroaromatische verbindingen:
Anthranilzuur kan worden geproduceerd door de reductie van de nitrogroep tot een amine.
De carbonzuurgroep vormt esters met alcoholen en 2-nitrobenzoylchloride met chloreringsmiddelen.
Bij temperaturen boven 180 °C vormt 2-nitrobenzoëzuur nitrobenzeen door decarboxylering.
De aromatische ring kan substitutiereacties ondergaan, maar het is moeilijk vanwege de aanwezigheid van deactiverende groepen.
Productie van 2-Nitrobenzoëzuur
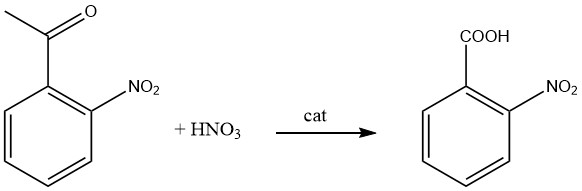
2-Nitrobenzoëzuur wordt bereid door de oxidatie van 2-nitrotolueen met salpeterzuur.

Monsanto Chemicals Ltd. had een productiemethode ontwikkeld voor 2-nitrobenzoëzuur door oxidatie van 2-nitroacetfenon met waterig salpeterzuur in aanwezigheid van ammoniummetavanadaat als katalysator onder reflux.
Acht mol salpeterzuur zijn nodig om één mol 2-nitroacetofenon bij een temperatuur van 60 °C om te zetten naar de refluxtemperatuur van het mengsel.
Door het reactiemengsel te koelen, vormen zich de ruwe 2-nitrobenzoëzuurkristallen en worden daaruit gewonnen door filtratie, en vervolgens gezuiverd door herkristallisatie uit oplosmiddelen zoals benzeen, ethanol, benzeen-ethanolmengsels, hexaan, enz.
3-nitrobenzoëzuur of m-nitrobenzoëzuur

3-Nitrobenzoëzuur is een witte vaste stof. De carbonzuur- en nitrosubstituenten bevinden zich in een metapositie ten opzichte van elkaar, daarom wordt het ook wel m-nitrobenzoëzuur genoemd. Het is een belangrijke voorloper bij de productie van kleurstoffen.
Fysische eigenschappen van 3-nitrobenzoëzuur
De fysische eigenschappen van 3-nitrobenzoëzuur worden hieronder vermeld:
- Molaire massa = 167,12 g/mol
- Smeltpunt = 142 °C
- Dichtheid = 1,494
- Oplosbaarheid in water = 0,24 g/100 ml (bij 15 °C)
- Oplosbaarheid in methanol = 47,34 g/100 ml (bij 10 °C)
- Oplosbaarheid in benzeen = 0,795 g/100 ml (bij 10 °C)
- Dissociatieconstante, Ka (bij 25 °C) = 3,48 × 10-4
- Decarboxyleringstemperatuur = 238 °C
Chemische reacties van 3-nitrobenzoëzuur
3-nitrobenzoëzuur ondergaat de typische reactie van aromatische carbonzuren en nitroaromatische verbindingen:
3-aminobenzoëzuur kan worden geproduceerd door de reductie van de nitrogroep tot een amine.
De carbonzuurgroep vormt esters met alcoholen en 3-nitrobenzoylchloride met chloreringsmiddelen.
Bij temperaturen boven 238 °C vormt 3-nitrobenzoëzuur nitrobenzeen door decarboxylatie.
De aromatische ring kan substitutiereacties ondergaan, maar dit is moeilijk vanwege de aanwezigheid van deactiverende groepen.
Productie van 3-nitrobenzoëzuur
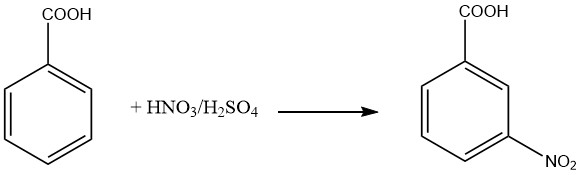
Het 3-nitrobenzoëzuur wordt bereid door de nitrering van benzoëzuur onder lage temperatuuromstandigheden. Tijdens dit proces worden ongeveer 20% van het 2-nitro-isomeer en 1,5% van het 4-nitro-isomeer geproduceerd naast het gewenste 3-nitrobenzoëzuur. Om gezuiverd 3-nitrobenzoëzuur te verkrijgen, kan herkristallisatie van het natriumzout worden toegepast.
Een hogere opbrengst van 3-nitrobenzaldehyde, een voorloper van 3-nitrobenzoëzuur, kan worden bereikt door de gecontroleerde oxidatie van benzaldehyde. 3-nitrobenzoëzuur dient als een tussenproduct in de synthese van 3-aminobenzoëzuur en azokleurstoffen. Het derivaat ervan, 4-chloor-3-nitrobenzoëzuur, fungeert als een tussenproduct in de productie van kleurstoffen.
4-nitrobenzoëzuur of p-nitrobenzoëzuur
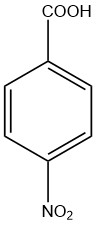
4-nitrobenzoëzuur is een mono-nitrobenzoëzuur met de twee groepen in een para-positie ten opzichte van elkaar. Het wordt ook wel para-nitrobenzoëzuur genoemd. Het is een lichtgele vaste stof die onoplosbaar is in water en licht oplosbaar in methanol.
Fysische eigenschappen van 4-nitrobenzoëzuur
De fysische eigenschappen van 4-nitrobenzoëzuur zijn de volgende:
- Molaire massa = 167,12 g/mol
- Smeltpunt = 240 °C
- Dichtheid = 1,61
- Oplosbaarheid in water = 0,02 g/100 ml (bij 15 °C)
- Oplosbaarheid in methanol = 9,6 g/100 ml (bij 10 °C)
- Oplosbaarheid in benzeen = 0,017 g/100 ml (bij 12,5 °C)
- Dissociatieconstante, Ka (bij 25 °C) = 3,93 × 10-4
- Decarboxylatietemperatuur > 240 °C
Chemische reacties van 4-nitrobenzoëzuur
4-nitrobenzoëzuur ondergaat de typische reactie van aromatische carbonzuren en nitroaromatische verbindingen:
4-aminobenzoëzuur kan worden geproduceerd door de reductie van de nitrogroep tot een amine.
De carbonzuurgroep vormt esters met alcoholen en 4-nitrobenzoylchloride met chloreringsmiddelen, wat een uitgangsmateriaal is voor procaïnehydrochloride en foliumzuur.
Bij temperaturen boven 240 °C, 4-nitrobenzoëzuur vormt nitrobenzeen door decarboxylatie.
De aromatische ring kan substitutiereacties ondergaan, maar dit is moeilijk vanwege de aanwezigheid van deactiverende groepen.
Productie van 4-nitrobenzoëzuur
4-Nitrobenzoëzuur wordt commercieel geproduceerd door de oxidatie van 4-nitrotolueen met moleculaire zuurstof. Oxidatie met 15% salpeterzuur bij 175 °C produceert het zuur in 88,5% opbrengst.

Monsanto Chemicals Ltd. had een productiemethode ontwikkeld voor 4-nitrobenzoëzuur door oxidatie van 4-nitroacetfenon met waterig salpeterzuur in aanwezigheid van ammoniummetavanadaat als katalysator onder reflux.
Acht mol salpeterzuur zijn nodig om één mol 4-nitroacetofenon bij een temperatuur van 60 °C om te zetten naar de refluxtemperatuur van het mengsel.
Door het reactiemengsel te koelen, vormen zich de ruwe 4-nitrobenzoëzuurkristallen en worden daaruit gewonnen door filtratie, en vervolgens gezuiverd door herkristallisatie uit oplosmiddelen zoals benzeen, ethanol, benzeen-ethanolmengsels, hexaan, enz.

Een interessante methode omvat de nitrering en daaropvolgende oxidatie van polystyreen. Deze methode gebruikt de sterische hindering van de polymeerketen om de para-tot-orthoverhouding van het product te verbeteren.
Referenties
- Benzoic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a03_555
- Preparation of 2-and 4-nitrobenzoic acid. – https://patents.google.com/patent/US2695311A/en
